2023-01-17 来源 : 国家自然科学基金委员会
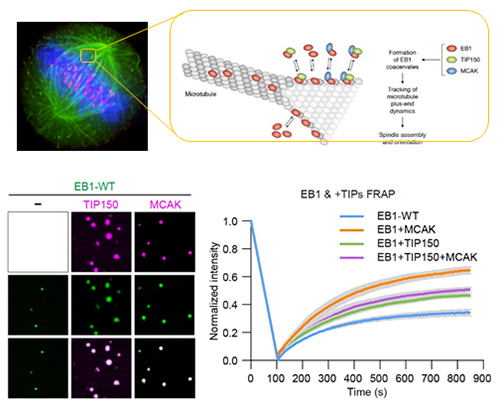 |
图 EB1蛋白相分离调控细胞分裂纺锤体微管可塑性的示意图 在国家自然科学基金项目(批准号:32090040、91854203、31621002、21922706)等资助下,中国科学技术大学姚雪彪课题组与合作者开展研究,阐明了末端结合蛋白(End-binding protein,EB1蛋白)相分离调控细胞分裂纺锤体微管可塑性的物理化学机制,在解析生物大分子凝聚态调控细胞命运可塑性的研究领域迈出了重要一步。相关研究成果以“EB1蛋白相分离引导微管正端动态(Phase separation of EB1 guides microtubule plus-end dynamics)”为题,于2022年12月19日发表在《自然·细胞生物学》(Nature Cell Biology)杂志上。论文链接:https://www.nature.com/articles/s41556-022-01033-4。 细胞是生命活动的最小功能单元,生物大分子通过构筑形态与功能各异的区室,精准催化生物化学反应,调控细胞稳态与增殖。细胞骨架是其区室化的物质基础,调控细胞生长、形态变化、细胞间信息交流与命运决定可塑性。2009年,姚雪彪课题组发现并克隆了一个新颖的EB1结合蛋白TIP150。TIP150含有典型EB1结合蛋白基序SxIP,负责招募微管解聚酶MCAK,在动态组装微管的正末端形成催化区室。在此基础上,课题组与其他研究者合作采用单分子技术TIRFM与FRET,解析了EB1与TIP150的动态作用机制与化学基础。 为进一步明确EB1蛋白的相分离特征与凝聚态物质基础,课题组与中国科学技术大学刘行教授等合作,利用结构光照明显微成像技术发现了EB1蛋白在活细胞动态微管追踪过程的液滴表征,随后利用基因编辑、物理化学模拟碱性氨基酸的丰度与间隔,并结合超高分辨成像,解析了相分离驱动EB1蛋白的微管正端追踪功能。该研究成果为后续生物大分子凝聚态调控细胞分裂质量控制与命运决定可塑性的研究奠定了基础(图)。 该研究成果是由单分子追踪、物理化学建模、核磁谱学以及细胞动力学的交叉团队协作完成的。武汉大学姜恺教授,中国科学院生物物理研究所李栋研究员,中国科学院分子细胞卓越创新中心李林研究员,湖南大学袁凯教授、清华大学李丕龙教授,中国科学技术大学项晟祺教授、许超教授、符传孩教授、臧建业教授、侯中怀教授和施蕴渝教授等课题组参与了该项研究。
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。





发表评论
注册或登后即可发表评论
登录注册
全部评论(0)