话说制药界,十年河东,十年河西。
2000年由辉瑞研发的第一代ADC药物Mylotarg获FDA批准上市,但终因毒副作用于2010年退市。
十年前,Seattle Genetics(现已更名为Seagen)以及Immunogen的2代ADC药物Adcetris及T-DM1(Kadcyla)先后上市,开启了ADC治疗的新纪元。当时这两家Biotech无疑是ADC领域的龙头企业,引来众多Big Pharma与之合作。
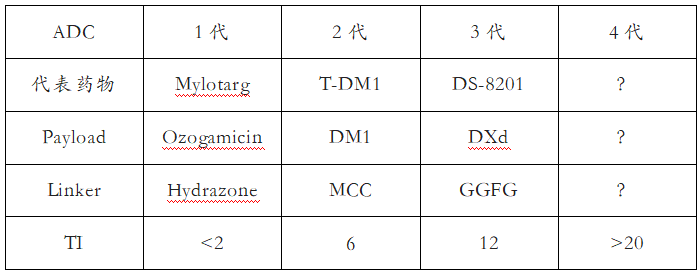
彼时,在ADC领域,第一三共还是一家默默无闻的企业。而今天,第一三共凭借其DS-8201惊艳的临床数据让业界折服,成为当之无愧的第三代ADC的霸主。往后再推十年后,我们能不能看到第四代ADC药物的获批上市?要回答这个问题,我们不妨先预测一下四代ADC长什么样、需要达到怎样的治疗效果。ADC从本质上来说是一种靶向化疗药,其目的是为了扩大治疗窗(Therapeutic Index; TI)(图1)。以既往ADC的TI来看,治疗窗呈现显著递增的趋势(表1),从第一代的不到2倍提高到如今第三代的12倍,由此推测(以Her2为靶点的)第四代ADC的治疗窗应该会达到20倍以上。
图1. ADC增大化疗药物治疗窗
如果说更大的治疗窗是为了使更多的患者受益(更高的ORR),那么,怎样使患者更长时间受益则是药物研发的更高目标,最终将癌症变为一种可控的慢性疾病。
然而,目前几乎所有的药物(化疗、靶向和免疫药物),随着患者使用时间的延长,癌症会对药物产生耐药,使得药物对癌细胞的作用停止。癌细胞的耐药性是癌症治疗失败的主要原因之一,这可能导致癌症很快复发/疾病进展,最终造成患者死亡。
以DS-8201治疗无法切除或转移性HER2低表达(HER2-low)乳腺癌患者为例,在HR+和总人群中,治疗组的mPFS分别为10.1和9.9个月,TPC对照组分别为5.4个月和5.1个月;mOS分别为23.9和23.4个月,TPC对照组分别为17.5个月和16.8个月。尽管DS-8201已经有了很大提高,但是距离将癌症变为可控的慢性疾病还相距甚远。因此,如何进一步延长mPFS以及mOS是四代ADC成功的关键。
要想设计出有更大TI,更长mPFS以及mOS的四代ADC,或许可以从ADC的耐药机制着手。研究表明,ADC至少有以下8种不同的耐药机制[1]。
靶点抗原改变
肿瘤是一种高度异质性的组织,存在基因与表型的不稳定性,同时肿瘤微环境中表达各种不同的蛋白酶会对肿瘤表面抗原进行剪切,从而使靶点抗原与ADC的结合表位缺失。此外,有些靶点抗原与ADC的结合表位同时也结合配体或其它蛋白,如果此类蛋白表达升高则会与ADC形成竞争结合靶点抗原。癌细胞还可以直接通过基因水平下调甚至关闭靶点抗原的表达。使用高效的旁观者杀伤效应(Bystander Killing)的第三代ADC,或靶向同一抗原的2个不同表位,或共表达在同一细胞上的2个不同抗原的双抗ADC,可以在一定程度上解决这一耐药问题。
内吞途径改变
目前的ADC几乎都依赖于细胞表面抗原介导ADC内吞进入细胞,然后经由胞内体(Endosome)到达溶酶体(Lysosome)实现ADC降解释放出毒素杀伤细胞。有研究表明,癌细胞可通过改变某些参与内吞转运的蛋白(如小窝蛋白Caveolae)的表达从而改变ADC内吞的路线使其无法到达溶酶体而产生耐药,针对这种耐药机制,目前Pyxis Oncology正在研发一种不需要内吞、靶向细胞外基质靶点Oncofetal Fibronectin Extradomain-B (EDB)的ADC,其Payload通过组织蛋白酶(Cathepsin)剪切释放然后进入细胞进行杀伤。
溶酶体的改变
不少在研ADC的Linker利用pH敏感型水解模式在溶酶体的酸性(pH4.8)环境下发生水解释放毒素,而有些癌细胞能够升高溶酶体的pH从而使毒素无法释放。如果能够找到一种在胞内体的弱酸(pH6.5)环境中发生水解的Linker则能规避这种耐药问题。
药物外排泵表达及活性增加
相当数量的肿瘤高表达ATP结合盒式蛋白(ATP-binding cassette transporter,ABC),这是一类ATP驱动泵,能将小分子药物从细胞中排出,从而抑制药物的细胞毒性作用。包括MMAE在内的许多ADC Payload是ABC的底物,因此ABC的高表达也能引起这类ADC的耐药。解决方法主要有2种:选择非ABC底物的毒素作为Payload或将ADC与相应的ABC抑制剂联用。
细胞周期改变
由于现有的Payload的杀伤机制大多基于细胞周期调控,而癌细胞可以通过调节细胞周期而对Payload的杀伤产生逃逸。对于此类耐药问题,选择可杀伤静息状态细胞的Payload(比如PBD)可以解决。
DNA损伤修复(DDR)通路改变
对于通过DNA损伤产生杀伤作用的Payload,癌细胞可以通过DNA损伤修复通路的改变产生耐药。针对此类耐药机制,可以选择与DNA损伤修复通路的相应抑制剂联用的方法,比如Topotecan联用ATR抑制剂在小细胞肺癌(SCLC)中就取得了不错的疗效。
凋亡通路改变
Payload毒素要想杀伤细胞最终都要依赖于细胞凋亡通路,而癌细胞的凋亡通路有时因异于正常细胞而不能发挥作用,比如高表达抗凋亡蛋白 BCL-2 和 BCL-XL从而引起ADC耐药,业内已有选择BCL-XL抑制剂作为ADC Payload或将BCL-XL抑制剂与ADC联用的尝试。
下游信号通路改变
PI3K/AKT作为癌细胞重要的信号通路节点蛋白,在相当数量的癌症患者中发生突变,对细胞周期、凋亡都产生重要影响从而导致癌细胞对ADC耐药,已有报道显示PI3K/AKT的抑制剂与ADC联用显现出一定药效。第四代ADC分子设计
抗体
在第二、三代ADC中,抗体部分并没有做太大的改变,比如T-DM1与DS-8201均使用Herceptin,因此第四代ADC抗体部分还有很大的提升空间。如果是确定靶点的单抗ADC,首先要评估该靶点在肿瘤组织及正常组织的表达差异,筛选合适的抗体亲和力及内吞效率以期达到抗体能有效的结合癌细胞并内吞但对表达该靶点的正常细胞结合较弱、内吞较少。这种筛选策略可以借鉴TeneoBio筛选CD3抗体的方法,在能激活T细胞的前提下尽量减小细胞因子释放从而获得最大的安全窗。
此外还可以将单抗做成Conditional Antibody,只在肿瘤微环境中才被激活从而提高治疗窗。Cytomx、BioAlta、Adagene等公司已经在做这方面的尝试。如果是双抗ADC,问题则要复杂得多。从目前市场上的研发情况来看主要可以分为2大类:一类是靶向同一抗原的2个不同结合表位(Epitope),以增强亲和力及内吞,代表药物如再生元的cMet/cMet双抗ADC(REGN5093-M114)及Zymeworks的Her2/Her2双抗ADC(ZW49);另一类是靶向同一癌细胞上的2个不同抗原,以增强癌症组织靶向特异性及内吞,代表药物如德国默克/Sutro的EGFR/MUC1双抗ADC(M1231)。第一类双抗ADC在增强对癌细胞的亲和力及内吞的同时也有可能增强对正常细胞的亲和力及内吞,因此治疗窗是否能够增大存在疑问,比如阿斯利康的Her2/Her2双抗ADC(MEDI4276)因毒性原因已止步于I期临床。后一类双抗ADC在靶点选择方面需要谨慎,仅仅是癌细胞共表达2个抗原不能作为双抗ADC的立项依据。以EGFR/MUC1为例,尽管EGFR在多种肿瘤中高表达,但由于其在上皮细胞中也高表达,导致EGFR-ADC无法提供足够的治疗窗。而MUC1在肿瘤中出现异常糖基化可被抗体识别,因此MUC1-ADC可提供更大的治疗窗。如果仅考虑EGFR/MUC1共表达这一方面,那么MUC1-ADC显然具有比EGFR/MUC1双抗ADC更明显的安全优势。双抗ADC必须要提供比单抗ADC更大的治疗窗才有开发的意义。要筛选到具有更大治疗窗的双抗ADC,则需要通过合适的体外实验筛选2个抗体的亲和力、选择合适的双抗Format(1:1, 2:1, 2:2),最后通过体内药效及毒性实验确定其治疗窗。
Payload
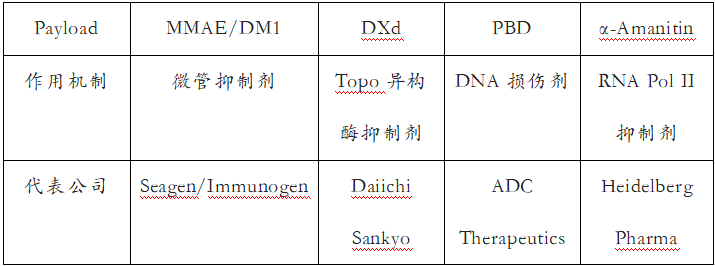
纵观不同研发阶段的Payload大体可以分为4类(表2)。其中,以MMAE、DM1为代表的微管抑制剂是第二代ADC的经典Payload,目前仍被广泛使用;以喜树碱衍生物DXd为代表的Topo异构酶抑制剂是第三代ADC的明星Payload;以PBD为代表的DNA损伤剂也是经典的ADC Payload,已经历了20多年的研究改进,除了2021年获批上市的ADC Therapeutics 的Loncastuximab Tesirine-lpyl(CD19-PBD)外,还有多款ADC目前在临床阶段;其它还有一些小众的ADC Payload近来也逐渐进入大家的视线,如德国公司Heidelberg Pharma研发的RNA Pol II抑制剂α-鹅膏蕈碱(α-Amanitin)及美国公司Mersana研发的STING激活剂Payload ImmunoLock。
越来越多研究表明,由于不同肿瘤存在巨大差异,没有一种Payload可以对所有癌种有效,因此在靶点及抗体确定以后筛选Payload也是第四代ADC设计的要素之一。如第一三共并没有止步于获得巨大成功的DXd,而是又开发了PBD作为其另一Payload。此外,双Payload ADC也正从实验室的概念走向工业界探索[2],但是由于其高研发成本及高技术难度使得大多数企业望而却步。表2. 不同Payload比较
另一种开发第四代ADC Payload的思路,是将Payload做成前药(Prodrug),即只在进入癌细胞内才被激活释放产生杀伤作用,从而进一步增强药物特异性及治疗窗。韩国公司LegoChemBio研发的dPBD就是这方面的代表分子,目前这家公司已有2款ADC在临床阶段,其临床治疗结果值得期待。目前业内对于Payload的研发有2个方向:一是高DAR值中低毒素,另一是低DAR值高毒素,如何选择不能一概而论而需要根据具体实验数据决定。
Linker
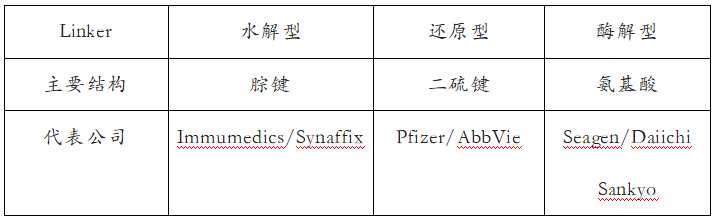
Linker按其作用机制可以分为Cleavable(可剪切)和Non-Cleavable(不可剪切)。目前业内的共识是针对实体瘤Cleavable Linker可更好的提供旁观者杀伤效应。而旁观者杀伤机制也是DS-8201取得巨大成功的法宝。Cleavable Linker按其化学结构或剪切机制可以分为3类(表3)。一类是依赖于酸水解的腙键Linker;第二类是依赖于细胞内谷胱甘肽(GSH)进行还原剪切的二硫键Linker;另一类是由多个氨基酸组成的肽段的酶降解Linker。已有的数据显示,酶降解Linker如果选择肿瘤细胞溶酶体高表达酶的底物可以提供额外的特异性进而增大治疗窗。理想的Linker在整个ADC分子中起到平衡作用,它平衡Payload的疏水性、增强Linker-Payload以及整个ADC分子的稳定性,Linker-Payload即使在血液中从抗体上脱落也很难进入细胞造成毒性。因此,设计Linker一定是要与Payload一起综合考虑。
Conjugation
ADC的偶联方式从最早的随机偶联到半胱氨酸半定点偶联再到现在的定点偶联,技术日趋成熟,ADC产物的均一性也在不断提高。定点偶联获得的产物均一性高可降低杂质带来的毒性及不稳定性,因此预计将成为第四代ADC的标配。比较成熟的定点偶联可以分为四类(表4):工程化半胱氨酸(THIOMAB)偶联、非天然氨基酸(nnAA)偶联、N297糖基偶联和抗体轻链(或重链)C端连接短肽偶联。其中,非天然氨基酸偶联方法技术难度最高,目前主要是Ambrx及Sutro在使用。工程化半胱氨酸偶联由于需要引入非配对的半胱氨酸可能引起抗体聚集,因而给CMC带来挑战。N297糖基偶联目前是最被业界接受的定点偶联方式,该技术的代表公司Synaffix已向多家ADC公司转让了其N297糖基偶联技术GlycoConnect。值得一提的是,第一三共在DS-8201中使用了半胱氨酸偶联,但其近期公开的专利显示其已开发出自己的N297糖基定点偶联技术用于下一代ADC的开发。第四代ADC需具备更大的治疗窗及(部分)解决3代ADC的耐药问题,就得从抗体、Payload、Linker、偶联、联用等多方面入手并进行综合改造优化,对ADC某一部分的改造或许已不能实现迭代,比如刚刚被GSK重金买入的XMT-2056虽然还不能称为第四代ADC,但临床前数据表明XMT-2056+DS-8201有叠加效果,临床上是否能进一步延长患者的生存时间尚待验证。
第三代ADC DS-8201给癌症治疗领域,特别是针对Her2低表达/Her2突变的癌症治疗带来了革命性的突破。期待有更多新技术加持的第四代ADC,结合适当的转化医学研究为癌症患者带来更好更持久的治疗效果。
1.Novel ADCs and Strategies to Overcome Resistance to Anti-HER2 ADCs. Cancers (Basel). 2021;14(1):154.
2.Antibody-drug conjugates with dual payloads for combating breast tumor heterogeneity and drug resistance. Nature Communications. 2021;12:352
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。







发表评论
注册或登后即可发表评论
登录注册
全部评论(0)