● 治疗HCV的HCV NS3/4A丝氨酸蛋白酶抑制剂
今天,我们主要综述治疗新冠病毒的主要3CL蛋白酶抑制剂(Mpro,CL代表类凝乳胰蛋白酶)。
在新冠病毒分子结构内部,其主蛋白酶(Mpro)负责多蛋白pp1a和pp1ab的多点位切割。生成的多蛋白片段是功能性的非结构蛋白,它们逐渐成熟,参与病毒复制机制,从而制造新的病毒。
Mpro可以控制病毒复制,也因此被认为是一个成功的靶点,拟开发以此为靶向的抗病毒药物。

Mpro是一种半胱氨酸蛋白酶,以Cys145-His41为特征,位于结构域I和结构域II之间的裂口的催化二元体。大多数的蛋白酶抑制剂都是通过与催化三元体相互作用发挥作用。[1]
早在2002年,为了发现治疗非典(SARS)的药物,辉瑞公司进行了基于荧光共振能量转移(FRET)的底物切割的筛选。PF-00835231(1)就被鉴定为重组非典病毒Mpro的有效抑制剂。
2020年新冠疫情爆发,药物再利用是找到对抗新冠病毒药物的最快方法。辉瑞公司制备了PF00835231(1)的磷酸前药PF-07304814(2)。尽管PF-07304814(2)是一种高效的Mpro抑制剂,但它生物利用度较低,必须静脉给药。后来,当口服Mpro抑制剂的生物利用度提高且发展前景十分明朗时,辉瑞停止了该药的临床试验。

PF-00835231(1)口服生物利用度较差的原因很明显:它有太多(五)个氢键供体,这大大地降低了药物被动渗透性吸收[2]。辉瑞通过使用融合环丙基取代了PF-00835231(1)分子中间的亮氨酸部分,能够消除一个氢键供体,同时保持仿制药的抗病毒活性。
这是一个“老伎俩”,先灵葆雅的科学家曾在丙型肝炎抗病毒药物波普瑞韦中使用过。但拥有刚性结构也有其代价:这种药物失去了与主蛋白酶的谷氨酰胺的关键作用。
为了重新获得与谷氨酰胺的相互作用,辉瑞将吲哚部分转化为三氟乙酰胺,与其他同分异构体相比,三氟乙酰胺在渗透肠道屏障的测试中表现突出。此外,在分子尾部,辉瑞选择丁腈,通过消除PF00835231(1)上的另一个氢键供体,进一步增强了药物的口服吸收。
与原型药相比,少了两个氢键供体的Nirmatrelvir(3)在2020年7月被确定为口服临床候选药物。
如下图所示,它是一种可逆抑制剂,与Mpro的半胱氨酸残基在145位(Cys145)形成共价键,形成加合物4。[3]
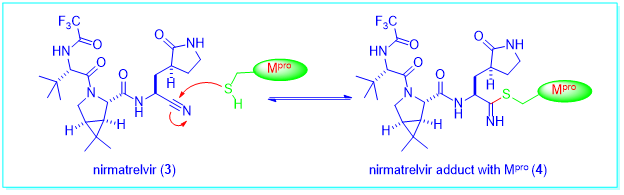
研究人员还是觉得nirmatrelvir(3)的口服生物利用度仍然很低。
Nirmatrelvir(3)作为CYP34A肝药酶的底物,研究人员发现其与CYP34A抑制剂利托那韦联合使用,可大大提高其口服生物利用度,这种联合用药称为Paxlovid,于2021年2月开始第一阶段临床试验。并于2021年12月,获得FDA批准。从那时起,世界各地的患者都从这种药物中获益。
奇怪的是,Paxlovid有一个有趣的“Paxlovid反弹”效应。例如,拜登总统在新冠病毒检测呈阳性后服用了Paxlovid。几天后,他的检测结果呈阴性。但在连续几天检测呈阴性后,他第二次检测呈阳性。这显然是一个已知的风险,这表明无论是否服用Paxlovid,一些患者都会出现复阳。
辉瑞的Paxlovid是科学的胜利。它的成功建立在几十年的研制成果,包括HIV蛋白酶抑制剂和HCV NS3/4A丝氨酸蛋白酶抑制剂抗病毒药物的相关研制成果。
然而,nirmatrelvir(3)仍然属于类酶药,容易被酰胺酶和肽酶水解,这大大影响了其生物利用度。
而盐野义的Mpro抑制剂ensitrelvir(7)不是类酶药。Ensitrelvir(7)是一种非肽类和非共价药物,只需每天口服一次。而辉瑞的nirmatrelvir(3)必须与利托那韦合用,一天两次。
疫情爆发后,盐野义迅速根据其化合物库来设计药物结构,直至筛查到一种三嗪5。尽管三嗪5对Mpro不是很有效(IC50= 7.8M),但此结构可使药品代谢更稳定,提高口服生物利用度,清除率更低。

结构经过快速优化得到了三嗪6,其中P1′六-氯代-二-甲基-2H-吲唑基取代了原来的二氟甲基-苯醚。在保持良好的DMPK的同时,这种修饰使该酶抑制剂的活性提高了90倍。最终,盐野义用三唑取代了P1′区域的酰胺,产生了ensitrelvir(Xocova,7)。[4]
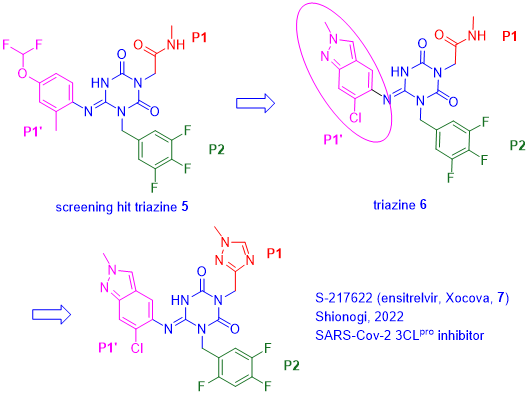
由于仍存在一些安全问题,近日日本当局还未批准ensitrelvir (Xocova,7)上市。
可以想象,有多少制药公司正在研究更好的抑制剂。但随着新冠疫情大势逐渐平息,研究还会继续么?
参考文献:
1.Zhuo, Lin-Sheng; et al. Insights into SARS‑CoV‑2: Medicinal Chemistry Approaches to Combat Its Structural and Functional Biology. Topics in Current Chemistry (2021),
3.Halford, Bethany How Pfizer scientists transformed an old drug lead into an oral COVID-19 antiviral. ACS Cent. Sci. 2022, 8, 405−407.4.Owen, Dafydd R.; et al. An oral SARS-CoV-2 Mpro inhibitor clinical candidate for the treatment of COVID-19. Science (2021), 374(6575), 1586-1593.
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。















发表评论
注册或登后即可发表评论
登录注册
全部评论(0)