2022-08-30 来源 : 风云药谈 ,作者张廷杰
创新:几乎是所有想做大做强药企的“共识”
在中国普通仿制药走向没落已经是“注定”,创新几乎是所有想做大做强药企的“共识”,创新这条路注定不是平坦的,在国外做创新药有双十的说法,“一个创新药做下来需要十年、需要十亿美金”(说的是完全创新,不是505b2等)。
在中国目前做创新药,先要有钱、有人,然后延伸到有技术、研发、临床、注册、生产,再然后商业化,组建团队,医保(国谈)、双通道,准入、开发。总结而言就是要有政策的土壤、人才的引领、资本的助力。
命好的产品比如:埃克替尼、阿帕替尼、安罗替尼等;命好的企业已经上市,并且项目篮子里已经有很多“鸡蛋”了。
就在近期,一家生物要创新企业通知停工、停产

(图片来源:公共网络)
是这家公司很新、很小?看了注册信息,似乎也还可以
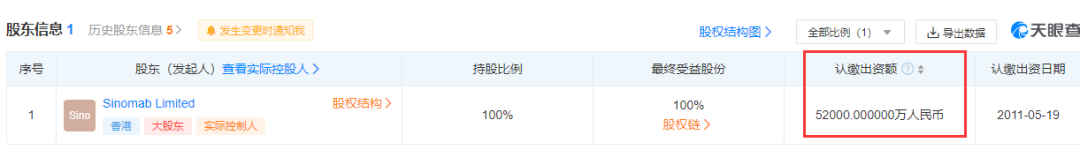
(图片来源: 天眼查)
是这家公司没有产品上市,还是没有营收?


(图片来源: 公共网络)
一个创新产品在中国市场能达到百亿RMB规模,就算是市场同意了,医保资金能受得了?
回过头来看看,国内的创新药及其市场情况。
一
创新药申报“如火如荼”
创新药先从美、欧爆发,再到日本爆发,那始终中国还在用粮票呢,后来中国仿制药“大爆发”,部分“优质”仿制药披了多年的“原研待遇”的外衣,在药品从劣到优、产品从少到多、价格从高到低这些资本主义走过的弯路,我们几乎一个都没落下。
仿制药的大潮在慢慢退去,创新药后浪还没跟上,大部分企业还是靠着“浪仿1、浪仿2”在续命亦或发展,818就是最具代表性的缩影。
表1:FDA历年各类型审批数量及对照
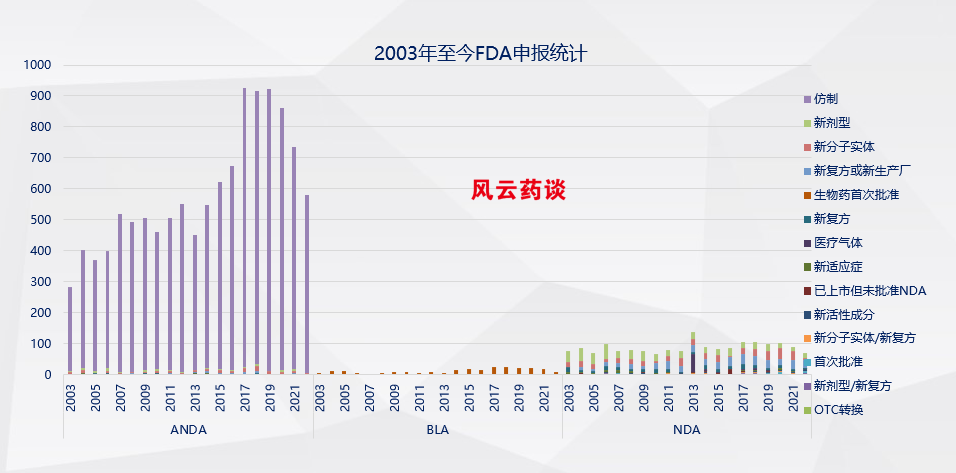
(数据来源:FDA 篱笆哥 风云药谈整理)
表2:全球历年阶段的新药数量各国对比
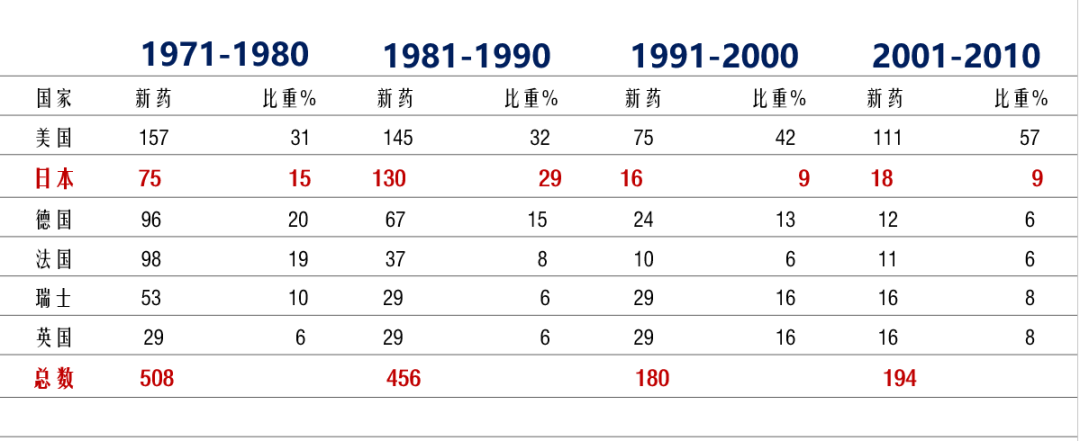
(数据来源:日本医药工业协会 Arthur Daemmrich 同写意公共资料 风云药谈整理)
表3:国内近几年的创新药(国产VS进口)申请情况
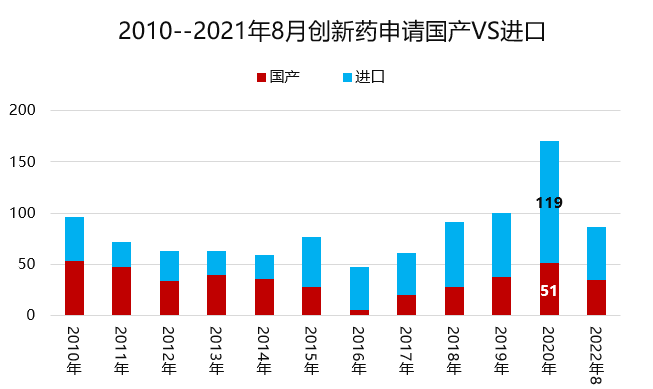
(数据来源:CDE 篱笆哥 风云药谈整理)
二
新药国谈想说爱你并不容易
不管是一类还是二类创新,似乎有一种误解,制药是产品能获批那么进入医保(国谈)就好像是流程一样,从目前来看似乎没有那么乐观。
尽管,国家从诸多政策层面给予了各种支持,但是,创新药进入医保的实际情况没有想象中那么乐观,这必须从两个主要维度去看,一个就是时间,一个就是价格。
表4:历年国谈成功与产品获批时间对照明细
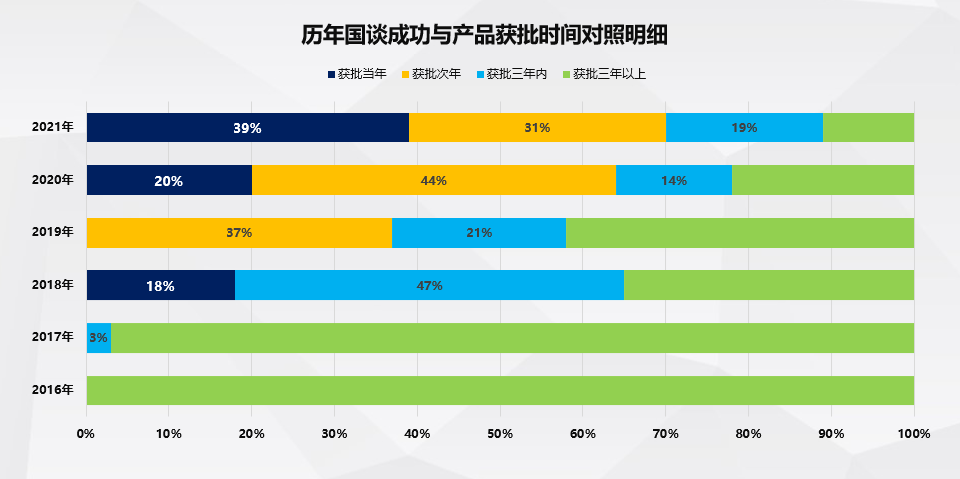
(数据来源:CDE 医保局官网 风云药谈整理)
表5:历年国谈产品从获批到进入医保谈判目录时间

(数据来源:CDE 医保局官网 风云药谈整理)
表6:历年国谈产品国产&外企纳入数量对比
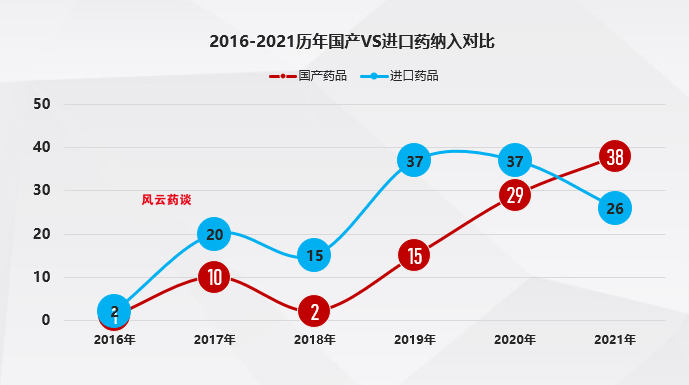
(数据来源:CDE 医保局官网 风云药谈整理)
表7:历年国谈产品及其领域的市场规模对比
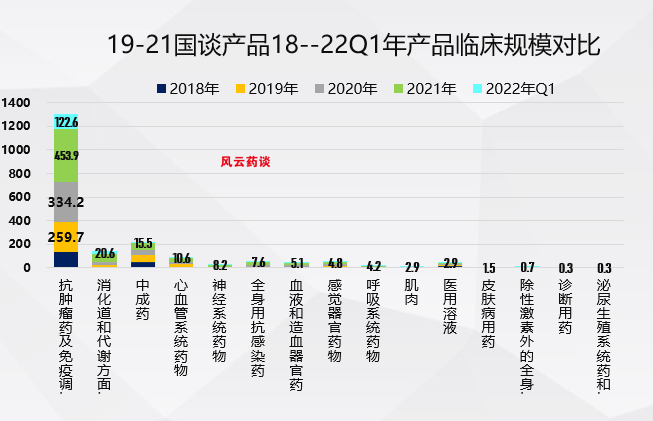
(数据来源:医保局官网 药融云 IMS 米内等 风云药谈整理)
从上面数据可以看得出来,进入医保产品的数量对比获批的数量比例没有想象中乐观,进入产品的降幅平均在50--60%之间(有官方公布),进入产品的年度实际规模增幅除了肿瘤产品,其他领域或者赛道并不是十分理想。
不管是从现状还是从未来的发展看,创新是一个药企通往未来制药大企业的“必经之路”,好摘的“桃子”先被美欧企业抢先一波,日本企业以武田为首的又抢了一波,留给中国企业的好摘的“桃子”基本上就是二类的居多,一类的还有实际和实力的差距。
集采对大部分企业的资金池是“减法”的多,国谈产品的崛起需要时间,传统企业起码“锅里有米、碗里有饭”,完全创新型企业就要不断的烧钱,要么,就实现阶段性的转让,比如:荣昌、科伦、济民可信等。
创新药不仅仅是在国内竞争、同时也面临和国际巨头“掰手腕”,生物制剂已经成为创新药的“桥头堡”,不仅仅是稳准狠,能在快速变现前活下去就目前来讲似乎也很重要。
创新药太宏大,就像是在迷雾中寻找宝藏,有很多宝藏同时也有“毒蛇”,有些人先挖到了宝藏、有些人还没挖到保障就遇到了“毒蛇”,收获与风险并存,看哪个更先遇到。
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。





发表评论
注册或登后即可发表评论
登录注册
全部评论(0)