2023-02-15

新型抗肿瘤药物价格昂贵,给国家卫生系统带来严重压力。因此,开发旨在提高耐受性、疗效、患者便利性和减轻经济负担的替代给药方案势在必行。且最近正在协助从小剂量到更大剂量的研究者发起研究方案的撰写,本文正好契合,自己学习提升的同时,也期望对你有所帮助。
在过去的几十年中,抗肿瘤药物的剂量选择主要基于耐受性而非疗效,即由最大耐受剂量(MTD)决定。耐受性驱动的剂量选择,可以在较短时间内,在随后的以疗效为主要探索目的数量有限的患者中快速进行,从而实现药物的最终获批上市。这种剂量选择方法往往忽略了暴露-反应关系、药代动力学个体间变异性、长期安全性和患者便利性。此外,新型抗肿瘤药物价格昂贵,给国家卫生系统带来严重压力。因此,开发旨在提高耐受性、疗效、患者便利性和减轻经济负担的替代给药方案势在必行。
尽管许多研究表明,与已经批准的标准剂量相比,各种替代给药策略都显示出一定的获益,但这些给药策略在真实的临床实践中往往是不可行的。在某些情况下,作为上市后要求的一部分,市场授权药物持有人可以探索优化的给药方案。这些研究的结果由监管机构评估,可能导致药物相关标签的修改,从而实现在临床实践中的应用。然而,大多数替代给药方案是通过研究者发起的研究进行研究的,没有得到市场授权的相关持有人的支持,也没有得到监管机构的评估,这些研究的结果也没有转化为药物适应症和临床实践中得到应用。
指导委员会可以评估研究者发起的研究的结果,但迄今为止,这仍然不是普遍的做法。这些给药方案也很少找到日常实践的方式,主要原因如下:
“off-label”状态、缺乏报销或缺乏临床终点的相关证据,可能是首要原因。
然而,受到质疑的是,是否总是需要对临床终点进行大规模临床试验,尤其是在药物的暴露-反应关系已经明确的情况下。尽管使用的许多药物的治疗窗口很窄,但肿瘤学家在临床药学方面的培训往往很少。
疗效和对临床试验方案的遵守往往比剂量和给药间隔的个性化更受青睐。
目前,对于在临床实践中实施替代给药方案所需的证据水平缺乏共识。未来,随着FDA的Optimus项目的实施,以及在药物开发过程中对暴露-反应关系的更深入理解,这种情况很可能会发生改变。然而,对于目前已经获批的抗肿瘤药物,优化剂量的需求尚未得到满足。从这个角度来看,我们就促进和加速实践中采用替代给药方案所需的证据水平提出了切实可行的建议。
延伸阅读:FDA支持肿瘤药物开发中剂量优化
FDA肿瘤学卓越中心的Optimus项目,该项目将为抗肿瘤药物厂家制定新的指南,以便在早期临床研究中对更广泛的剂量进行开发探索。具体目标包括:
通过指导原则、研讨会、和其他公开会议传达对剂量探索和剂量优化的期望;
为药物开发人员提供机会并鼓励其在开发计划的早期与FDA肿瘤审查部交流,在进行旨在注册的研究之前,讨论剂量探索和剂量优化;
制定剂量探索和剂量优化策略,在剂量选择中利用非临床和临床数据,包括在研究中对一系列剂量进行随机评估。这些策略的重点将放在开发计划中尽早进行这些研究,并尽可能有效地为患者带来有希望的新疗法。
给药方案分类
许多抗肿瘤药物显示出药代动力学暴露(即AUC作为血浆浓度与时间曲线下的面积)与治疗效果和毒性之间的关联。因此,使用这种暴露来评估替代给药策略是一种合理的方法。根据药代动力学暴露,替代给药方案可分为以下三类:
导致等效暴露的替代给药方案;
导致较低或较短暴露的替代给药方案;
导致更高暴露的替代给药方案。
我们假设,在临床实践中实施替代给药方案的证据水平应符合每一类别的具体要求,如下文所述,并在表1和图1中总结。
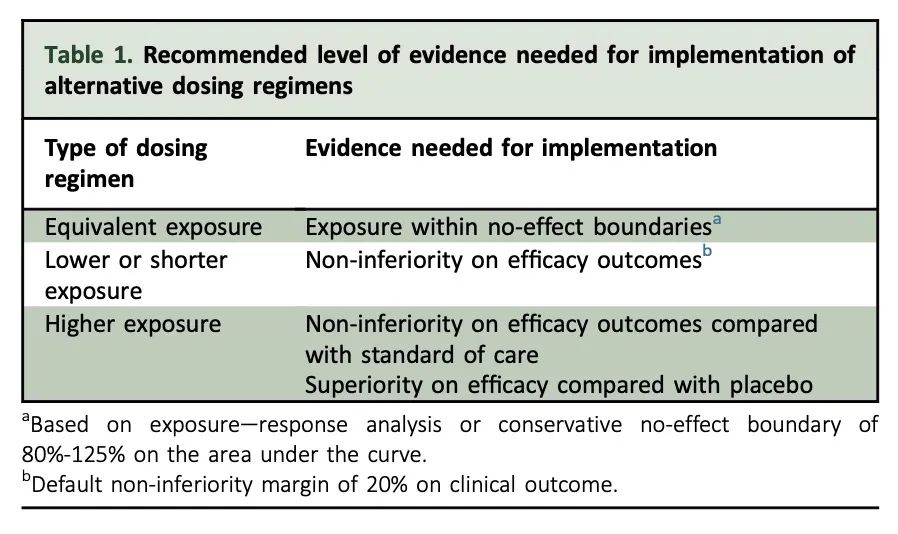
表1. 实施替代给药方案所需的推荐证据水平

图1. 实施不同类型的替代给药方案所需的证据水平
y轴表示累积药物动力学暴露。虚线水平线表示暴露的临床无影响边界。在x轴上表示了不同的替代给药方案。这些分为三种类型:导致同等暴露(粉色)、较低或较短暴露(绿色)或较高暴露(灰色)。顶栏表示实施所需的拟议证据。点代表替代给药方案的相关药代动力学暴露参数,随机选择以说明示例。
导致等效暴露的替代给药方案
等效药代动力学暴露是指药物暴露水平保持在界定治疗结果临床显著变化的界限内。导致等效暴露的替代给药方案的主要目标是改善患者方便性和耐受性,并减少药物变异性或财务负担。
导致等效暴露的给药方案亚型
可区分确保等效暴露的三个子类替代给药方案。
第一类是更高剂量给药,给药间隔更长,随着时间的推移累积暴露量相等。延长给药间隔提高了患者的便利性,并减轻了医院或门诊设施容量的负担,如果毒性不增加,则可以接受。
此类给药方案与较高的峰值药物浓度和较低的谷浓度相关。该方法已应用于几种单克隆抗体,已表明这些变化不会影响其疗效和耐受性,并可应用于峰值浓度和毒性之间没有明显关联的其他药物。
例如,纳武利尤单抗的批准剂量为每2周3 mg/kg(Q2W)。随后,基于建模和模拟研究中类似的平均稳态浓度,批准了240 mg Q2W和480 mg每4周(Q4W)的固定剂量。
第二类是较低剂量,同时服用食物,以提高药物口服生物利用度
由于在亲水性消化道内的溶解度有限,一些亲脂性口服抗癌药物表现出较低的口服生物利用度。因此,当这些药物与食物一起服用时,在脂肪和/或胆汁盐的存在下能够更好地溶解,从而会产生更大的吸收(即提高口服生物利用度)。
对于某些药物,食物中脂肪的含量对溶解度和生物利用度有显著影响。对于这些药物,应指定脂肪量,以减少由于世界各地饮食差异导致的吸收变异。然而,对于许多药物来说,食物效应主要由胆汁盐驱动,胆汁盐在每餐后分泌。饮食和膳食中的脂肪量与那些不太相关的药物有关。
此外,较低剂量,也会减少胃肠道疾病的副作用,对患者来说往往更容易接受和更加方便。
最后,较低的剂量可以减轻药物和财务负担。
最近,食品对塞瑞替尼生物利用度的有益作用被证明。在关键的随机III期研究中,塞瑞替尼每日一次750 mg(QD)的剂量,根据药代动力学研究证明,450 mg QD随餐组,展示出等效的暴露量和有益的毒性曲线,从而获得批准随餐使用450 mg QD。
第三类是药代动力学增强
在药代动力学增强模型中,代谢酶的非治疗性抑制剂可以与相同酶代谢的较低剂量的治疗药物组合。因此,口服生物利用度增加,治疗药物的全身清除率降低,导致与标准剂量相比,较低增强剂量的暴露相似,但药物暴露的患者间变异性可能降低,因此治疗结果更可预测。
这一概念已在抗逆转录病毒治疗领域使用了几十年,目前已在数百万人免疫缺陷病毒感染患者中使用。在肿瘤学领域,应用也逐渐增多起来。
近期的研究表明,较低剂量的厄洛替尼与细胞色素P450(CYP)3A抑制剂利托那韦联用,呈现出的药代动力学暴露与使用标准剂量的厄洛替尼相似。
实施剂量方案导致等效暴露所需证据水平
实施这些替代给药方案的要求可从评估药物-药物相互作用和药物对器官损伤的药代动力学的监管指南中得出。根据有效性和安全性的暴露-反应关系,可以定义暴露范围,在该范围内,预期疗效和安全性没有临床相关差异。该暴露范围受到无效应边界的限制。
例如,与禁食摄入相比,吉非替尼与食物一起服用时的暴露量明显更高(AUC 132%)。基于以下因素,暴露差异被认为与临床无关:
之前的暴露反应分析,因此可以与食物一起或不一起服用。因此,没有影响边界界定禁食或喂食吉非替尼的等效暴露,这在临床上是等效的。
如果对暴露-反应关系缺乏了解,建议AUC的保守无效应边界为80%-125%。
为了评估药代动力学暴露是否在定义的无影响范围内,首选随机交叉研究。药代动力学患者间变异性通常比患者内变异性大得多。通过使用交叉设计,需要一组小得多的患者(通常约20人)在无效应边界内显示暴露。
如果替代给药方案的药代动力学暴露和置信区间在预定义的无效应边界内,则无需进一步评估治疗效果。
如果暴露在这些无影响范围之外,则需要进一步的有效性和/或安全性证据来实施。
最后,一旦证明等效性,可以考虑对治疗药物进行监测,以进一步优化个体患者的暴露。
替代给药方案导致更低或更短的暴露
对于目前因耐受性驱动的剂量选择而过量使用的靶向抗癌药物,较低剂量可能同样有效,但毒性较小。当该较低剂量导致在无效应边界内的药代动力学暴露时,前一节中提出的证据水平应足以实施。
使用新抗癌药物治疗的患者中,有相当一部分经历了与治疗相关的不良事件。由于不良事件,50%的患者需要中断剂量,26%的患者需要减少剂量,10%的患者需要永久停止治疗。减少剂量或提前停药可减少副作用,同时保持功效。此外,它可以减轻财政负担。
导致较低或较短暴露的给药方案亚型
由于耐受性驱动的剂量选择,目前批准的许多抗癌药物都是在MTD附近给药的,这是在短时间内相对较小的研究中确定的。这会导致药物过量,在较长的治疗期内,患者耐受性较差,而较低剂量可能同样有效。
达沙替尼是一种酪氨酸激酶抑制剂,用于治疗慢性髓系白血病。最初批准的剂量为70 mg,每日两次(BID)。随后,将该剂量调整为每天一次100 mg,这导致血液学毒性和液体潴留减少,同时保持疗效。目前,更低剂量的50 mg QD被认为对慢性髓性白血病有效且安全。
在免疫疗法中,一些研究正在研究较低的给药剂量。例如,在DEDICATION-1/NVALT30(EudraCT 2020-000493-15)试验中,正在探索300mg Q6w 替代 400mg Q6w的可能性。
I期研究显示,在剂量为1mg/kg Q3W的情况下,受体即可以被完全占据,预期较低剂量的疗效与注册的剂量效果相同。
过去几年,癌症患者的治疗持续时间大幅增加。长期服用抗癌药物会导致持续的副作用,影响患者的生活质量。
早期停药在辅助治疗中已经验证有效,例如,在HER2阳性的早期乳腺癌症患者中被证明是可行的,在这些患者中,6个月的曲妥珠单抗与12个月的疗效相同,心脏毒性更低,严重不良事件更少。对于最初给予的直到疾病进展的抗PD-1免疫疗法,后来的试验支持在特定癌症中使用预定义的2年。
表2列出了导致更短或更低暴露的各种替代给药方案。
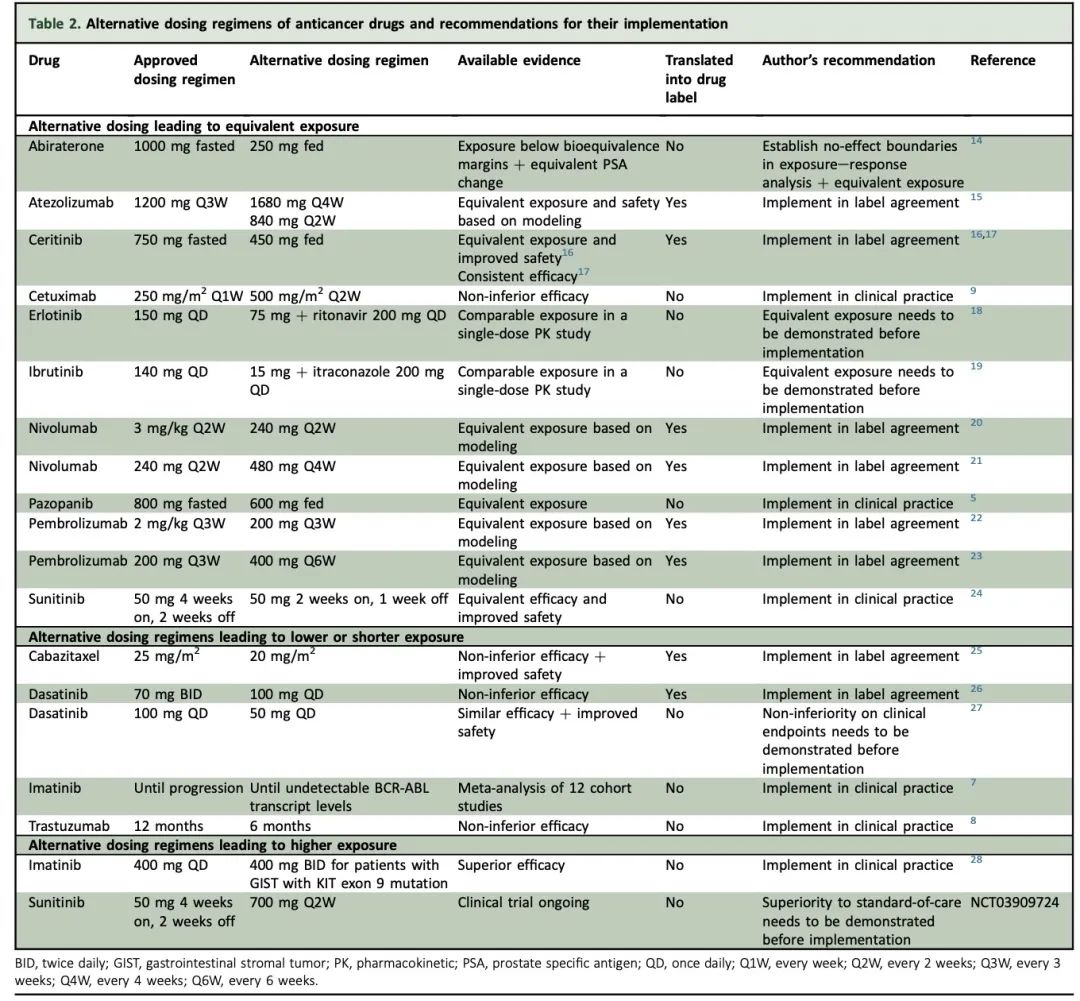
实施较低或较短暴露剂量的给药方案所需的证据水平
较低或较短的暴露量不能保证可比的疗效。在非劣效性(NI)研究中应证明这些替代给药方案的类似疗效,确认替代给药与批准的给药方案相比,不会导致更差的治疗结果(中位数和置信区间超出预定义的NI界限)。当替代剂量导致更好的耐受性或患者便利性时,可以接受更大的NI裕度和更小的样本量,这与接近等效性研究一致。然而,当缺乏证实较小或较大NI裕度的数据时,可以使用20%的默认NI裕度,与肿瘤学环境中生存研究的平均NI裕度一致。如果在临床实践中证明非劣性结果,则可以实施暴露量较低或较短的方案。
替代给药方案导致更高的暴露
尽管许多抗癌药物在MTD附近或在MTD时给药,但较高的暴露量可能是患者可以耐受的,甚至对不同的患者群体是更为有益的。对于这些患者,替代给药方案导致更高的暴露,正在被研究推进中。
给药方案的亚型导致更高的暴露
抗癌药物是在相对未选择的患者群体中开发和测试的。然而,在个性化医学和基因检测的时代,可以识别出不太敏感的肿瘤患者。这些肿瘤可能需要更高的药物暴露水平,这可以通过替代给药方案达到。
例如,在胃肠道间质瘤患者中,伊马替尼的剂量为400 mg QD。然而,在KIT外显子9突变的胃肠道间质瘤患者中,更高剂量的400mg BID导致更好的治疗暴露和结果。
此外,不同肿瘤类型或部位可能需要更高的药代动力学暴露。间歇性高剂量舒尼替尼导致更高峰值浓度,在晚期结直肠癌患者中显示出良好的疗效
实施导致更高暴露的给药方案所需的证据水平
作为导致更高药代动力学的替代给药方案,暴露可能会增加毒性,必须显示可接受的耐受性。此外,与标准剂量相比,替代剂量方案必须证明对致癌突变不敏感的患者具有更高的暴露水平。
如果针对不同的适应症测试替代给药方案,治疗需要证明与安慰剂或NI相比,优于标准疗法。表2列出了导致更高暴露的各种替代给药方案。
未来方向
到目前为止,大多数抗癌药物的剂量选择都是基于在短时间内相对较小的剂量发现研究,目的是为进一步研究确定安全剂量。因此,在市场授权后,有多种可能性可以改善给药方案。
我们在此从临床药理学角度为实施抗癌药物替代给药方案所需的证据水平提供了实用建议,如图1所示。
FDA最近实施了Optimus项目,该项目将使临床药理学成为抗癌药物开发期间选择给药方案的坚实基础。与基于耐受性的剂量选择不同,鼓励药物开发人员使用暴露响应分析进行剂量发现和剂量优化。然而,该项目不包括目前市场上大量获批的抗癌药物。
对于已经批准的药物,还应评估研究者驱动的研究中的替代给药方案,以促进更广泛地实施这些数据。
理想情况下,这些研究的给药策略应包含在药物标签中。但是,只有授权持有人才能请求更改标签,而授权持有人可能不急于在批准后优化剂量。有鉴于此,FDA已启动项目更新,旨在根据已发表文献中的相关科学证据更新已注册肿瘤药物的过期标签信息。这可能会导致标签更新和新指示给药方案。此外,优化给药方案的努力不应掩盖通过减少药代动力学暴露的个体间差异来进一步优化个体患者剂量所需的同样重要的努力。
结论
替代给药方案可以通过提高当前批准的抗癌药物的风险收益比来优化癌症治疗。从这个角度来看,根据监管机构的现有指南,制定了评估替代给药方案的建议。这些建议可以为实施优化的给药方案铺平道路,从而有助于改进和可持续的抗癌治疗。
参考文献
Long GV, Tykodi SS, Schneider JG, et al. Ann Oncol. 2018;29(11):2208-2213.
百度浏览 来源 : Biotech前瞻
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。




发表评论
注册或登后即可发表评论
登录注册
全部评论(0)