我常说“小统计大文章”,意思是很多时候好的临床试验文章,不需要复杂的统计学方法。今天说的一篇论文就是如此。但是简单的统计学,非常重要的是要遵守统计分析规范和写作规范。我看到很多临床试验论文,它们质量都不高,但问题不在于方法简单,而在于规范性的问题。
今天要介绍的文献的统计学方法是最常见的卡方检验和秩和检验,而且是阴性结果,却刊登在《新英格兰医学杂志》。我们不禁要思考,它用的卡方和秩和有特殊地方吗?有什么值得我们学习?美国杜克大学的研究团队,针对超免疫球蛋白预防婴幼儿先天性原发性巨细胞病毒(cytomegalovirus,CMV)感染问题开展了多中心随机双盲平行对照试验。他们聚焦的问题是如果CMV感染的孕妇服用超免疫球蛋白后,能否预防婴幼儿的CMV感染。因此,他们于2012-2018年期间,在16个医疗中心招募了399名CMV感染的孕妇。患者以1:1 进行随机化分组分为干预组和对照组。干预组服超免疫球蛋白,而对照组服用安慰剂。主要结局指标是一个复合结局,结局事件为胎儿CMV感染或 3 周龄前诊断出的先感染或胎儿或新生儿死亡(包括终止妊娠)。根据该信息,该研究是探讨两组不良结局发生率的差异性。次要结局指标,包括早产率、婴幼儿出生周数、头围、体重、是否终止妊娠等。这些次要结局中,有定量结局(可能是偏态的),也有分类结局从而计算发生率。
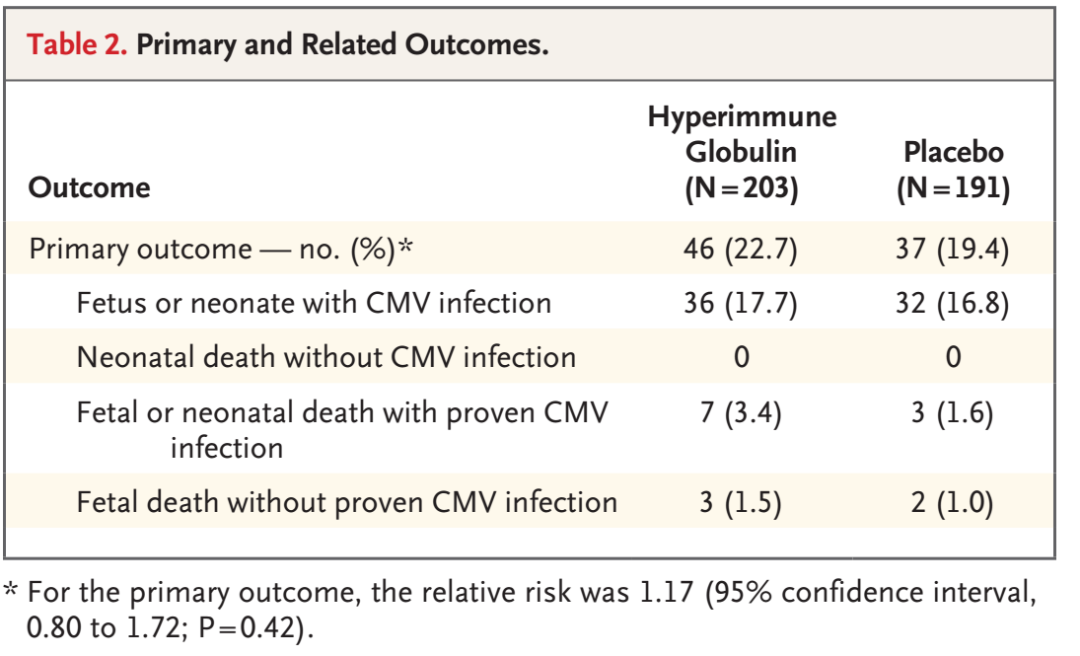
分析结果发现,在总共394名纳入最终分析的人群中,超免疫球蛋白组发生CMV感染或者胎儿或婴幼儿死亡的人数46人(占总数的22.7%,46/203),安慰剂组发生CMV感染或者胎儿或婴幼儿死亡的人数37人(占总数的19.4%,37/191)。两组人群阳性率没有统计学差异(RR= 1.17; 95CI, 0.80 to 1.72;P=0.42)。这意味着该结局是阴性结果。
因此,该研究结果意味着,孕妇孕周24周开始服用超免疫蛋白,无法阻断后代发生先天性感染巨细胞病毒(CMV)。为什么这篇文章值得学习!
从2012年到2018,再到现在发表文章,十年期间的努力,得到的却是阴性结果。
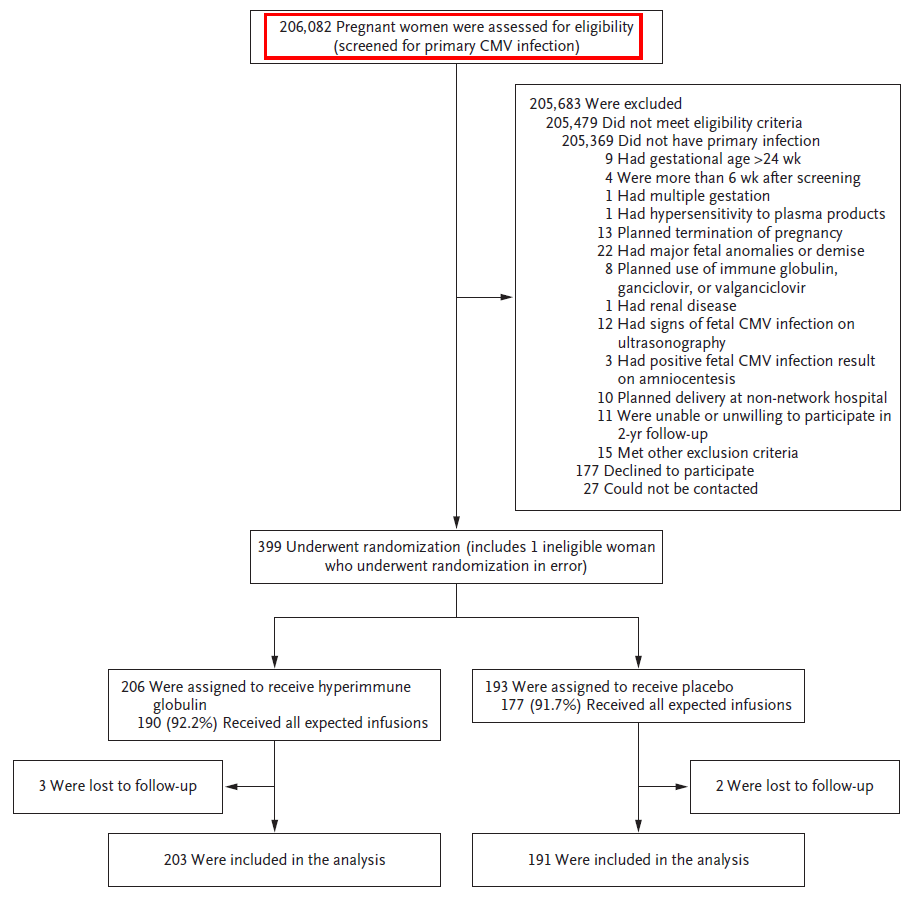
实际上,早在2014年,在该临床项目启动不久,《新英格兰医学杂志》就刊登过类似的结果--发现超免疫球蛋白不能阻止巨细胞病毒宫内传播。因此可想而知,该团队看到该报道时心理有何等崩溃!导致研究团队到2018年再也无法坚持继续进行临床试验,提前终止(原设计样本量为800例)。那这一阴性结果,如何能够发表在《新英格兰医学杂志》?这篇提前终止的研究,有哪些值得学习的呢?尊敬在哪里?第一,它花了差不多10年的功夫坚持研究,第二,为挑选合适的对象,他们筛选了20万孕产妇。从他们流程图可以看出,20万人最后筛选了400人开展临床试验,过程漫长而艰辛。
这张流程图代表了研究的团队的努力,也是审稿人倾心的一个原因吧。很多人不认同,说我们做临床研究,也花了很多精力很多时间,也是百里挑一一啊。问题是,你有写出流程图么?你有严谨地写出人群的筛选过程么?没有!很多时候,差的不是你的努力,而是你记录你努力的那一实验记录本!一般来说,《新英格兰医学杂志》论文的统计学方法是高大上的,复杂又精准,不过也有不少文字的统计学方法也不复杂----简单统计学方法就能解决问题,没有必要用复杂的统计学方法(小统计),其结果也照样能够发表在顶级医学期刊(大文章)。本篇论文的主要结局指标是胎儿和新生儿不良结局结局事件,那么在此基础上可以计算率,根据该信息,该研究是探讨两组不良结局发生率的差异性。次要结局指标有定量数据,有分类数据。定量数据有正态分布,也有偏态分布数据。根据数据类型的特点,最基本的比较组间差异性的方法如下:
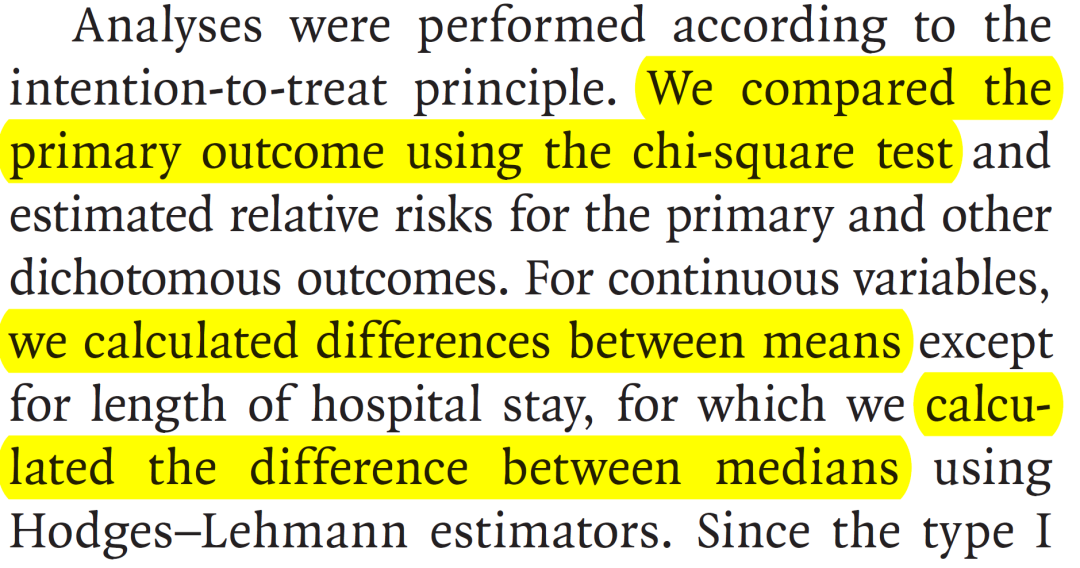
没错,这篇《新英格兰医学杂志》论文采用的方法也就是这些最最基本的的统计学方法。它的核心统计学方法,就是下面一段话。统计学方法就是卡方、t检验和秩和检验。
不过,诸位统计学方法虽然很简单,但是统计分析结果规范表达必须很重要。不知道诸位从上述这段话里面能够体会到什么样的重要信息?
事实上,高质量的临床试验,统计学结果中,除了计算P值,非常重要的信息,是要提供效应值!我们可以看看这篇文章的统计分析提供了什么效应值?
不仅如此,除了效应值还需提供置信区间,所以看这篇文章的结果是这么描述的:The fetus or neonate of 22.7% of the participants in the hyperimmune globulin group and of 19.4% in the placebo group had a primaryoutcome event(relative risk, 1.17; 95% confidence interval [CI], 0.80 to 1.72; P = 0.42) 在统计表里面,也提供了相应的参数
统计方法选择什么不是那么重要,条条马路通罗马,规范表达跟重要。3. 阴性结果如何是好?
研究人员都怕阴性结果,更不敢有勇气提前终止。这么大代价的临床试验,怎么说停就停?
首先,是因为阴性结果也很重要,这个研究以较大的样本量,再次证明了超免疫球蛋白无法隔断母婴传播CMV病毒,具有较强的临床意义,简直是盖棺定论!其次,结果阴性而提前终止,是早已经写入研究设计方案的。作者设计了多次期中分析,并考虑了提前终止的条件,研究设计和实施都很 严谨。为此,作者写了老长的一段文字。An independent data and safety monitoring committee monitored the trial.项目成立独立的数据与安全监察委员会来监测临床试验。
We used a group sequential method to control the type I error, with the Lan–DeMets characterization of the O’Brien–Fleming boundary providing the stopping rule for benefit.研究根据一定的规则进行多次的期中分析,并控制假阳性错误,委员会可以根据情况中断临床试验。We also used conditional power analysis as a stopping guideline for futility. If the conditional power was low (<10%) given the observed data and assuming the alternative hypothesis for the remainder of the trial, termination for futility could be considered. In addition, the data coordinating center continuously monitored the outcomes of infusions for serious adverse events of special interest that occurred during the treatment period (defined above) in the hyperimmune globulin group. If the percentage of women in the hyperimmune globulin group who had one of these events within 72 hours after an infusion was not consistent with the assumed percentage among pregnant womenin the general population (≤0.5%), the trial would be halted until the data and safety monitoring committee determined whether the trial should continue. Five interim analyses were performed for the primary outcome.这篇论文是少见、如此详细撰写中断临床试验过程的论文了。很多临床试验建议进行期中试验,不过我们可以规范地开展本项工作么?我们可以从中学到什么?
2)阴性结果也不见得不能发表,如果你研究的内容新颖重要,哪怕是提前终止也值得发表,而且提前终止可能还有助于你发表论文。
3)流程图最好从纳入筛选的对象开始。
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。








发表评论
注册或登后即可发表评论
登录注册
全部评论(0)