2022-03-30

胃癌分为散发性胃癌、家族聚集性胃癌(FGC)及遗传性胃癌(HGC),大多数胃癌为散发,其中5%~10%的胃癌患者有家族聚集现象,1%~3%的患者存在遗传倾向。
家族遗传性胃癌还包括以胃癌为次要表现的胃肠道遗传综合征,如林奇综合征、幼年性息肉病综合征(JPS)、黑斑息肉综合征(PJS)、家族腺瘤性息肉病(FAP)等,上述综合征以家族遗传性结直肠癌为主要表现,同时有较高的胃癌发病风险。

胃腺癌伴近端多发息肉(GAPPS)是一种罕见的胃息肉综合征,具有显著胃腺癌风险,其特点是局限于胃近端的常染色体显性遗传性胃息肉病[包括异型增生病变和(或)肠型胃腺癌],无十二指肠或结直肠息肉病或其他遗传性胃肠道肿瘤综合征。
临床诊断标准
致病基因改变
四、健康管理及治疗策略
1.针对CDH1突变健康携带者方案
HDGC是一种高外显率的常染色体显性遗传病。CDH1胚系致病或可能致病突变(以下均表述为致病突变)携带者发生胃癌的终生累积风险在男性约为37%~42%,女性约为25%~33%。
预防性全胃切除术(PTG)被多数指南推荐。基于Seevaratnam等系统性总结的多个关于PTG家系临床研究数据,充分告知CDH1基因突变携带者发病风险、手术获益和围手术期风险情况下,推荐行PTG,术者可根据情况决定是否行淋巴结清扫和迷走神经保留。通常,推荐进行预防性手术患者年龄为20~30岁,或为最小发病家庭成员年龄减5岁。
1)有显著癌症家族史且无症状的CDH1胚系致病突变携带者,预防性切除需慎重考虑患者意愿,对发病风险、手术安全性及生存质量进行评估。未接受预防性胃切除术者,建议进行密切内镜监测,推荐每年行1次胃镜检查,包括30个随机位点的活组织检查,所有接受监测的患者应充分了解内窥镜监测的局限性。
2)无DGC和HDGC家族史或LBC个人史,且为评估癌症风险行临床基因检测后发现有CDH1致病突变或有意义不明的CDH1突变。

1.1 内镜监测
目前,尚无可靠筛查方式能在突变携带者中早期诊断DGC。HDGC患者的胃癌是印戒细胞癌,位于完整的表面上皮下方,仅在病程晚期才能通过直接黏膜评估发现。
内镜监测最佳频率尚未统一,推荐1年1次。此外,推荐多处随机活检以提高检出率。
1.2 预防性全胃切除术
1)手术时机把握:对有HDGC风险者,决定是否手术时需考虑患者年龄、生育需求、家族表型(尤其先证者发生癌症的年龄)和基线营养状态。
2)手术切除范围:由于CDH1致病变异存在于所有胃组织中,故外科医生须在PTG中确保切除整个胃。远端切缘应超出幽门至少1 cm。胃肠重建之前应对近端边缘进行冰冻切片检查以确定没有残余胃黏膜,因为残留会增加未来恶性肿瘤的风险。
3)淋巴结清扫范围:单纯PTG可不进行正规淋巴结清扫,仅行D1(胃周)淋巴结清扫。因为大多数此类患者的癌症分期不超过pT1a,此时并无淋巴结转移的报道。而另一些外科医生则提倡在PTG时进行D1(胃周)淋巴结清扫,以防最终病理检查时发现T1b或更高分期的病变。
4)消化道重建:全胃切除后理想的重建方法是保留十二指肠和空肠的连续性,并且提供一个功能性贮袋,以将功能和营养失调降至最低。在为预防HDGC而行全胃切除后,倾向于在条件允许时使用Roux-en-Y食管空肠吻合术。
5)术后并发症:PTG术后近期并发症包括常见的吻合口瘘、出血、狭窄,腹腔积液感染等;术后远期并发症包括吸收不良导致铁、维生素B12缺乏性贫血,食管反流,腹泻,体质量下降,倾倒综合征,迷走神经离断后继发胆囊结石胆囊炎等。其中食管反流、迷走神经离断后胆囊功能障碍都会很大程度降低术后生存质量。故迷走神经保留,改良消化道重建方式以降低食管反流都是未来PTG手术的发展方向。
2. 针对CDH1突变胃癌患者的方案
1)在患HDGC相关肿瘤[DGC和(或)LBC],但家族史阴性的先证者中检出CDH1致病突变。这种情况先证者的肿瘤可能是HDGC的首发表现,且已有新发致病突变的报道。
2)在患非HDGC相关肿瘤的先证者中检出CDH1致病突变。这种情况CDH1致病突变可能为偶然发现,也可能为未报道过的扩展类型。
符合上述两种情况的人群均建议内镜筛查方案。

五、CDH1突变家系健康管理及优生优育
1. 家系健康管理
一旦确认家系成员为CDH1致病突变携带者,需要长期随访。若不考虑行PTG,则应每年行1次胃镜检查。但因HDGC病理特殊性,多灶性及病变早期在黏膜下固有层生长的特征,给内镜下早期发现癌灶造成较大困难。在胃体窦交界处多点活检或每次全胃活检标本不少于28~30块等手段均被提出可以增加早期发现原位癌和癌前病变的阳性率。此外,由于CDH1基因致病突变女性携带者LBC发生率较高,可考虑每年行1次的乳腺专科门诊和乳腺磁共振成像(MRI)检查。
对于结直肠癌筛查尚存争议,可考虑40岁后或家系中最小肠癌发病者年龄减10岁开始行每3~5年1次的结肠镜检查。
2. 优生优育
产前筛查作为遗传病(包括肿瘤相关遗传病)有效预防重要手段,已经比较成熟。
六、其他基因突变携带者方案
其他基因(如CTNNA1、STK11、APC、TP53、MMR基因等)突变携带者方案,包括CTNNA1、STK11、APC、PTEN以及错配修复(mismatch repair,MMR)基因胚系突变导致的遗传性胃癌整体发病率极低(<1%),多为回顾性小样本研究,缺乏大样本的数据指引治疗和随访筛查策略。
针对CTNNA1处理可参考CDH1胚系突变的治疗和随访筛查指南;STK11、APC和PTEN较罕见,对于胚系致病突变携带者通常建议在20岁左右开始,每2~3年进行上消化道内镜筛查;
而对于林奇综合征,高发肿瘤为结直肠癌和子宫内膜癌,胃癌外显率相对较低,故目前对于胚系致病突变携带者除每1~2年1次的肠镜检查以外,推荐40岁开始每3~5年行1次胃镜检查。
合并幽门螺杆菌(HP)感染时同时给予除菌治疗。针对有胃癌危险因素者,如萎缩性胃炎、广泛性或不完全性肠上皮化生、胃癌家族史以及来自胃癌高发区域的第一代移民(东亚裔),建议每2~3年筛查1次。
另外,家庭群集性胃癌主要是由于幽门螺杆菌的感染。幽门螺杆菌感染者较无感染者胃癌发病风险增加1倍。目前,我国是幽门螺杆菌感染高发国家,感染率高达50%。因此,根治幽门螺杆菌感染是胃癌一级预防的重点。
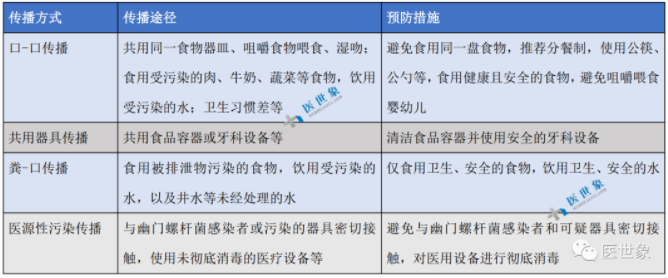
7个四联根除方案(PPI+铋剂+2种抗生素),疗程为10或14 d

引用资料:
1. 中国抗癌协会家族遗传性肿瘤专业委员会. 中国家族遗传性肿瘤临床诊疗专家共识(2021年版)(3)—家族遗传性胃癌[J]. 中国肿瘤临床, 2021, 48(24): 1248-1252.
2. 国家消化系疾病临床医学研究中心(上海), 国家消化道早癌防治中心联盟,中华医学会消化病学分会幽门螺杆菌和消化性溃疡学组, 等. 中国居民家庭幽门螺杆菌感染的防控和管理专家共识(2021年) [J] . 中华消化杂志,2021, 41(4) : 221-233. DOI: 10.3760/cma.j.cn311367-20210219-00108.
以上内容有医世象 夏雨整编
百度浏览 来源 : 网络
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。




发表评论
注册或登后即可发表评论
登录注册
全部评论(0)