蛋白激酶调节细胞生命的几乎所有方面,其表达的改变或基因的突变涉及各种癌变过程,并在病理上涉及许多其他疾病,包括自身免疫和炎症性疾病、退行性疾病和传染病。过去20年里,在提高蛋白和脂质激酶小分子抑制剂的效力和特异性以及解决激酶抑制剂耐药性的方面取得了显著进展。2001年,FDA批准Imatinib上市,它是首个通过针对特定蛋白激酶开发的药物、也是人类第一个用于抗癌的分子靶向药,此举也被认为是激酶抑制剂开发的里程碑。目前已有70多种新药获得批准,激酶抑制剂一度成为肿瘤治疗的主导药物,也对一些非癌性疾病的现有治疗产生重大影响。
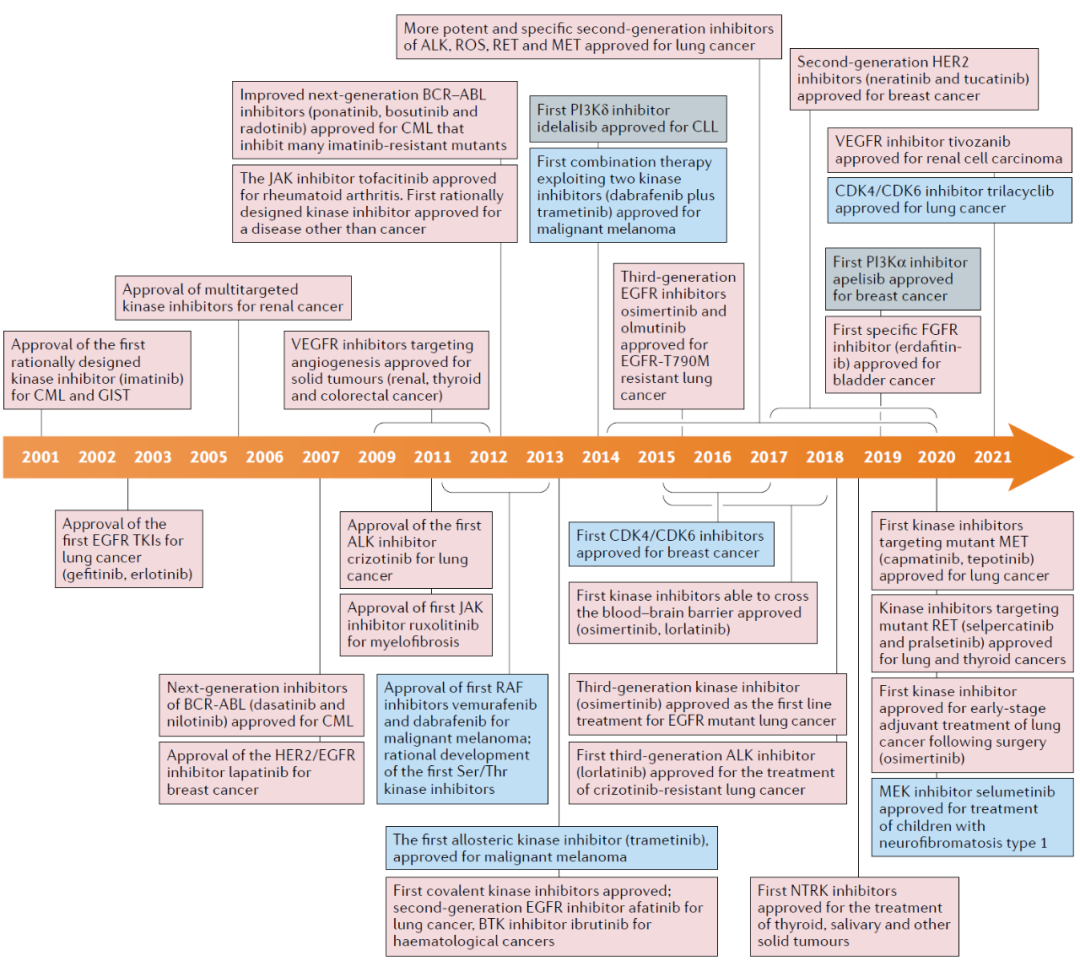
图1、自2001年伊马替尼被批准用于治疗cML以来,过去20年激酶抑制剂开发和批准的重要事件时间表。
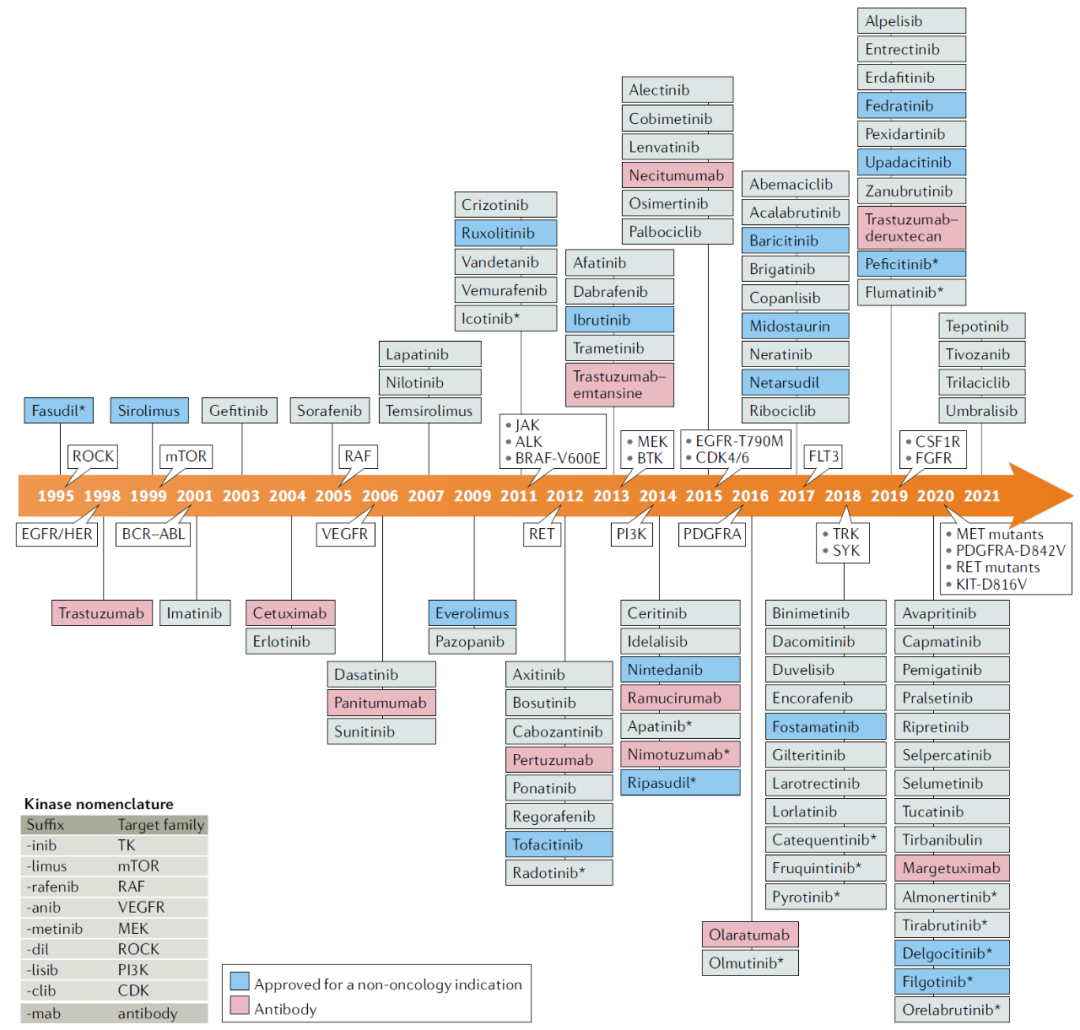
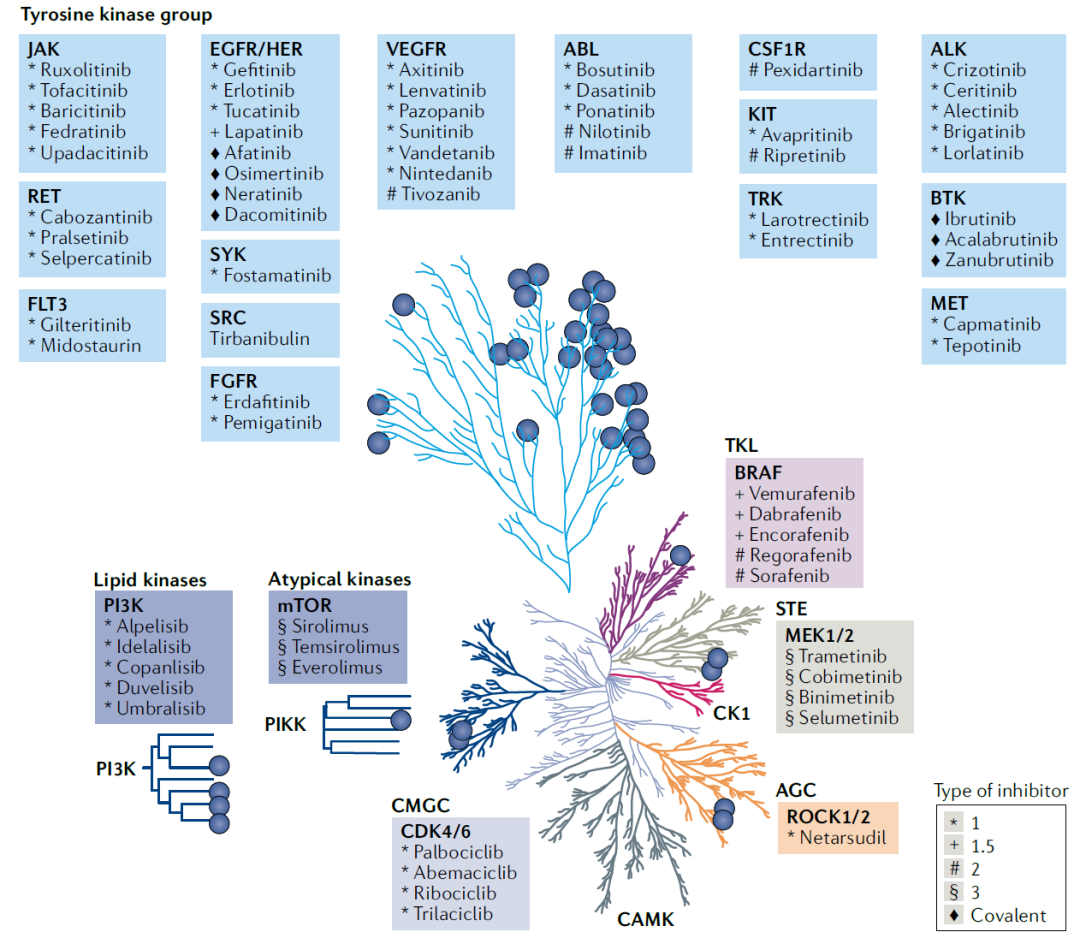
图2、批准的激酶抑制剂时间表,以及激酶抑制剂命名的后缀方式激酶和磷酸酶介导的蛋白磷酸化和去磷酸化在众多细胞生理过程中,扮演调控开关的角色,如细胞的增殖、凋亡,亚细胞水平的迁移、炎症及代谢等。人类激酶组共包括560种蛋白激酶,主要分为8种类别,如酪氨酸激酶(TK),非典型蛋白激酶等。激酶抑制剂作用靶点分布于21个激酶家族,约占人类激酶组的20%。其中以TK、TKL、STE、CMGC和AGC五类激酶家族的研究最为深入,以及非典型蛋白激酶及脂质激酶各有一个家族分布。即便研究最多的TK家族也有70%的靶点尚未开发,因此,激酶靶点的开发仍然具有很大的空间。图3、人类激酶组中,FDA批准的71个激酶抑制剂
靶向癌症的激酶抑制剂
易位或突变导致激酶异常激活,将驱动癌症的发生。对于这些驱动因素的识别和鉴定促进了分子靶向癌症治疗的发展,一个开创性的例子:BCR-ABL易位的识别促进Imatinib的诞生,BCR-ABL易位会导致酪氨酸激酶活性升高,最终驱动CML的发生。目前 FDA 批准的61个激酶抑制剂(89%) 和10个单抗(100%)的适应症均包括癌症。
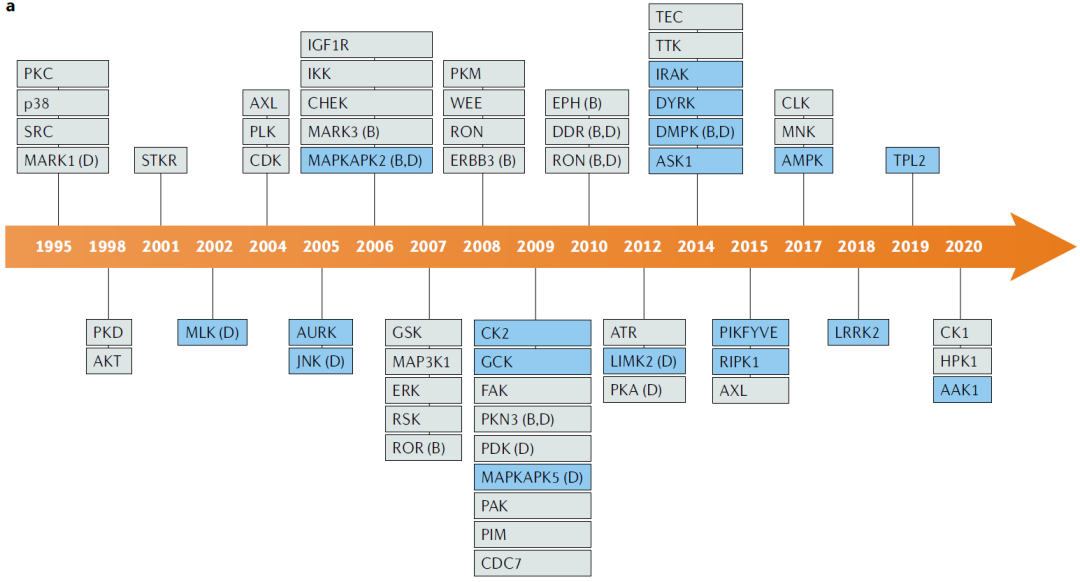
图4、新的激酶家族的靶向药物进入临床试验的时间表
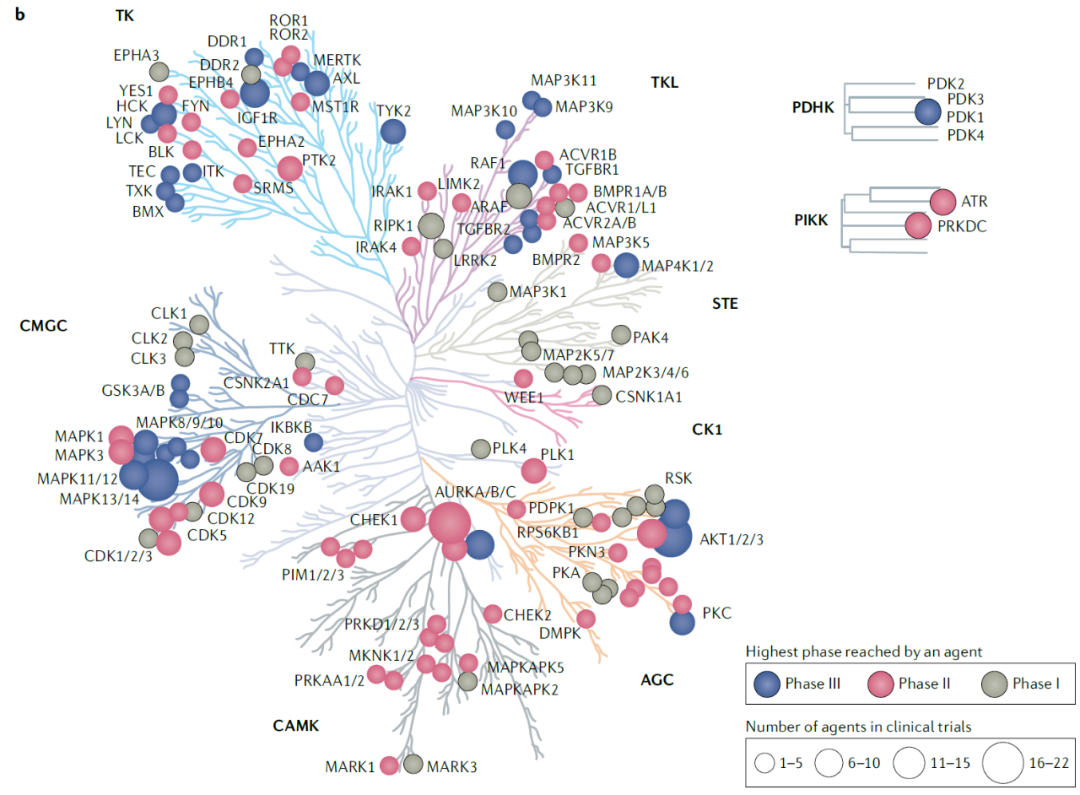
图5、小分子激酶抑制剂的激酶靶点映射到人类激酶组的系统发育树上
肺癌在所有癌症中死亡率位居第一,其中80~85%的肺癌属于非小细胞肺癌 (NSCLC) 。目前超过20%的药物 (19个激酶抑制剂和2个mAbs)被批准用于治疗NSCLC。
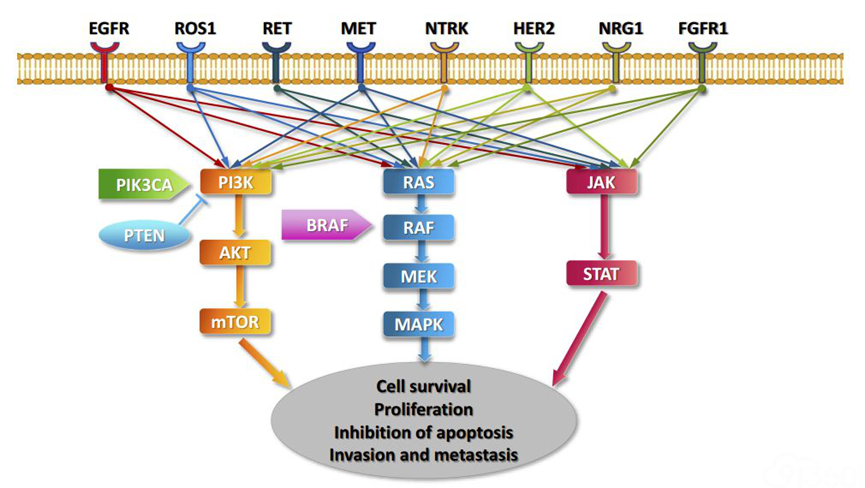
图6、NSCLC中11种致癌驱动基因的靶向治疗
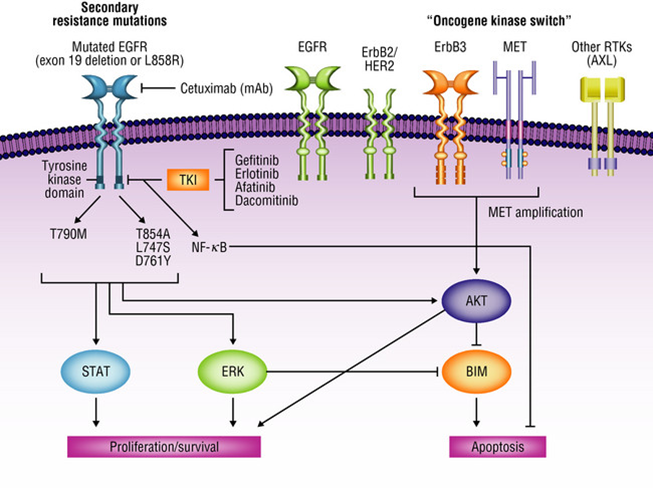
EGFR在肿瘤生长和发展中扮演重要角色。治疗NSCLC的第一代激酶抑制剂是靶向EGFR发挥作用,包括 Gefitinib 和 Erlotinib。由于基因突变常常导致耐药性,目前已开发针对突变的第二代抑制剂,包括Afatinib和Dacomitinib,以及第三代抑制剂Osimertinib,均已上市。
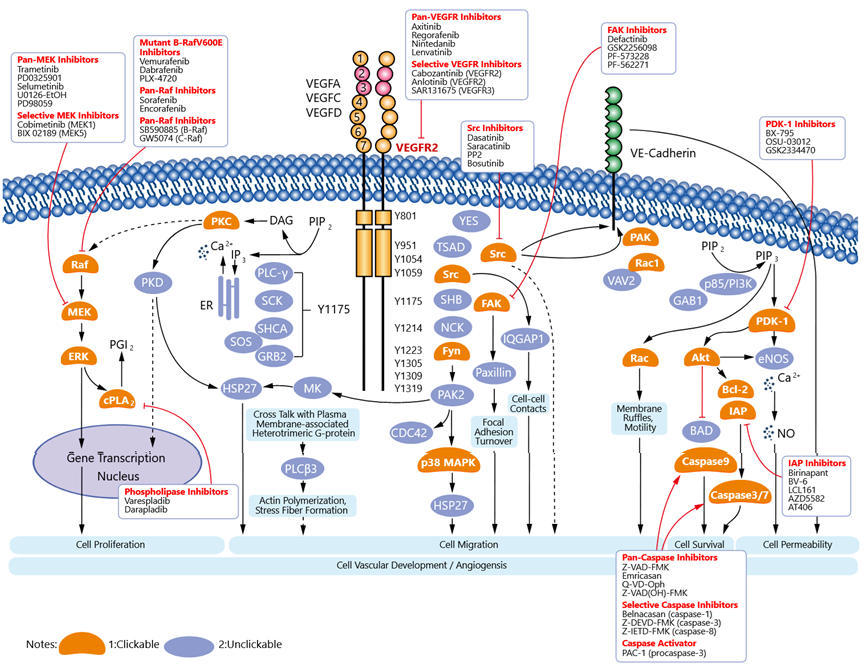
图7、EGFR信号通路图及抑制剂
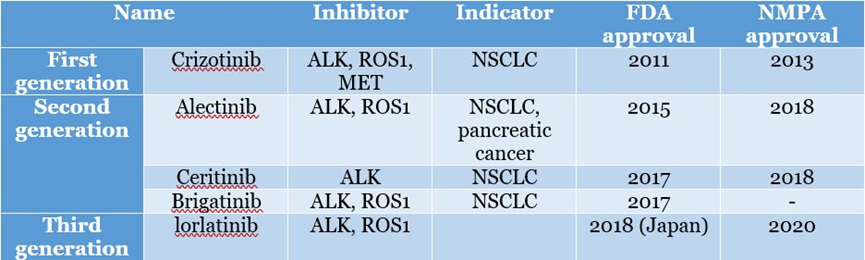
ALK重排会产生异常的ALK蛋白,促进癌细胞增殖和迁移,5% NSCLC患者出现ALK 重排。ROS1与ALK 紧密相关,也是ALK抑制剂的作用靶点,1~2% NSCLC患者中发生ROS1重排。Crizotinib是第一个ALK抑制剂药物,已于2011年批准上市。为了改善Crizotinib的活性和耐药性,科学家们开发了第二代和三代抑制剂,包括4个同时靶向ALK & ROS1的抑制剂,分别是Ceritinib、Alectinib、Brigatinib和Lorlatinib,均已上市。
图8、NSCLC中ALK & ROS1的靶向治疗药物
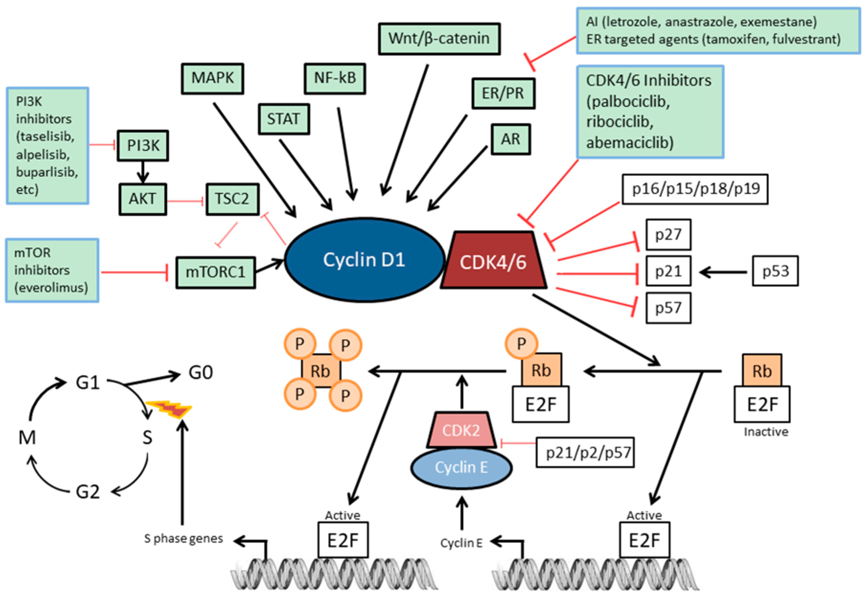
靶向抗肿瘤血管生成是一种重要的抗癌策略,许多激酶抑制剂靶向由VEGFR、PDGFR、KIT、FGFR和MET驱动的血管生成途径。其中5个FDA批准的激酶抑制剂和2个rapalogue抑制剂(Temsirolimus、Everolimus)分别通过抑制VEGFR信号通路和VEGFR下游的mTOR实现对肾癌的治疗。FDA批准的Ramucirumab 和中国批准的Fruquintinib 通过抑制VEGFR治疗转移性结直肠癌。VEGFR抑制剂Vandetanib、Cabozantinib和Lenvantinib,以及RET抑制剂Pralsetinib和Selpercatinib被批准用于甲状腺髓样癌的治疗。FDA批准的激酶抑制剂也靶向各种细胞内激酶,CDK4和CDK6在细胞分裂中发挥重要作用。Palbociclib、Ribociclib和Abemaciclib靶向CDK4/6,已经成为癌症尤其是乳腺癌的常规治疗药物。CDK4/6抑制剂Trilaciclib于2021年获批用于小细胞肺癌的骨髓保守治疗。
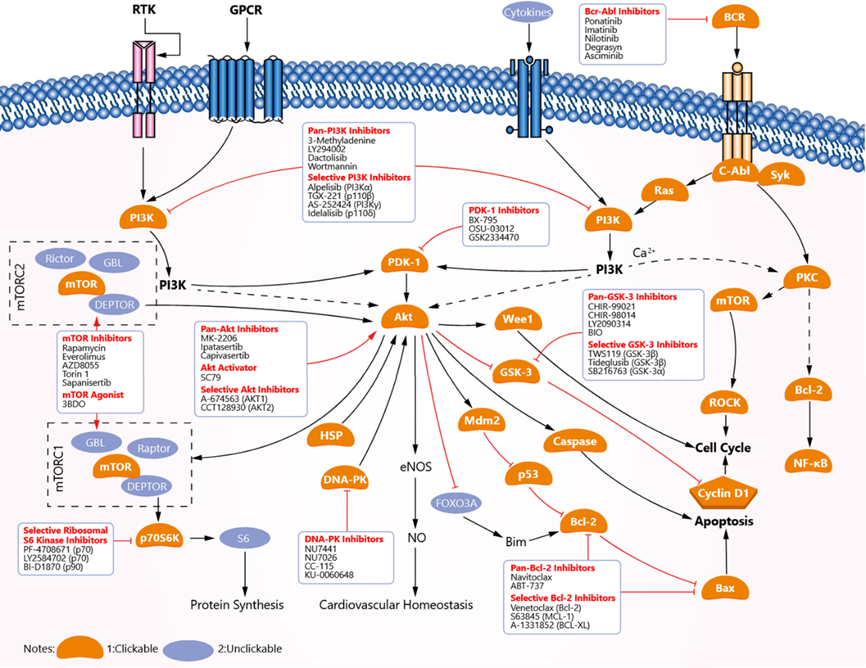
众多癌症的发生与PI3K-AKT-mTOR通路的失调密切相关,该通路参与细胞存活、代谢和细胞生长调节。Idelalisib是一种靶向PI3Kδ的抑制剂,2014年被FDA批准用于治疗各种淋巴瘤。2017年,靶向PI3Kα/β的双靶点抑制剂Copanlisib被批准用于治疗滤泡性淋巴瘤;2018年,靶向PI3Kδ/γ的双靶点抑制剂Duvelisib被批准用于几种淋巴瘤;2019年,PI3Kα选择性抑制剂Alpelisib被批准用于治疗乳腺癌。此外还有3种靶向于mTOR的抑制剂被批准用于癌症及其它适应症的治疗,包括Sirolimus——最早的激酶抑制剂之一。
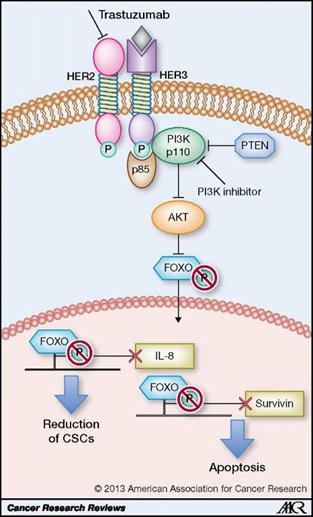
针对其他的RTK蛋白也已开发出相应的激酶抑制剂。目前已有 9 个获批的激酶靶向药物,其中最突出的是靶向HER2治疗乳腺癌的药物。1998年批准HER2靶向药物Trastuzumab,最近批准的HER2靶向药物为Margetuximab、lapatinib、Neratinib、Tucatinib和Pyrotinib,以及两个抗体药物偶联物Trastuzumab-emtansine、Trastuzumab-deruxtecan。靶向激酶治疗其他血液系统恶性肿瘤已取得实质性进展。已有3种FDA批准的Bruton激酶抑制剂正用于治疗套细胞淋巴瘤和慢性淋巴细胞白血病:Ibrutinib、Acalabrutinib和Zanubrutinib。研究发现NTRK家族蛋白是CRC致癌融合基因的组成部分。2018年,开创性的泛TRK抑制剂larotrectinib被FDA批准用于NTRK基因融合实体瘤的治疗,是继 Pembrolizumab 后第二个肿瘤不可知疗法(基于肿瘤分子特征而不考虑原发肿瘤的位置开发的治疗方法)抑制剂。之后 Entrectinib 被批准用于 NTRK 基因融合实体瘤的治疗,也成为了不可知疗法抑制剂的一员。其他激酶抑制剂也相继用于肿瘤不可知疗法,例如RET抑制剂Pralsetinib和Selpercatinib。
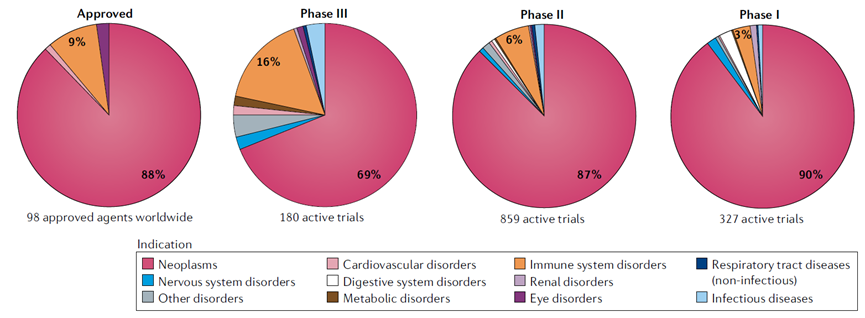
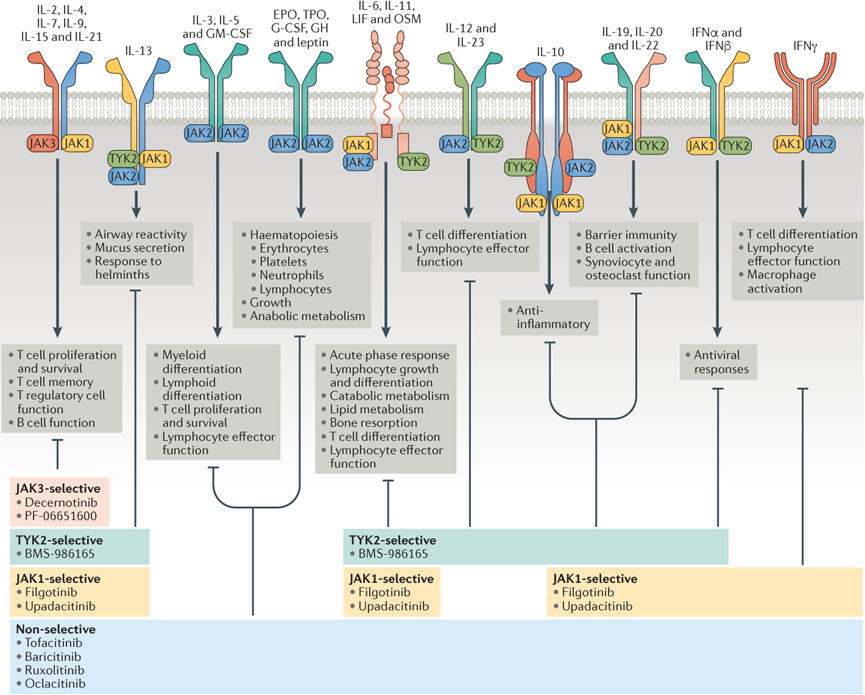
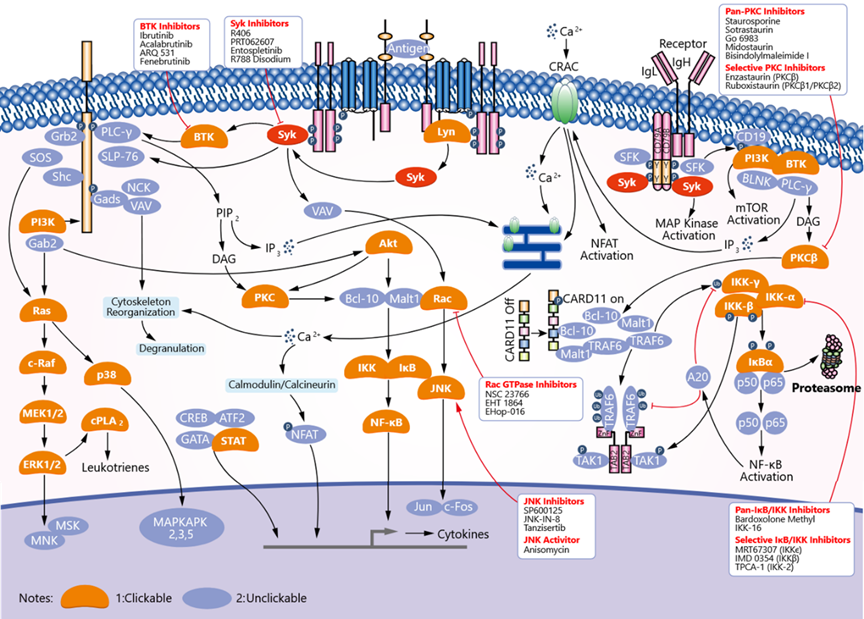
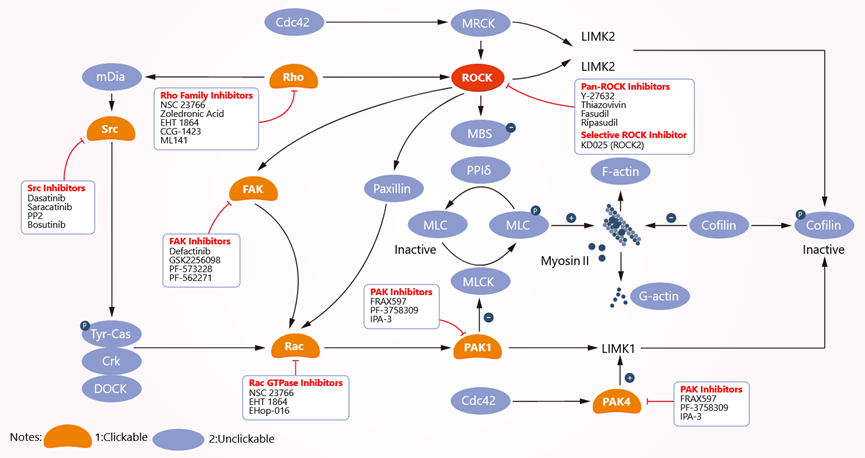
许多激酶参与免疫反应的调节。超过13%的激酶抑制剂(11个)已被批准用于免疫系统相关的适应症,主要是自身免疫性和炎症性疾病。图14、正在进行的临床试验和批准的药物之间的适应症分布JAKs是许多细胞因子的第二信使,例如干扰素、白介素等,在辅助T细胞 (TH1、TH2和TH17) 免疫反应中扮演重要的角色。2011年,JAK1和JAK2抑制剂Ruxolitinib被FDA批准用于中等或高危骨髓纤维化的治疗,这是第一个应用于癌症以外的激酶抑制剂。2019年,JAK2抑制剂Fedratinib也被批准用于治疗此疾病。在自身免疫性疾病中,类风湿性关节炎获批的激酶抑制剂数目最多(共5个),它们均选择性靶向JAK亚型。2012年,第一个被批准用于类风湿性关节炎的激酶抑制剂——Tofacitinib上市。之后,Baricitinib、Upadacitinib、Peficitinib和Filgotinib也相继上市。JAK抑制剂也被研究用于其他的免疫相关疾病,如 Delgocitinib第一个被批准用于特应性皮炎,于2020年在日本获批上市。SYK激酶参与先天性和适应性免疫反应。SYK激酶抑制剂用于治疗过敏、自身免疫性疾病以及血液恶性肿瘤。例如Ibrutinib和Ruxolitinib分别被批准用于预防器官移植排斥及移植物抗宿主病。Fostamitinib用于慢性免疫性血小板减少症,能够减少抗体介导的血小板破坏。还有几种激酶抑制剂被批准用于癌症和免疫性疾病以外的适应症。ROCK1/ROCK2 抑制剂Fasudil用于治疗脑血管痉挛,另一个ROCK1/ROCK2抑制剂Netarsudil用于治疗青光眼和高眼压症;mTOR抑制剂Everolimus用于结节性硬化症患者中部分性癫痫发作者的治疗;VEGFR抑制剂Nintedanib用于治疗特发性肺纤维化;FLT3抑制剂Midostaurin用于治疗晚期系统性肥大细胞增多症。截至目前,小分子抑制剂的临床试验信息显示大约有110个激酶正被开发为新的靶点,这些靶点加上已获批激酶抑制剂的45个靶点,仅占人类激酶组的30%,因此激酶抑制剂的开发仍有巨大的空间。

[1] Misty
M Attwood, et al. Trends in kinase drug discovery: targets, indications and inhibitor
design. Nat Rev Drug Discov. 2021
[2] Philip
Cohen, et al. Kinase drug discovery 20 years after
imatinib. Nat Rev Drug Discov. 2022
[3] selleck.cn官网
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。








发表评论
注册或登后即可发表评论
登录注册
全部评论(0)