咚咚咚,大家好,癌症相关成纤维细胞(CAF)相信大家都不陌生。之前已经有相关文章出现(见下图),影响因子还不低:杂志Hepatology(IF:17+)。这篇文章讲述了基于实验发现CAF可以通过分泌IL6和IL33调控MDSCs(骨髓源性抑制细胞)来达到最佳微环境以提高肿瘤干性。
肿瘤组织中大量的肿瘤相关成纤维细胞(cancer associated fibroblasts, CAFs)为肿瘤的发展构建了良好的环境(占基质细胞50%以上)。CAFs在癌症中扮演重要作用:CAFs不仅可通过分泌多种细胞因子或代谢产物抑制免疫细胞的功能,促进肿瘤发展、侵袭、转移;CAFs 还具有塑造肿瘤外基质、形成药物或治疗性免疫细胞渗透屏障的阻止药物与免疫细胞向肿瘤组织的深层渗透,从而降低肿瘤治疗效果。因此,通过调控 CAFs 或克服其屏障作用抑制肿瘤是肿瘤治疗的新手段。
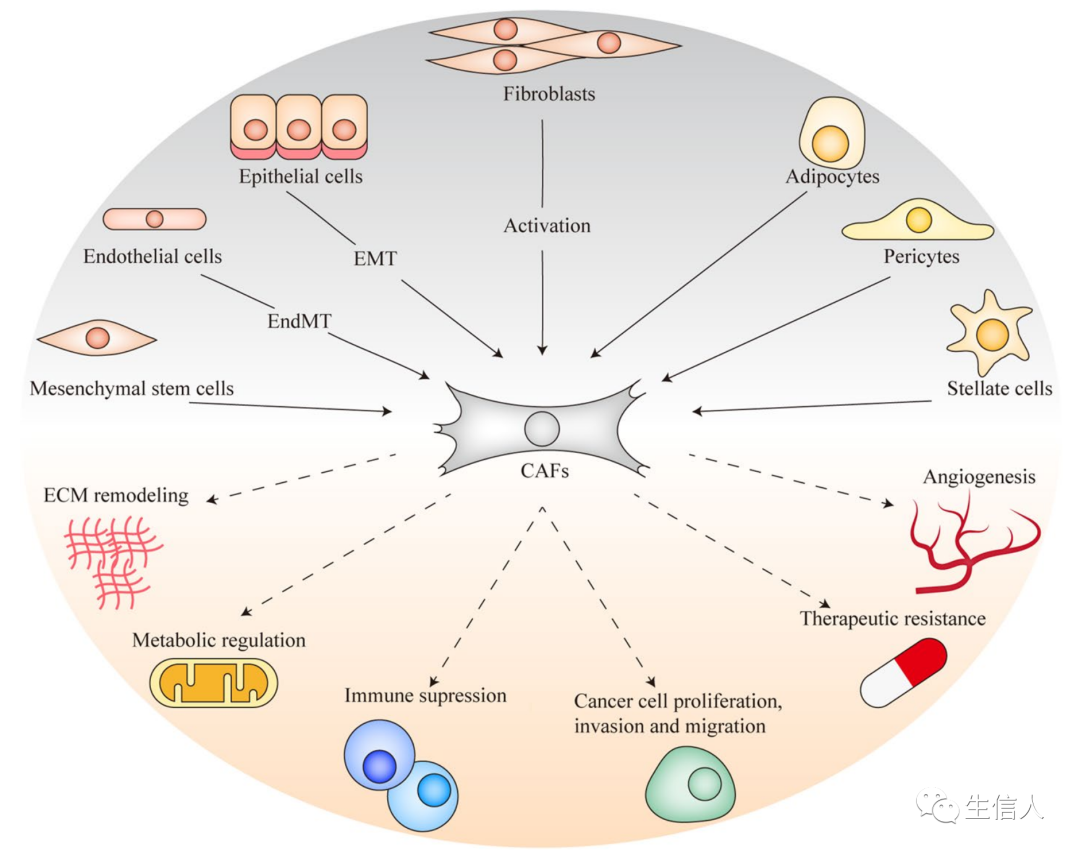
(Ref:doi.org/10.1186/s12943-021-01463-y; IF:27)1、来源:主要是由组织中固有成纤维细胞或星状细胞在生长因子,e.g.转化生长因子-β(TGF-β)刺激作用下转变为 CAFs;此外,肿瘤组织中的上皮细胞、内皮细胞、骨髓间充质干细胞(MSC)等细胞也可分化为CAFs(Ref:PMID: 30470818; IF:84)。2、肿瘤组织中CAFs异质性:不同亚型CAFs表面标志物表达情况不同,如成纤维细胞活化蛋白(FAP)、α-平滑肌动蛋白(α-SMA)、成纤维细胞特异性蛋白1(FSP1)、血小板衍生生长因子受体(PDGFR)等。FAP被认为是 CAFs 特异性表达蛋白,因此FAP被广泛用作靶向CAFs的靶标用于肿瘤治疗或影像学诊断。α-SMA是活化成纤维细胞的标志,通常作为靶向CAFs治疗效果的一个主要评价指标。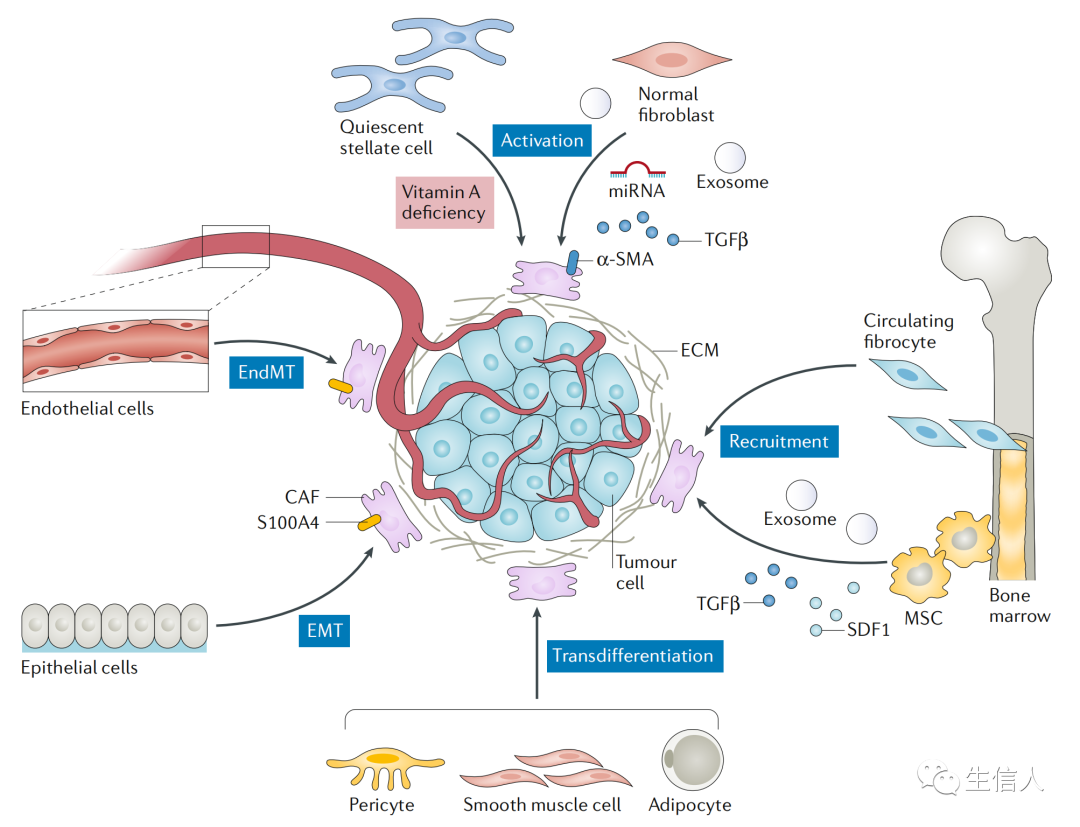
(Ref:PMID:30470818; Nat Rev Drug Discov;IF:84)CAFs 通过分泌各种细胞因子与其他基质细胞、肿瘤细胞进行信息交流,抑制免疫细胞功能,促进肿瘤发展。CAFs可分泌一系列细胞因子: 如血管内皮生长因子(VEGF)可调控肿瘤血管网;TGF-β抑制DC成熟、促进Treg分化;白细胞介素6(IL-6)可促进MDSC分化,抑制细胞毒性T细胞;CXCL12使肿瘤细胞抗凋亡蛋白Bcl-2和Survivin上调从而产生耐药性等;CAFs可调控胞外基质,对药物与免疫细胞的浸润产生屏障作用。CAFs 通过分泌大量胶原、纤连蛋白等促进肿瘤外基质固化,抑制由肿瘤组织分泌趋化因子招募的免疫细胞、抗肿瘤药物的渗透;CAFs进行糖酵解排出大量乳酸与氢离子,形成酸性微环境,抑制免疫细胞活性。此外,CAFs能诱导上皮细胞发生上皮-间质转化;CAFs 产生的大量细胞外基质还能增加微环境刚性和间质压力,促进肿瘤的侵袭与迁移;CAFs 产生的乳酸和丙酮酸等代谢产物还能作为肿瘤细胞营养物质,支持肿瘤代谢。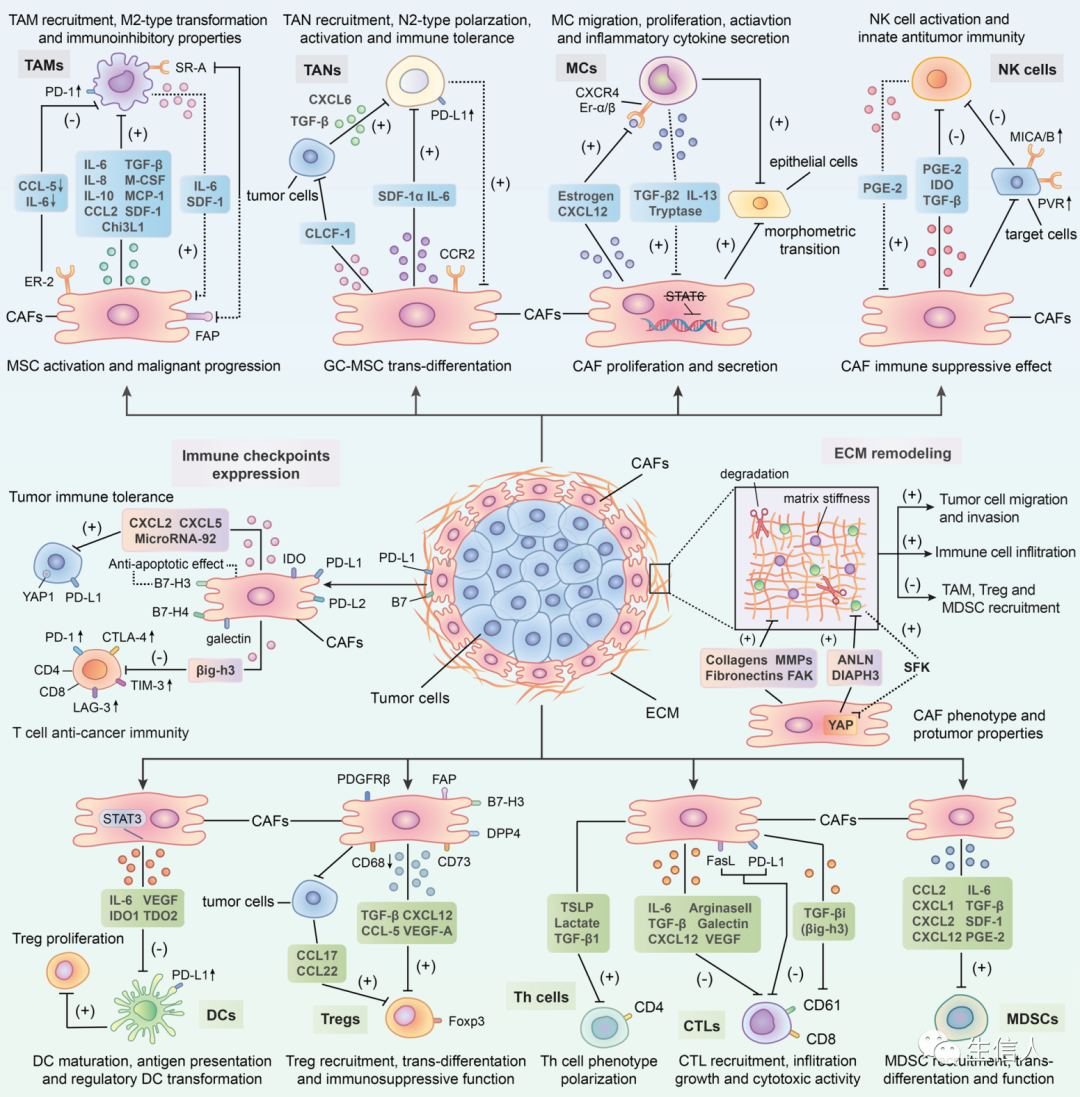
(Ref:PMID:34635121; Mol Cancer;IF:27)
通过上述介绍我们已经知道CAFs 对肿瘤发展有着重要的促进作用。因此,靶向调控 CAFs的肿瘤治疗策略有望抑制肿瘤进展。但传统药物递送策略仍存在药物分布特异性不足、易产生系统毒性等问题从而限制这一肿瘤治疗新策略的发展。纳米载体因其具备靶向递送能力、药物可控释放和生物相容性好等特点,应用于靶向调控CAFs治疗策略可增强药物在靶部位的蓄积,提高耐受剂量并增强疗效。目前靶向调控CAFs的肿瘤治疗策略主要包括杀伤CAFs、干扰 CAFs 功能和干扰 CAFs 活化。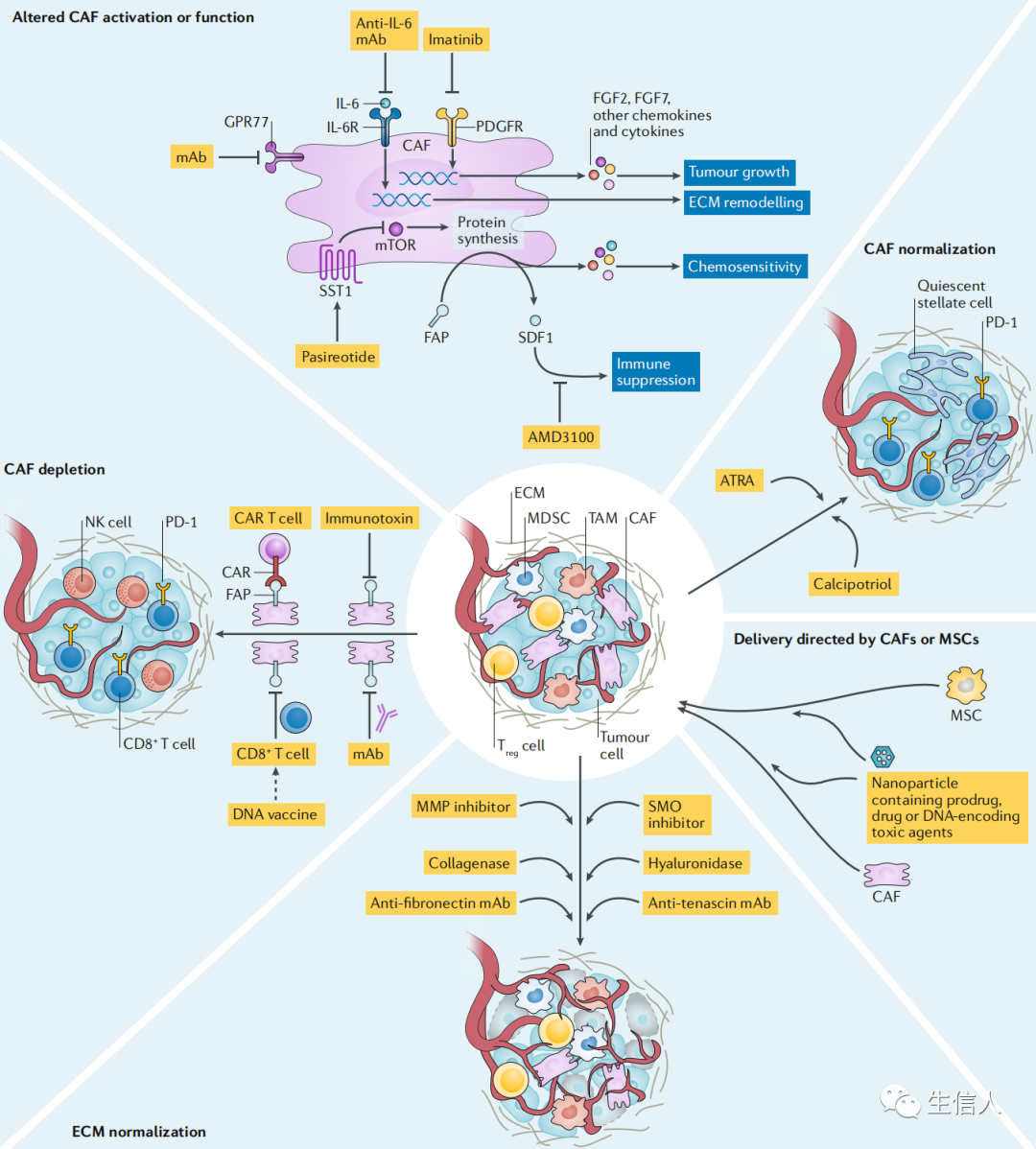
(Ref:PMID: 30470818; Nat Rev Drug Discov; IF:84)1、Cancer associated-fibroblast-derivedexosomes in cancer progression(Mol Cancer;IF: 27+;21年12月)在这篇综述专注于CAF衍生的外泌体在癌症进展中的作用。首先介绍CAFs 在癌症发展中的作用以及CAFs如何与TME中的其他细胞通信。然后描述了CAF衍生的外泌体如何调节肿瘤细胞和TME的其他细胞。最后,由于外泌体在肿瘤生长相关的异质生物学过程并具有治疗潜力,作者还讨论了外泌体的临床应用,特别是在免疫检查点治疗的增效作用。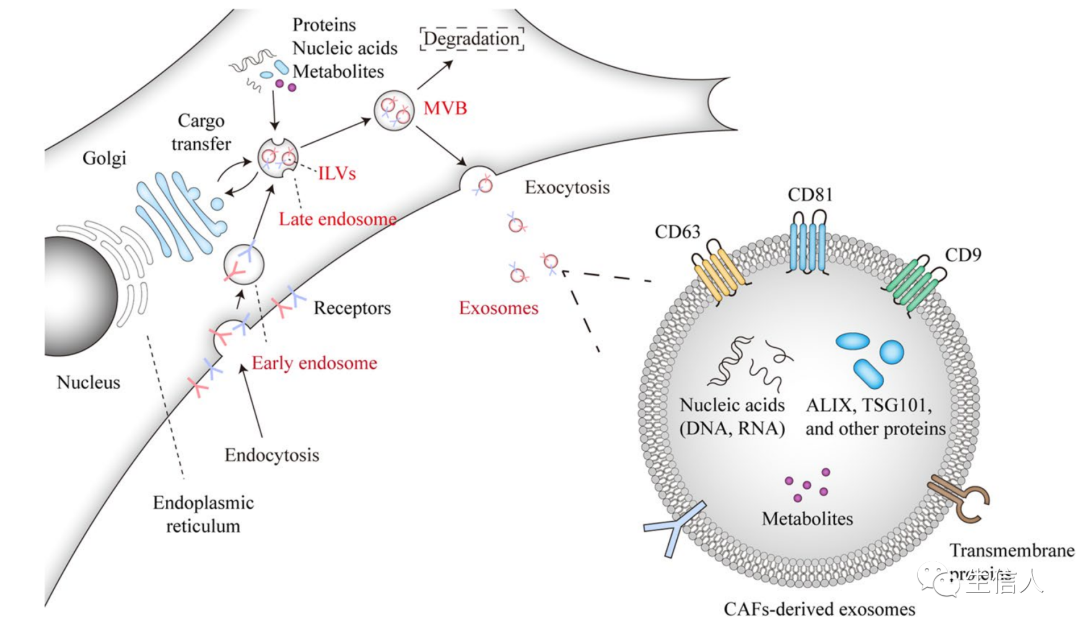
2、中山大学肿瘤防治中心和香港大学的关新元团队在Science Advances(IF:14+)杂志上发表文章《Laminin gamma 2–mediating T cell exclusion attenuates response to anti–PD-1 therapy》揭示了癌症相关成纤维细胞与肿瘤细胞相互作用,抑制T细胞浸润,降低PD-1抗体药物疗效的新机制。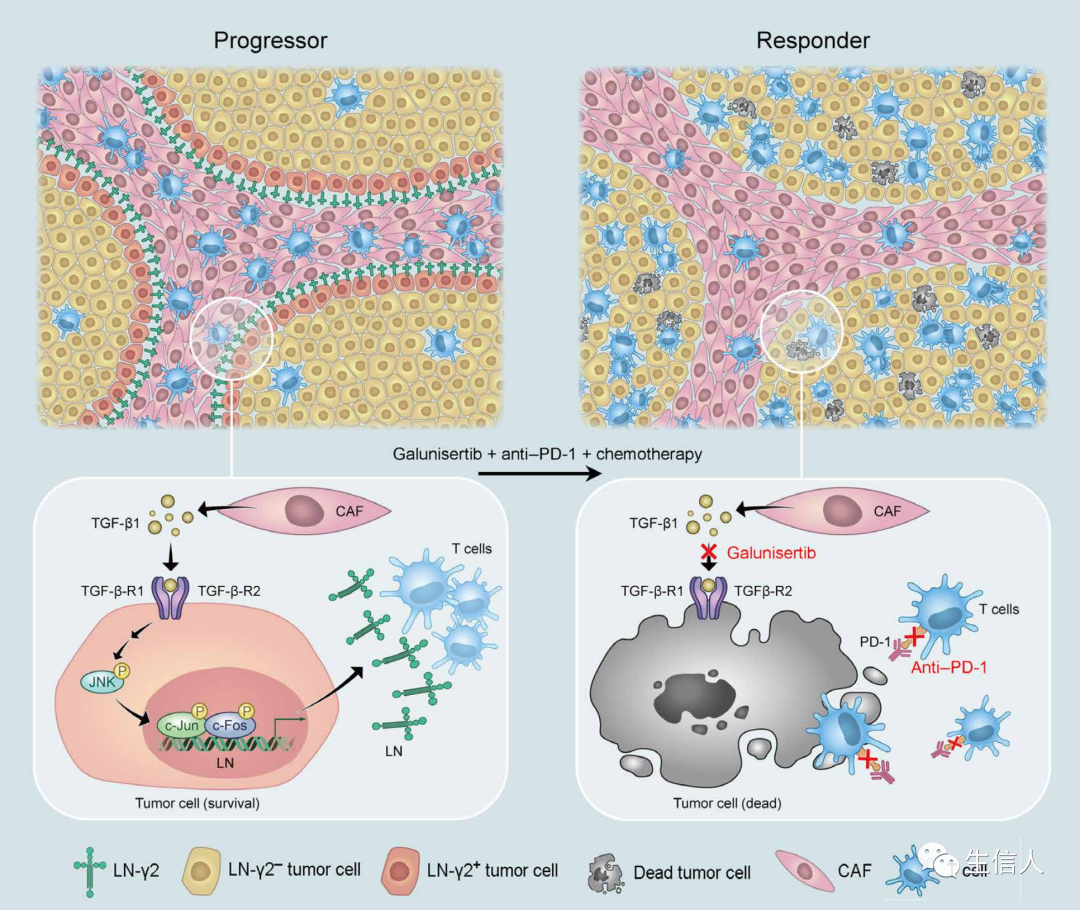

该研究依据癌症相关成纤维细胞 (CAF) 具有高度的异质性。缺乏对不同CAF之间功能区别的全面认识,目前仍无法基于患者肿瘤中的CAF制定个体化治疗方案。研究建立了一个来自非小细胞肺癌 (NSCLC) 患者活检的 CAF 生物库,其中包含临床 NSCLC中CAF 的广泛分子谱。通过对接受相同治疗的患者追溯 CAF功能上的异质性,确定了三种功能亚型。CAF功能分类与患者对靶向治疗的临床反应相关,也与肿瘤免疫微环境相关,为个体化治疗提供了指导。以此为灵感,我们是否能基于CAF marker在癌症中做亚型的研究呢 。
。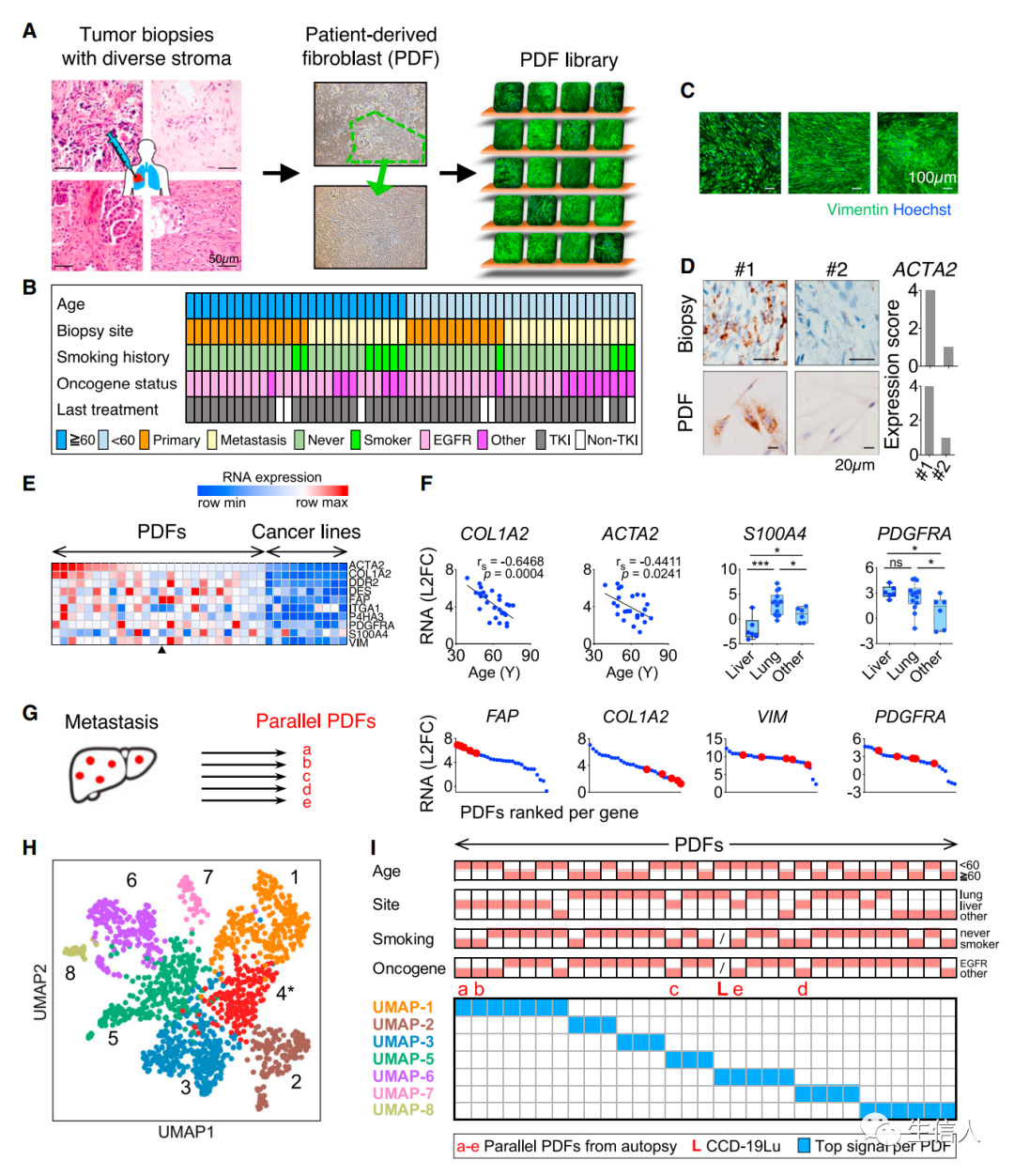
建立活体生物样本库充分捕捉非小细胞肺癌CAF异质性今天的CAF专题分享到这里就结束了,大家读完后是不是有收获。如果没有建议重新看一遍 。总之而言,肿瘤相关成纤维细胞不仅促进肿瘤的发生、增殖、浸润、转移和耐药,同时参与血管生成、淋巴管生成、细胞外基质重塑、重构微环境等诱发癌症的事件,还对耐药有十分重要的影响。说了那么多,研究它SCI肯定没跑了。
。总之而言,肿瘤相关成纤维细胞不仅促进肿瘤的发生、增殖、浸润、转移和耐药,同时参与血管生成、淋巴管生成、细胞外基质重塑、重构微环境等诱发癌症的事件,还对耐药有十分重要的影响。说了那么多,研究它SCI肯定没跑了。
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。








 。
。
 。总之而言,肿瘤相关成纤维细胞不仅促进肿瘤的发生、增殖、浸润、转移和耐药,同时参与血管生成、淋巴管生成、细胞外基质重塑、重构微环境等诱发癌症的事件,还对耐药有十分重要的影响。说了那么多,研究它SCI肯定没跑了。
。总之而言,肿瘤相关成纤维细胞不仅促进肿瘤的发生、增殖、浸润、转移和耐药,同时参与血管生成、淋巴管生成、细胞外基质重塑、重构微环境等诱发癌症的事件,还对耐药有十分重要的影响。说了那么多,研究它SCI肯定没跑了。




发表评论
注册或登后即可发表评论
登录注册
全部评论(0)