2013年,James Rothman、Randy Schekman 和 Thomas C. Südho 三位科学家因发现细胞囊泡运输与调节机制而荣获诺贝尔生理学或医学奖。
此后的十年里,作为细胞囊泡主要类型的外泌体(Exosome)开启“狂飙”模式,大量科研经费投入,每年数千篇论文发表,成为当仁不让的科研热点。
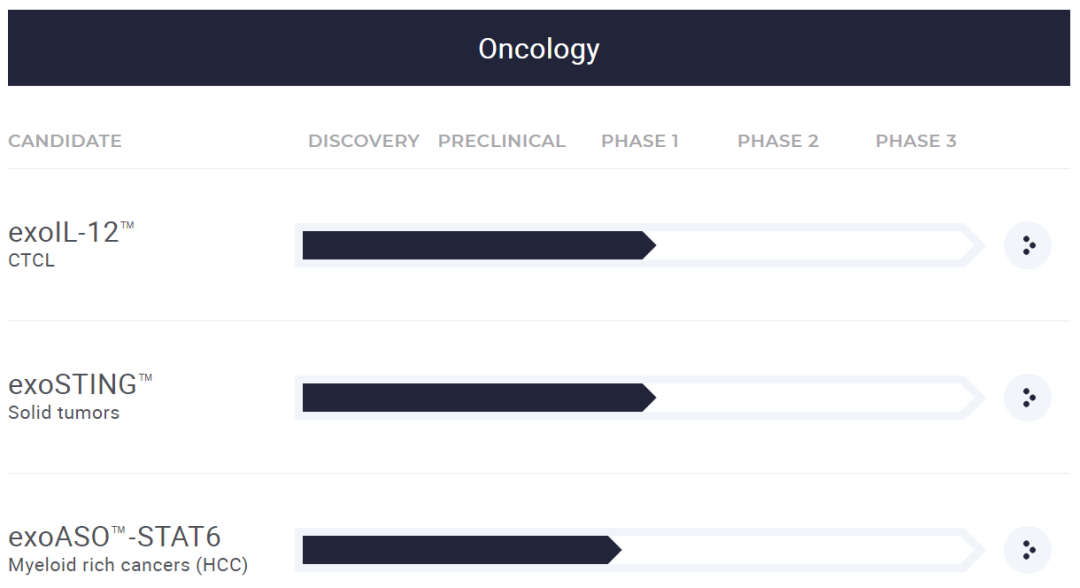
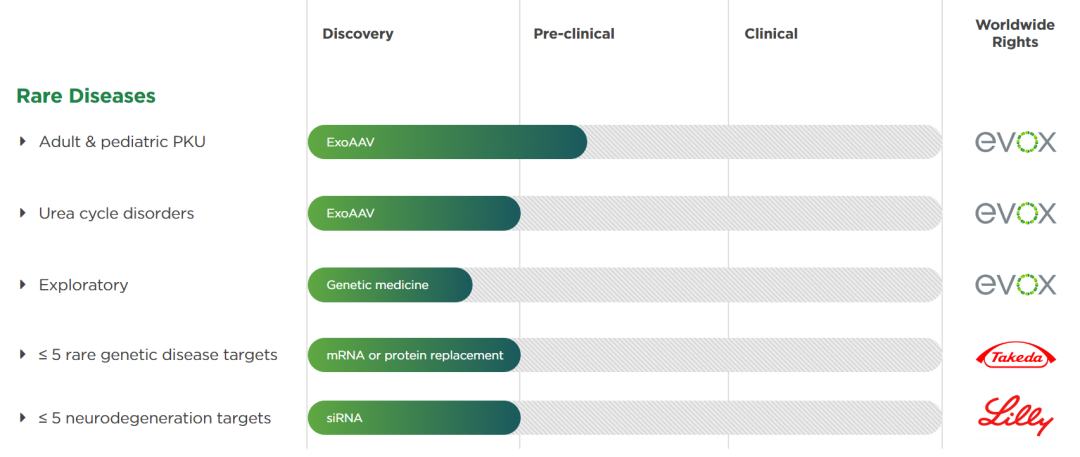
因为具有作为药物递送载体的潜力,外泌体同样备受产业界关注。在这十年里,有多大数十家外泌体研究公司创立并获得融资,分布在疾病治疗、疫苗研发、疾病诊断、医美修复等多个领域。其中最具代表性就是Codiak BioSciences,Codiak是全球首家外泌体医疗科技公司,成立于2015年,由著名风投机构Flagship参与孵化。2020年,Codiak首次将外泌体疗法推进到人体临床试验,并在随后登陆纳斯达克。外泌体不仅备受资本市场青睐,同样也受到制药巨头追捧,2018-2020年之间,罗氏、爵士制药、武田制药和礼来分别与几家外泌体公司签订了10亿美元级的大额合作,其中,爵士制药与Codiak在2019年签订了超10亿美元的合作开发计划,预付款5600万美元开发基于外泌体的癌症疗法。2023年3月27日,Codiak宣布已申请破产保护,并将在合理可行的情况下为整体业务或核心资产寻求买家。这也意味着Codiak对外泌体疗法的尝试走到了尽头。外泌体(Exosome),细胞外囊泡(EV)的一种主要类型,是直径为30-150nm的纳米大小的膜结构,大多数细胞都会分泌外泌体,通过其携带的蛋白质、核酸、脂质和代谢物等来发挥细胞间通讯功能,参与免疫应答、病毒感染、代谢和心血管疾病、神经退行性疾病以及癌症进展等多种生理和病理过程。相较于AAV等病毒载体和LNP等非病毒载体,天然来源的外泌体具有组织相容性高、可到达常规载体无法到达的组织和细胞、载体容量大、生产成本低等诸多优势,被认为是一种理想的新型药物递送载体。然而,开发新型递送载体的道路上坎坷不断,曾经备受期待的红细胞载药就是前车之鉴。Rubius Therapeutics是全球首家红细胞治疗研发公司,曾将基因工程改造的红细胞疗法推进到人体临床试验,市值一度高达18亿美元。但后续临床进展不利,在进行了大面积裁员、砍临床管线、转型等尝试后,也未能扭转乾坤。2023年2月,Rubius宣布解散。Rubius的这些经历也在Codiak上一一出现,这两家公司也都是由Flagship参与孵化。去年8月份,Codiak宣布解雇超过三分之一的员工,只剩了53名全职员工,并且暂停了两个处于临床试验阶段的研发管线,分别是exoSTING和exoIL-12,前者是通过外泌体递送STING的小分子激动剂,用于治疗多种实体瘤,后者是通过将IL-12表达在外泌体表面,用于治疗早期皮肤T细胞淋巴瘤。然后,Codiak将资源集中在硕果仅存的临床管线exoASO-STAT6上,该项目通过外泌体选择性递送反义寡核苷酸(ASO),破坏肿瘤相关巨噬细胞中的STAT6信号,诱导抗肿瘤免疫反应。临床前研究显示,该疗法在侵袭性肝细胞癌模型具有治疗潜力。此时,Codiak还保留了其engEx-AAV发现平台,这是一项旨在增强AAV基因治疗的战略。新冠疫情爆发后,Codiak还开发了基于外泌体的疫苗项目——exoVACC,旨在开发针对泛β冠状病毒的疫苗,希望提供对新冠病毒及变种和其他冠状病毒的广泛保护性免疫。Codiak首席执行官 Douglas Williams 博士在新闻稿中表示,董事会和管理团队已经全面评估了公司所有的战略选择,考虑到财务需求及现有的临床和研究项目,这已经是Codiak的最佳解决方案了。公司管理团队将于下周结束离开,只有首席技术官 Konstantin Konstantinov 博士暂时留任。除了Codiak,另一家备受关注的外泌体制药公司Evox,致力于开发通过外泌体递送的罕见病疗法。2021年2月,Evox完成约9500万美元的新一轮融资,将推进其外泌体疗法进入临床试验,如今两年多过去了,其研发管线仍全部停留在临床前阶段。与武田和礼来签订两项十亿美元级合作,也尚未获得进展。ir.codiakbio.com/news-releases/news-release-details/codiak-biosciences-pursue-asset-sale-through-voluntary-chapter
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。









发表评论
注册或登后即可发表评论
登录注册
全部评论(0)