
*仅供医学专业人士阅读参考
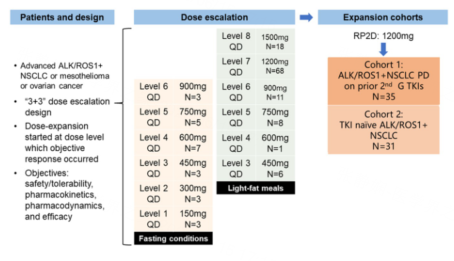
随着肺癌驱动基因的发现及药物研发的快速发展, 晚期非小细胞肺癌(NSCLC)靶向治疗取得长足的进步, 大大降低NSCLC的死亡率。作为NSCLC常见两个驱动基因EGFR和ALK的相关治疗已逐渐成熟,相比之下,少见突变靶点的治疗仍然面临很大挑战。在2023年美国临床肿瘤学会(ASCO)大会上,少见突变靶点的相关研究取得突破性进展, 有望改变少见靶点突变NSCLC的治疗格局,小编特整理成文,为临床医生带来NSCLC少见靶点最新资讯。BI 1810631用于晚期HER2 NSCLC患者,结果出炉[1]在实体瘤治疗中,针对HER2突变的有效酪氨酸激酶抑制剂(TKIs)的需求尚未得到满足,BI 1810631作为一种高效选择性HER2 TKI,可与野生型和突变型 HER2 受体共价结合,包括EGFR外显子20插入 (ex20ins)。Beamion Lung 1是一项正在进行的Ia/Ib期研究(NCT 04886804),旨在探索BI 1810631单药在 HER2+实体瘤患者中的安全性和初步疗效,本研究公布的是Ia 期的初步结果。在 Ia 期,入组难治或不适合标准治疗且存在 HER2 突变(例如过表达、基因扩增、体细胞突变或基因重排)的晚期、不可切除或转移性实体瘤患者。试验设计从开始接受15 mg(每日两次,BID)或者60 mg(每日一次,QD)的BI 1810631治疗,再逐渐递增剂量(图1)。在Ib期,最初纳入30例既往接受过治疗的晚期 HER2+ NSCLC 患者,后期也可纳入其他队列患者。试验的主要终点:基于DLT(剂量限制毒性)的最大耐受剂量(MTD), MTD评价期发生DLT的患者人数(Ia期);客观缓解率(ORR,Ib期)。截至2023年1月23日,共有36名患者接受治疗,包括NSCLC(n = 22)、结直肠癌(n = 3)和其他肿瘤(n = 11),大多数患者(n = 26)有病理性HER2突变。患者接受剂量15、30、60、100、150 mg BID(n = 3/3/4/4/3)或60、120、180、240、300 mg QD(n = 5/4/5/4/1)治疗(图2)。结果显示,在安全性方面,3例患者出现DLT(2级水肿,3级贫血,3级谷丙转氨酶[ALT]升高)。最常见的不良事件(AEs)为腹泻(n = 10),贫血(n = 5);碱性磷酸酶升高、肌酐升高、ALT升高、低白蛋白血症(均n = 4);低钙血症、AST升高、皮肤干燥、GGT升高(均n = 3)。同时,患者在所有剂量水平上均观察到疗效,总体ORR达37%,DCR达89%,在24例可评估的NSCLC患者中疗效更佳,ORR达46%,DCR达96%,其中10例达部分缓解(PR),11例达疾病稳定(SD)。在其他肿瘤,2例达PR(1例食道癌、1例胆管癌)(图3)。NSCLC患者:METex14 vs 高水平MET扩增,人群特征有哪些不同?[2]在NSCLC中,MET酪氨酸激酶受体可因突变和/或基因扩增而失调。最常见的MET突变位于外显子14,为MET14外显子跳跃突变(METex14),会使受体降解受损,增加MET介导的信号传导,进而导致肿瘤的持续增殖。而MET扩增也会导致持续的MET信号传导和肿瘤发生,可能是靶向治疗耐药的机制之一。基于此,研究者设计研究比较METex14和高水平MET扩增肿瘤的基因组图谱(图4)。试验针对18047例 NSCLC 肿瘤 (任何分期/亚型) ,使用Tempus xT 检测测序 [500x覆盖度下的648个基因测序 (DNA-seq) 和全转录组测序 (RNA-seq) ] 进行分析。在MET突变组和MET野生型组(METwt,17606例)之间使用免疫肿瘤学(IO)生物标志物进行比较。结果显示,共有276例METex14突变患者、138例高MET扩增(拷贝数CNG≥10,METamp)患者和27例其他MET突变(METother)患者。与METamp和METwt相比,METex14组偏向于年龄较大、不吸烟、女性的患者,且肿瘤突变负荷(TMB)表达更低(图5)。同时METex14 NSCLC患者PD-L1阳性率为82%,高于METamp的75%和METwt的57%(图6)。值得注意的是,与METex14相比,METamp表现出TP53(83% vs 37%)、TFE(46% vs 1.1%)、CFTR(37% vs 1.4%)、EGFR(31% vs 7.6%)、WNT2(11% vs 0.4%)、KEAP1(14% vs 0.7%)和STK11(8% vs 1.4%)的突变发生率增长,MDM2(4.3% vs 14%)和FRS2(2.9% vs 12%)的突变发生率降低(图7)。针对靶向治疗耐药NSCLC患者,APG2449或有望改变治疗困境[3]APG2449作为一种三代TKI口服靶向药,针对ALK、ROS1以及FAK等靶点都具有良好的活性。既往二代ALK靶向药耐药后的NSCLC患者,往往存在G1202R等原位ALK位点突变,或者旁路激活耐药。而APG2449对G1202R等位点具有显著活性,本次ASCO大会报道关于APG2449的临床研究,旨在评估 APG-2449用于二代 ALK 抑制剂耐药后的NSCLC 患者的安全性和疗效。在确定II期临床试验推荐剂量为每日1200mg,QD后,将NSCLC患者分为2个剂量扩展队列。TKI组:对接受第二代TKI治疗后耐药ALK/ROS-1阳性患者;TKI-naïve组:包括ALK/ROS-1阳性初治患者(图8)。截至摘要公布时,入组的136例NSCLC、间皮瘤或卵巢癌患者接受 APG-2449治疗,剂量范围为900 ~ 1500 mg。安全性方面,在136例患者中,有123例患者至少出现了一个治疗相关不良事件(TRAE),占比为90.4%,有19例患者出现至少一个≥3级TRAE,占比为14%。大部分药物相关AEs都是轻度且可逆转的,如肌酐升高(46.3%),转氨酶升高(40.4%),恶心(27.2%),呕吐(22.8%)等,其中≥3级的严重不良事件(TRAEs)有9例(图9)。结果显示,在TKI-naïve组(n = 33),ROS1+和ALK+患者的ORR分别为70.6%和78.6%,疾病控制率(DCR)分别为88.2%和100%。在TKI组中(n=27),7例为PR(图10)。[1] John Heymach, et al.Phase I Beamion Lung 1 trial of BI 1810631, a HER2 tyrosine kinase inhibitor (TKI), as monotherapy in patients (pts) with advanced/metastatic solid tumors with HER2 aberrations: Updated data.2023 ASCO,Abstract 8545.[2] Rachel Minne, et al.Genomic comparison of MET exon 14 skipping and MET amplified non-small cell lung cancer.2023 ASCO,Abstract 8553[3]Yuxiang Ma, et al.FAK inhibition with novel FAK/ALK inhibitor APG-2449 could overcome resistance in NSCLC patients who are resistant to second-generation ALK inhibitors.2023 ASCO,Abstract 9015.
百度浏览
来源 : 医学界
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。














发表评论
注册或登后即可发表评论
登录注册
全部评论(0)