2010年,Carl June 教授率先将CAR-T细胞疗法推进到人体临床试验,并成功“治愈”了多名白血病患者。2017年,FDA首次批准了CAR-T疗法上市,如今,已有6款CAR-T疗法获得FDA批准用于治疗白血病和淋巴瘤等血液类癌症。而我们国内也已有几款CAR-T细胞疗法获批上市。CAR-T细胞疗法的成功应用,让许多在等待骨髓配型中绝望的癌症患者重新燃起了希望,也标志着细胞治疗时代的到来。然而,CAR-T细胞疗法仍然存在着诸多限制,包括成本高昂、制造周期长,以及副作用(细胞因子风暴、神经毒性等),还需要在专门的医疗中心进行治疗,这些因素严重限制了这种救命的疗法的可及性。现在,科学家们越来越关注更具成本效益、安全、有效的“现货型”细胞疗法。自然杀伤细胞(NK Cell)作为一种重要的免疫细胞,能够靶向杀伤癌细胞,可以被设计为CAR-NK细胞,并且无需严格的HLA(人白细胞抗原)匹配,具有开发成现货、通用细胞疗法的巨大潜力。2024年1月18日,德克萨斯大学MD安德森癌症中心的研究人员在 Nature Medicine 上发表了题为:Safety, efficacy and determinants of response of allogeneic CD19-specific CAR-NK cells in CD19+ B cell tumors: a phase 1/2 trial 的研究论文。
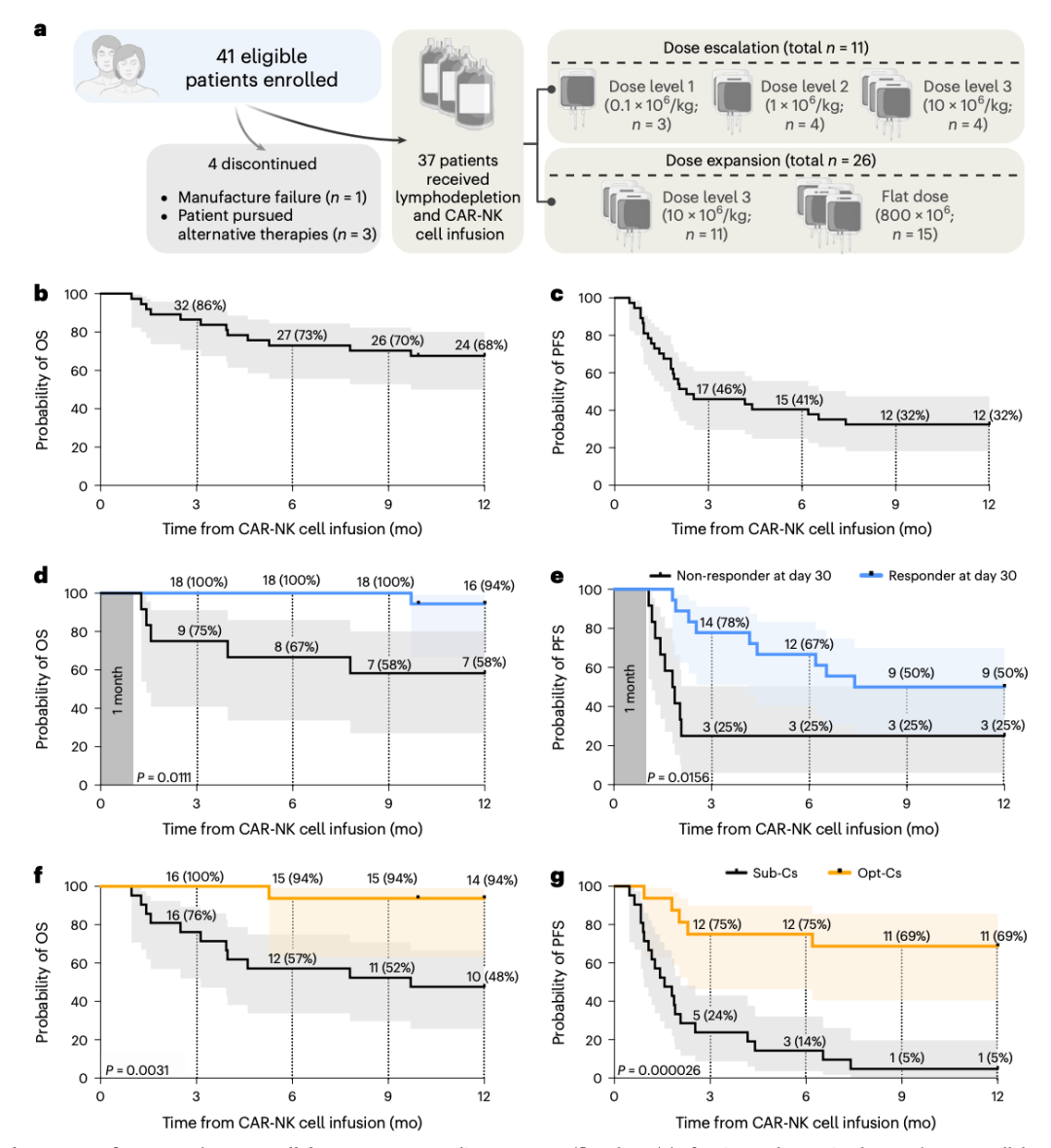
在这项针对37名复发或难治性CD19阳性的B细胞恶性肿瘤患者的1/2期临床试验中,脐带血来源的表达抗CD19 CAR和IL-15的CAR-NK细胞疗法,与自体CD19 CAR-T细胞疗法有相似的治疗效果,但安全性却大大提高,该CAR-NK细胞疗法未导致严重细胞因子风暴、神经毒性或移植物抗宿主病(GvHD)。这项研究还发现,从有核红细胞含量低且采集后24小时内冷冻保存的脐带血单位(CBU)中制造的CAR-NK细胞是获得优异治疗结果的最重要预测因素。该研究开发了一种CAR-NK细胞疗法——CAR19/IL-15 NK,通过逆转录病毒转导脐带血来源的NK细胞以表达抗CD19 CAR,还表达了IL-15来增强CAR-NK细胞在体内的扩增,还表达了诱导性caspase-9(iC9)自杀基因,可在出现不可接受的毒性作用情况下诱导CAR-NK细胞凋亡,从而增加其安全性。研究团队启动了一项1/2期临床试验,该临床试验共37名复发或难治性CD19阳性的B细胞恶性肿瘤患者参与,该试验旨在验证表达了抗CD19 CAR和IL-15的脐带血来源的NK细胞疗法(CAR19/IL-15 NK)的安全性和有效性。该临床试验的主要目标是安全性和有效性,定义为治疗第30天时的总缓解率(OR),次要目标包括第100天时的总缓解率(OR)、无进展生存期(PFS)、总生存期(OS)和CAR19/IL-15 NK细胞的持久性。试验结果显示,在第30天和100天时,接受治疗的患者的总缓解率(OR)均为48.6%,一年无进展生存率为32%、总生存率为68% 。此外,该试验报告了良好的安全性,患者没有出现严重细胞因子风暴、神经毒性或移植物抗宿主病(GvHD)。该试验的另一个关键发现是,用来制造CAR NK细胞的异体脐带血捐赠者的选择标准至关重要,采集后24小时内就冷冻的脐带血单位(CBU)和那些有核红细胞含量低(≤8×107)的脐带血单位(CBU)与明显更好的治疗结果相关。从这些脐带血单位(CBU)制造的的CAR NK细胞在给予患者治疗后,一年无进展生存率高达69%,一年总生存率高达94%,而那些有核红细胞含量高或采集至冷冻间隔时间较长的脐带血单位(CBU)制造的CAR NK细胞,在给予患者治疗后,一年无进展生存率和总生存率分别为5%和48%。这些结果表明,从有核红细胞≤8×107且采集后24小时内冷冻保存的脐带血单位(CBU)中制造的CAR-NK细胞是获得优异治疗结果的最重要预测因素。研究团队还实用多种小鼠模型证实了来自最佳CBU的CAR/IL-15 NK细胞在体内具有更优异的抗肿瘤活性。这些这些发现揭示了CAR-NK细胞生物学的新特征,并强调了异体细胞疗法中供体选择的重要性。论文通讯作者 Katayoun Rezvani 教授表示,在这些患者中观察到的反应非常令人鼓舞,团队将继续评估CAR NK细胞在治疗这些恶性肿瘤中的长期疗效。
www.nature.com/articles/s41591-023-02785-8
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。







发表评论
注册或登后即可发表评论
登录注册
全部评论(0)