2022-11-15 来源 : 学术查
Arginine Methylated Modification
精氨酸甲基化修饰(Arginine Methylated Modification)是常见的蛋白质翻译后修饰的类型之一,是指在底物蛋白的精氨酸胍基基团上形成甲基化修饰。催化形成精氨酸甲基化修饰的酶,被称为蛋白精氨酸甲基转移酶(protein arginine methyltransferase, PRMT),精氨酸甲基转移酶家族共有9位成员,分别是PRMT1-9,它们通过催化多种底物蛋白甲基化,影响底物蛋白稳定性、定位、活性,或者与底物蛋白相互作用,参与调控多种生理病理过程。研究发现,PRMT在肿瘤发生发展、耐药或者转移等过程中发挥调控作用,展现了作为肿瘤生物标记物或者治疗靶点的潜力,目前已有多款PRMT特异性抑制剂被研发,部分已经进入临床试验阶段。
近些年,关于蛋白质精氨酸甲基化修饰的高质量研究论文层出不穷,越来越多的研究证明PRMT具有重要的生理病理功能。近几年的国家自然科学基金的资助项目中,精氨酸甲基化修饰相关项目也不断增多。说明精氨酸甲基化修饰是当前生命科学和基础医学研究的热点之一。
小编为大家整理了5篇精氨酸甲基化修饰的相关高分文章,另附每篇文章的分子机制图和原文链接,有助于了解精氨酸甲基化的研究思路,感兴趣的文章可跳转具体链接研读全文。
★
1.Loss of PRMT7 reprograms glycine metabolism to selectively eradicate leukemia stem cells in CML
Cell Metabolism (IF 31.373)
Pub Date: 2022-06-07
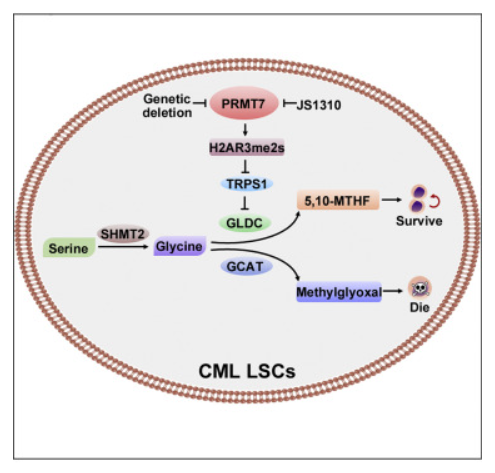
分子机制:敲除PRMT7的表达会显著抑制甘氨酸脱羧酶的表达,从而造成甘氨酸代谢紊乱,产生甲基乙二醛(methylglyoxal),影响白血病干细胞的功能。本研究阐述了蛋白质精氨酸甲基化修饰与甘氨酸代谢之间存在调控关系,表明PRMT7可作为急性慢性粒细胞白血病治疗靶点。
原文链接:
https://doi.org/10.1016/j.cmet.2022.04.004

2. Malic enzyme 2 connects the Krebs cycle intermediate fumarate to mitochondrial biogenesis
Cell Metabolism (IF 31.373)
Pub Date: 2021-05-04
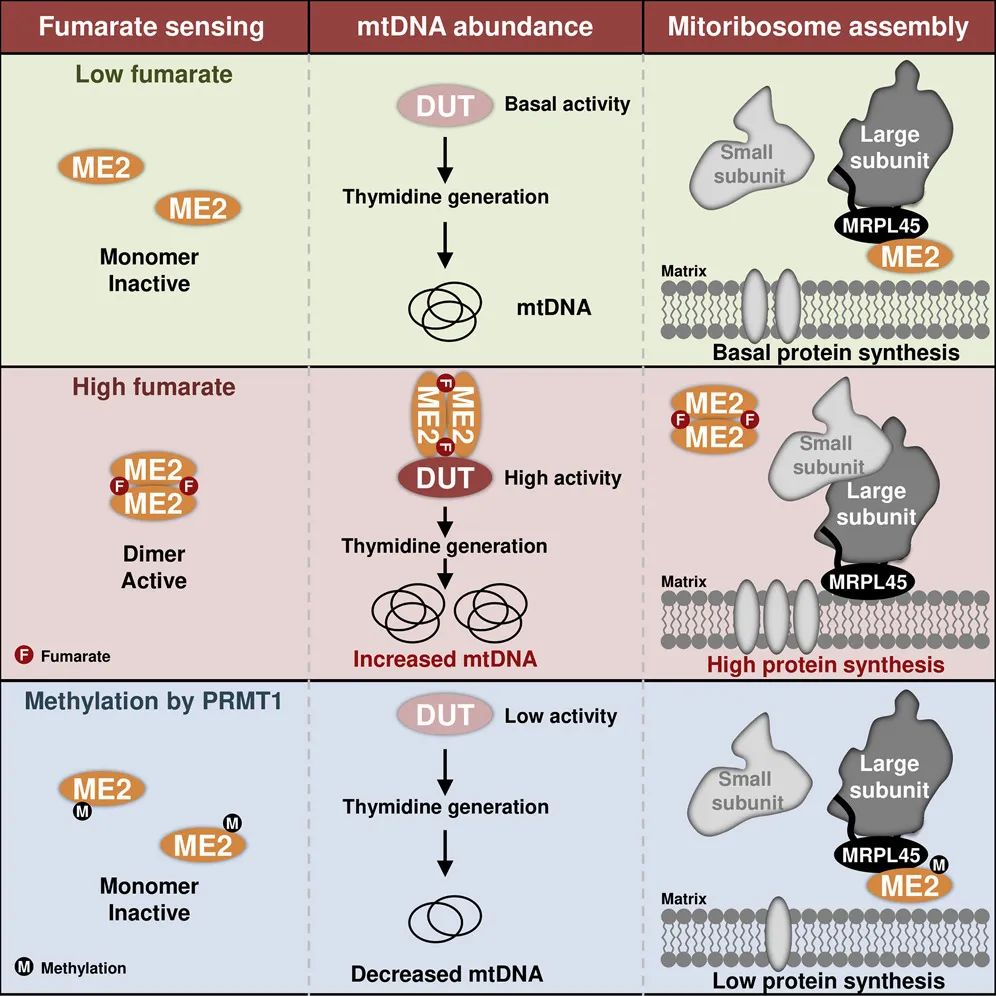
分子机制:延胡索酸促进ME2形成二聚体,ME2二聚体结合并活化线粒体内脱氧尿嘧啶三磷酸核苷水解酶(DUT),促进嘧啶的生成从而上调线粒体DNA(mtDNA)。此外,ME2单体与MRPL45结合,阻碍其结合在线粒体内膜上,从而破坏线粒体核糖体的正确组装和蛋白合成。进一步研究表明,ME2的延胡索酸结合位点受精氨酸甲基化修饰,蛋白精氨酸甲基化酶PRMT1可甲基化ME2,抑制ME2对延胡索酸的识别以及ME2二聚体的合成,最后抑制线粒体生物合成。这些证据充分说明延胡索酸介导的线粒体生物合成在白血病的发生发展中起调控作用。因此,延胡索酸信号转导可能具有成为急性髓系白血病的生物标记物或者治疗靶点。
原文链接:
https://doi.org/10.1016/j.cmet.2021.03.003
3. PRMT6 methylation of RCC1 regulates mitosis, tumorigenicity, and radiation response of glioblastoma stem cells
Molecular Cell (IF 19.328)
Pub Date: 2021-03-18
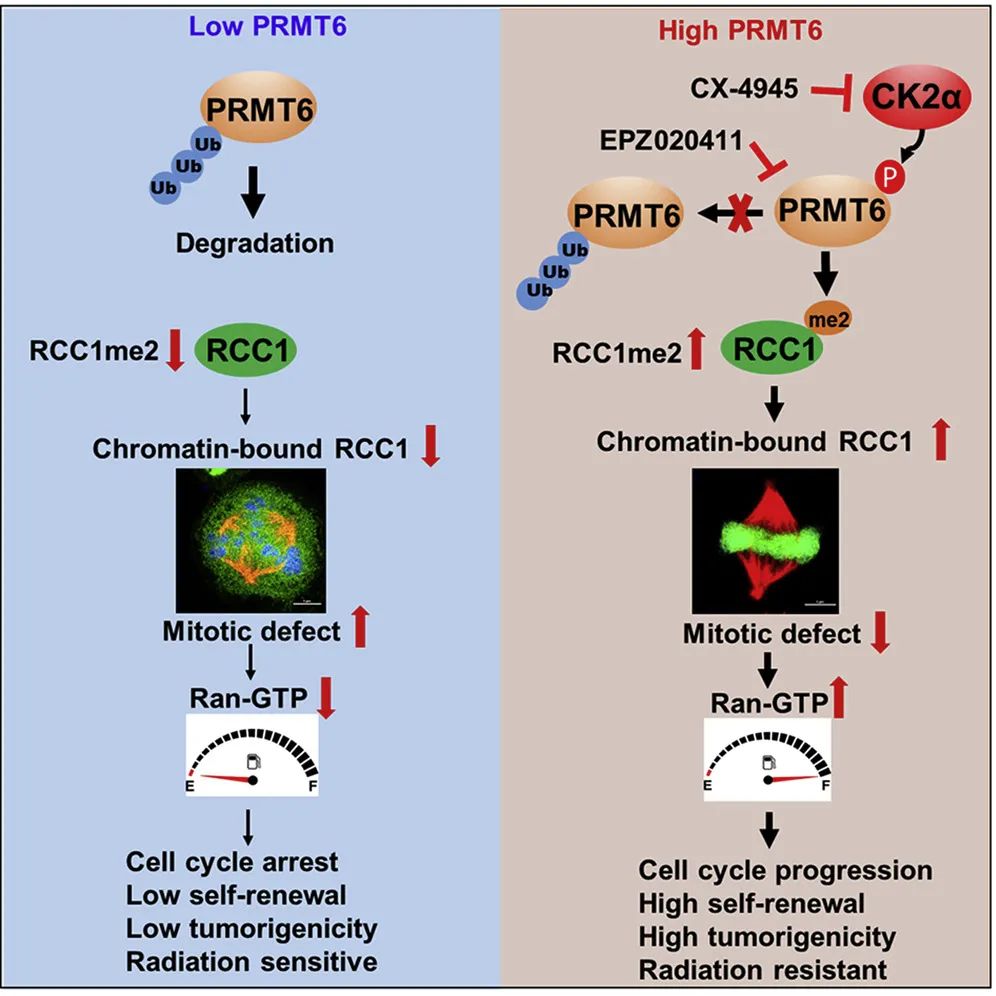
分子机制:PRMT6介导染色体浓缩调节因子(RCC1)的精氨酸甲基化修饰,从而促进RCC1与染色体的结合,并激活Ran GTPase,进而调控核质物质运输和有丝分裂过程。进一步研究发现,磷酸蛋白激酶(CK2α)可以磷酸化PRMT6,促进其发生去泛素化,从而增强其稳定性。上调GSCs中的PRMT6蛋白水平,靶向干预CK2α可以导致PRMT6蛋白发生泛素化降解。这项工作阐述了CK2a-PRMT6-RCC1调控轴在GSCs中的调控作用,并进一步揭示了其作为神经胶质瘤治疗靶点的可能性,为神经胶质瘤的诊疗提供了新的依据。
原文链接:
https://doi.org/10.1016/j.molcel.2021.01.015
4. Arginine Methylation of MDH1 by CARM1 Inhibits Glutamine Metabolism and Suppresses Pancreatic Cancer
Molecular Cell (IF 19.328)
Pub Date: 2016-11-17
分子机制:精氨酸甲基转移酶4 (PRMT4/ CARM1) 通过催化MDH1第248位精氨酸发生甲基化修饰,破坏其形成活性形式的二聚体,进而抑制酶活,干扰谷氨酰胺代谢,最终抑制胰腺癌细胞增殖。另外,KRAS激活型突变KRAS12C通过下调CARM1蛋白水平,抑制MDH1甲基化水平,从而提高其酶活,促进谷氨酰胺代谢和细胞增殖。研究还发现,活性氧ROS能够抑制CARM1活性,上调MDH1甲基化水平,增强其活性,促进谷氨酰胺代谢,从而产生更多还原性物质(如GSH),抵抗氧化应激压力,促进细胞增殖。本研究进一步揭示了胰腺癌细胞中谷氨酰胺代谢机理,为胰腺癌的诊疗提供了更多理论依据。

原文链接:
https://pubmed.ncbi.nlm.nih.gov/2784003/
5. CARM1 Methylates GAPDH to Regulate Glucose Metabolism and Is Suppressed in Liver Cancer
Cell Reports (IF 9.995)
Pub Date: 2018-09-18
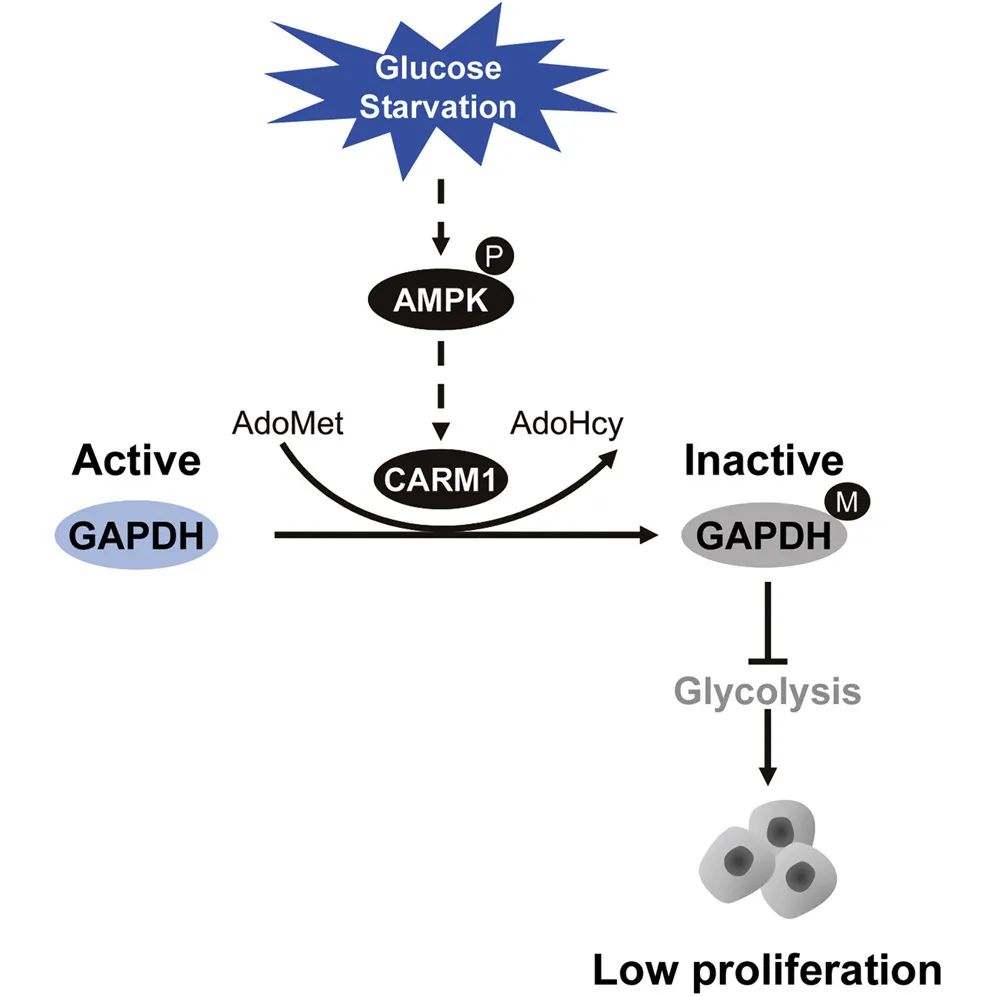
分子机制:精氨酸甲基转移酶1 (PRMT4/ CARM1)催化甘油醛-3-磷酸脱氢酶(GAPDH)发生精氨酸甲基化修饰。作者结合位点特异性抗体和点突变技术,确认234位精氨酸为甲基化位点。进一步发现,该位点的甲基化会降低GAPDH与辅酶NAD+的亲和力,从而抑制其活性,进而干扰糖酵解,抑制肝癌细胞增殖。作者发现葡萄糖缺失会激活AMPK信号通路,进而上调CARM1蛋白水平,促进GAPDH甲基化,抑制其活性和糖酵解。结果表明,CARM1介导的GAPDH甲基化是肝癌葡萄糖代谢的关键调节机制。该研究为肿瘤细胞感受利用葡萄糖的机制研究提供了新的思路。
原文链接:
https://pubmed.ncbi.nlm.nih.gov/30232003/
2022年度国自然医学部国自然40大科研热点的中标数统计如下:
2022热点 | 2022中标数 | 2022热点 | 2022中标数 |
免疫调控 | 907 | 中性粒细胞 | 112 |
巨噬细胞 | 591 | 反馈回路 | 104 |
线粒体 | 491 | 乳酸化 | 104 |
血管功能 | 487 | 可变剪接 | 71 |
外泌体 | 470 | AI机器学习 | 67 |
自噬 | 404 | 类器官 | 67 |
铁死亡 | 337 | 炎症小体 | 62 |
干细胞 | 329 | 染色质重塑 | 58 |
代谢重编程 | 325 | 单细胞测序 | 54 |
m6A/m5C/m7G | 320 | 糖基化 | 50 |
泛素化 | 225 | 低氧缺氧 | 50 |
circRNA | 221 | 相分离 | 50 |
lncRNA | 204 | 泛凋亡PANoptosis | 42 |
细胞焦亡 | 175 | 细胞衰老 | 37 |
组蛋白 | 171 | 胞葬 | 33 |
肠道菌群 | 133 | CRISPR | 33 |
乙酰化 | 125 | 增强子 | 29 |
内质网 | 125 | 精氨酸甲基化 | 25 |
转录调控 | 112 | 迁移体 | 8 |
糖酵解 | 112 | 血管拟态 | 8 |
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。





发表评论
注册或登后即可发表评论
登录注册
全部评论(0)