2023-04-20 来源 : e药界
摘要
2023年第114届美国癌症研究协会年会(AACR)将于4月14日~19日在奥兰多举行。本次大会上,可切除非小细胞肺癌(NSCLC)围术期免疫治疗的相关研究进展引人瞩目。CCMTV小编特此整理如下,以飨读者。
3、3期CheckMate 816研究中国人群数据:新辅助纳武利尤单抗+化疗 vs 新辅助化疗(摘要号CT081);

AEGEAN研究:新辅助度伐利尤单抗+化疗、度伐利尤单抗辅助治疗
未经治的ⅡA~ⅢBN2期可切除NSCLC患者,按1:1随机接受术前度伐利尤单抗(D)1500mg或安慰剂+含铂化疗(Q3W 4周期),后续D 1500mg或安慰剂(Q4W至12周期)。疗效分析时,改良意向治疗人群(mITT)排除具有EGFR/ALK异常的患者。双重主要终点为中央实验室评估的病理完全缓解(pCR),以及盲态独立评审委员会(BICR)评估的无事件生存期(EFS)。
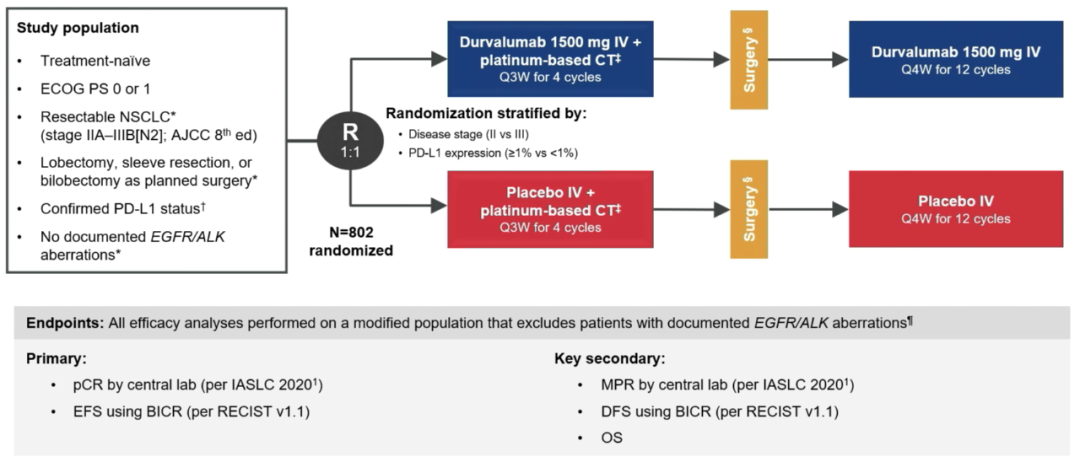 图. AEGEAN研究设计
图. AEGEAN研究设计
截至2022年11月10日,mITT人群中位随访11.7个月,研究达到显著改善EFS和pCR的双重主要终点。EFS成熟度为31.9%,两组的中位EFS为尚未达到 vs 25.9个月(HR=0.68,P=0.003902)。无论应用哪种铂类化疗,D组均可观察到确切且一致的EFS获益。
 图. mITT人群EFS
图. mITT人群EFS
两组的pCR率为17.2% vs 4.3%(P=0.000036),D组的pCR率为单纯化疗组的4倍,绝对值提高13%;主要病理缓解(MPR)率为33.3% vs 12.3%(P=0.000002),绝对值提高21%。
 图. mITT人群pCR和MPR
图. mITT人群pCR和MPR
结论
AEGEAN研究是第一项阐述围手术期免疫治疗+新辅助化疗获益的3期研究,该治疗模式既实现了提高pCR的主要终点,又显著降低了患者疾病进展、复发或死亡的风险,有望成为可切除NSCLC患者新的治疗方案。度伐利尤单抗的加入不影响手术,也不影响4周期新辅助化疗的完成率。未观察到预期之外的治疗相关AE。期待AEGEAN研究后续报道经过更长时间随访更成熟的EFS,以及无病生存期(DFS)、总生存期(OS)等次要终点数据,以了解该疗法对可切除NSCLC患者的全面影响。
2期LCMC3研究:阿替利珠单抗新辅助+选择性辅助治疗
该开放标签、单臂、2期研究,旨在探索可切除的ⅠB~ⅢA期或部分经选择的ⅢB期NSCLC患者应用阿替利珠单抗单药(1200mg IV d1和22)新辅助治疗至多2周期,术后选择性应用阿替利珠单抗辅助治疗(Q3W,至多12个月)的疗效及安全性。主要研究终点为MPR(定义为手术切除标本中存活肿瘤细胞≤10%);次要终点包括根据PD-L1表达进行分层的病理学缓解和根据PD-L1、肿瘤突变负荷(TMB)、新抗原和基因表达谱(GEP)进行分层的影像学缓解;探索性终点为DFS和OS等。

图. LCMC3研究设计
截至2022年10月21日,137例EGFR/ALK阴性并接受手术的患者(主要疗效分析人群,PEP)可进行MPR评估,其中,53例(39%)接受阿替利珠单抗辅助治疗,84例(61%)未接受阿替利珠单抗辅助治疗。接受 vs 未接受阿替利珠单抗辅助治疗的患者的3年DFS率为83% vs 64%(HR=0.43;95%CI:0.21, 0.90;P=0.025),3年OS率为89% vs 77%(HR=0.48;95%CI:0.19, 1.21;P=0.118)。
多因素分析显示,接受阿替利珠单抗辅助治疗的患者与未接受者相比,DFS有更好的趋势(HR=0.52;95%CI:0.22,1.21;P=0.126)。
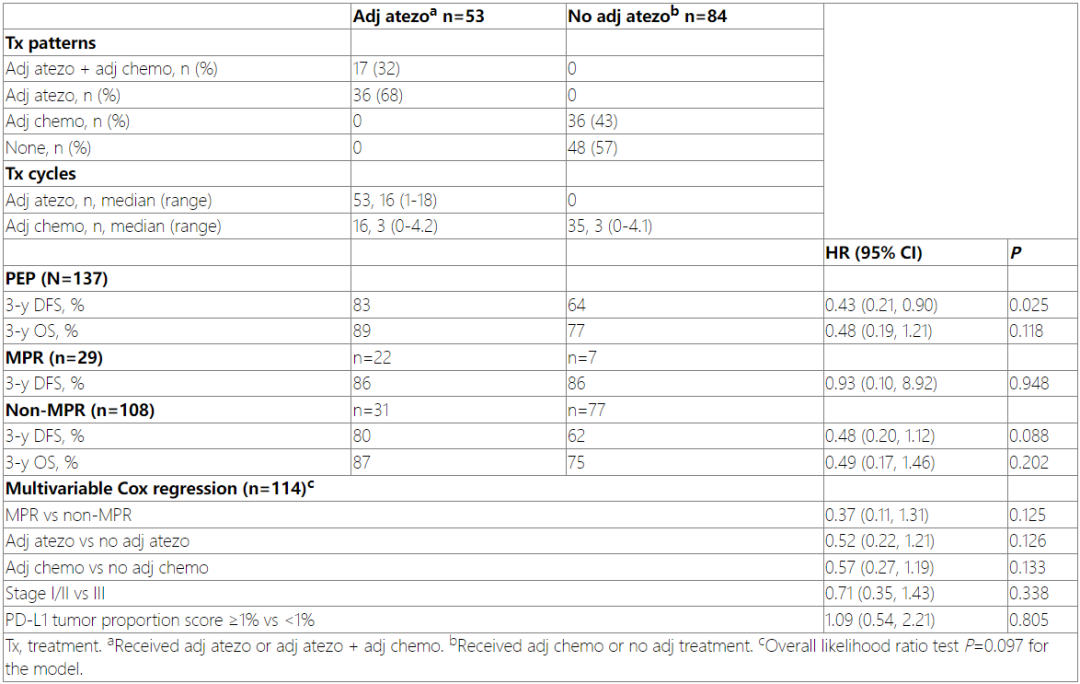
阿替利珠单抗辅助治疗安全性分析人群(n=57)中,阿替利珠单抗辅助治疗后的治疗相关AE发生率为97%(3/4级发生率为40%),因TRAE导致阿替利珠单抗辅助治疗停药的发生率为19%(3/4级发生率为16%)。辅助治疗阶段未见5级TRAE。
结论
LCMC3研究探索性分析显示,接受阿替利珠单抗辅助治疗的可切除ⅠB~ⅢA期或部分经选择的ⅢB期NSCLC患者,与未接受者相比,DFS有所改善,OS也有改善的趋势。此外,非MPR亚组患者中,接受阿替利珠单抗辅助治疗的患者也比未接受者有相同的DFS和OS改善趋势。阿替利珠单抗辅助治疗的耐受性很好,未见新的安全性问题。
CheckMate 816研究中国人群数据:新辅助纳武利尤单抗+化疗
全球、随机、3期CheckMate 816研究显示,新辅助纳武利尤单抗(NIVO)+化疗较单纯化疗,为可切除NSCLC患者带来具有统计学显著性和临床意义的EFS和pCR获益。本次报道中国人群亚组的数据。
 图. CheckMate 816研究设计
图. CheckMate 816研究设计
中国人群亚组共97例患者,NIVO+化疗组44例,单纯化疗组53例。单纯化疗组ⅢA期NSCLC患者比例较高,除此之外,两组患者的基线特征整体均衡。
最少随访38.2个月的数据显示,NIVO+化疗组 vs 单纯化疗组显著改善EFS,中位EFS分别为尚未达到 vs 13.9个月(HR=0.47; 95%CI, 0.25-0.88);pCR率为25.0% vs 1.9%(OR=11.05; 95%CI, 1.41–86.49)。NIVO+化疗组的MPR和至死亡或远处转移时间(TTDM)也更优。

总体而言,NIVO+化疗组和单纯化疗组分别有36例(81.8%)和41例(77.4%)患者接受了手术。NIVO+化疗组分别有18例(41.9%)和5例(13.9%)发生3~4级治疗相关性和手术相关性AE,而化疗组分别为22例(41.5%)和9例(22.0%)
结论
与CheckMate 816研究全球人群的结果一致,新辅助NIVO+化疗 vs 化疗显著改善中国患者的EFS和pCR。在新辅助化疗中加入NIVO可维持治疗的耐受性,并且不影响手术的可行性。这些结果支持新辅助NIVO+化疗作为中国可切除NSCLC患者的治疗选择。
新辅助阿替利珠单抗+化疗的2期研究
该开放标签、多中心、单臂、研究者发起的2期研究在美国3家医院进行。可切除NSCLC患者术前接受至多4周期的阿替利珠单抗、卡铂和白蛋白紫杉醇新辅助治疗。主要终点MPR既往已报道,本次报道成熟的DFS和OS,以及复发性脑转移(BM)患者的临床特征、来自肿瘤基因组学、基因表达和免疫标记物的定量免疫荧光(QIF)测量的综合数据。
STK11和KEAP1突变的患者没有统计学上较差的DFS或OS,尽管他们的BM发生率呈上升趋势。均位于19p染色体上的STK11和KEAP1,可在约1/3的肿瘤中观察到拷贝数减少。
结论
成熟的OS数据显示,新辅助阿替利珠单抗+化疗具有持续的临床获益。影像学和病理学替代终点对OS的预测性有限。有必要进一步研究STK11和KEAP1基因组改变与早期NSCLC关键临床结果之间的关系。
参考文献
1. John V. Heymach, David Harpole, Tetsuya Mitsudomi, et al. AEGEAN: A phase 3 trial of neoadjuvant durvalumab + chemotherapy followed by adjuvant durvalumab in patients with resectable NSCLC. 2023 AACR. Abs CT005.
2. David Paul Carbone, Saiama N. Waqar, Jamie E. Chaft, et al. Efficacy and safety of adjuvant (adj) atezolizumab (atezo) from the Phase 2 LCMC3 study. 2023 AACR. Abs CT215.
3. Changli Wang, Ke-Neng Chen, Qixun Chen, et al. Neoadjuvant nivolumab (NIVO) + chemotherapy (chemo) vs chemo in Chinese patients (pts) with resectable NSCLC in CheckMate 816. 2023 AACR. Abs CT081.
4. Brian S. Henick, Justin F. Gainor, Mark M. Awad, et al. 3-year update of neoadjuvant atezolizumab + chemotherapy in patients with resectable non-small cell lung cancer. 2023 AACR. Abs CT217.
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。





发表评论
注册或登后即可发表评论
登录注册
全部评论(0)