
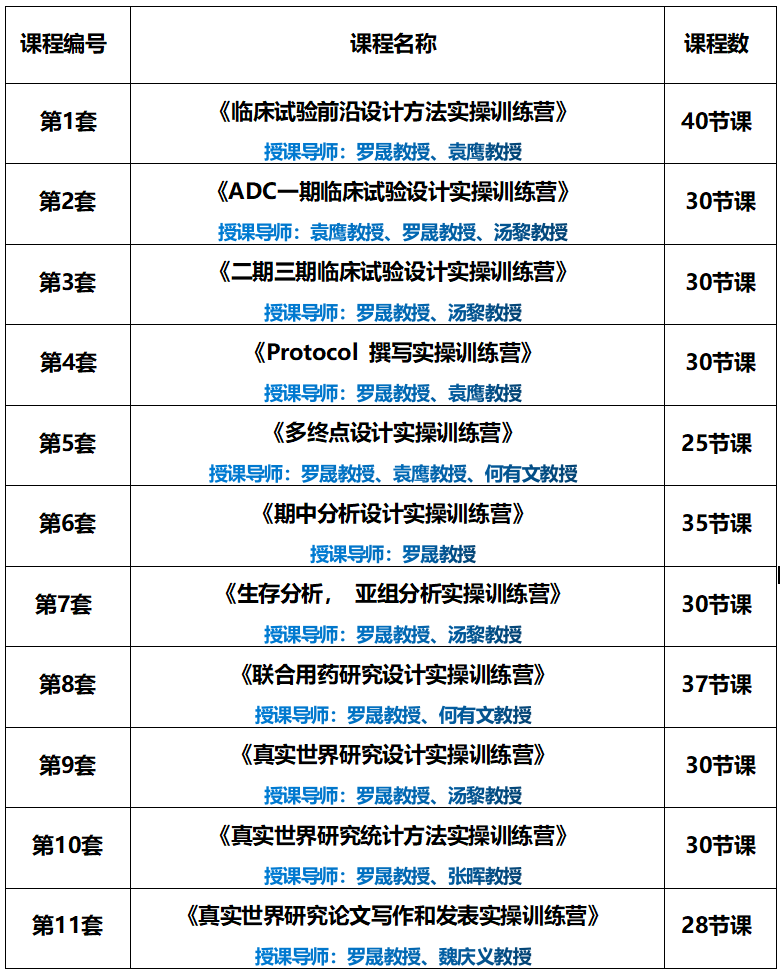
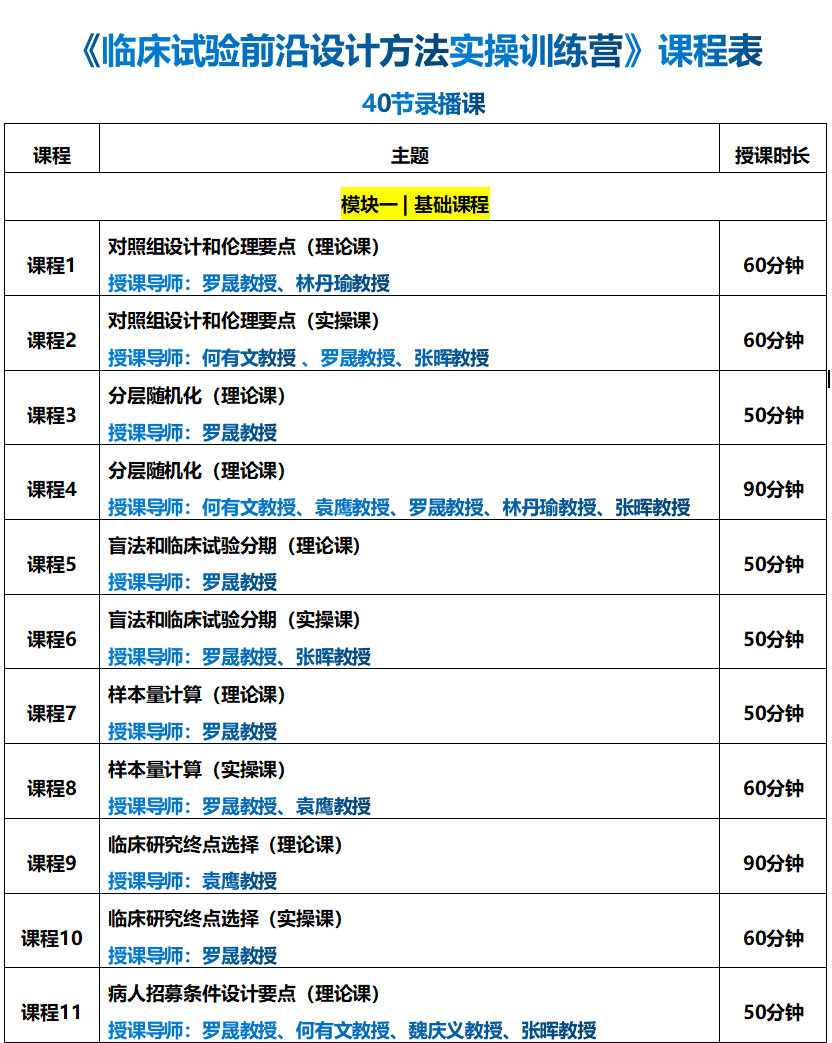
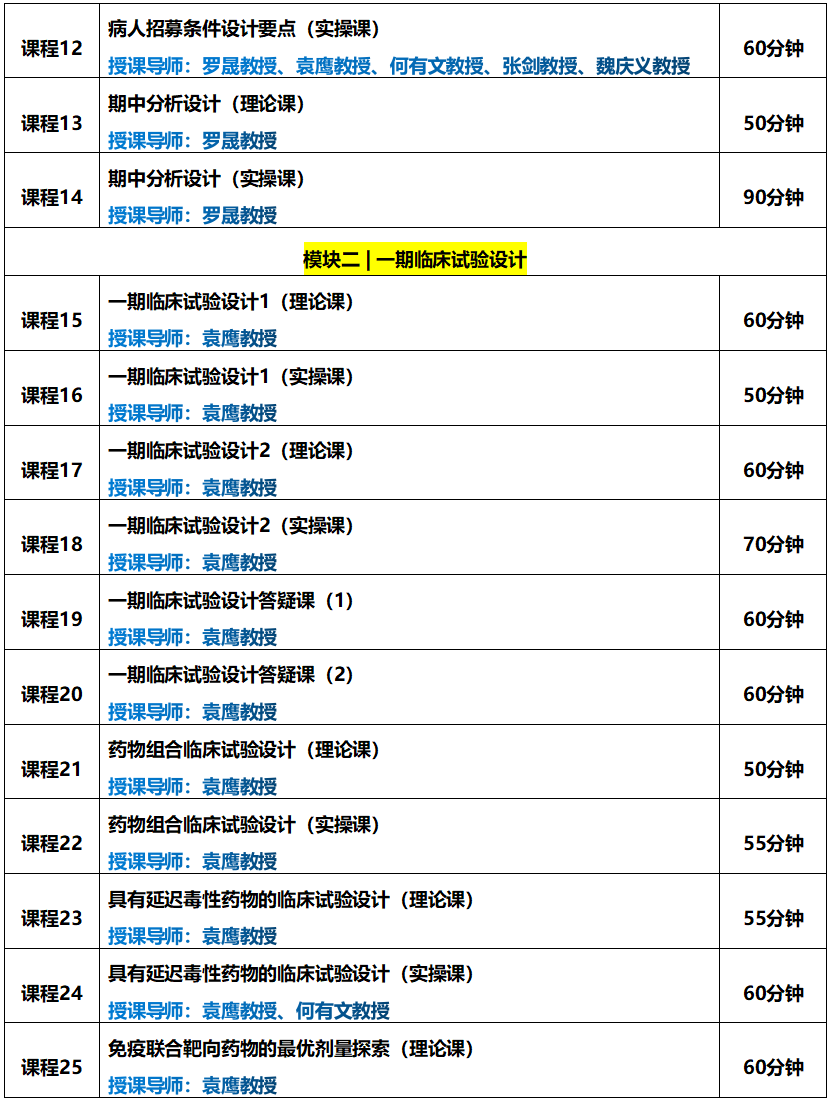
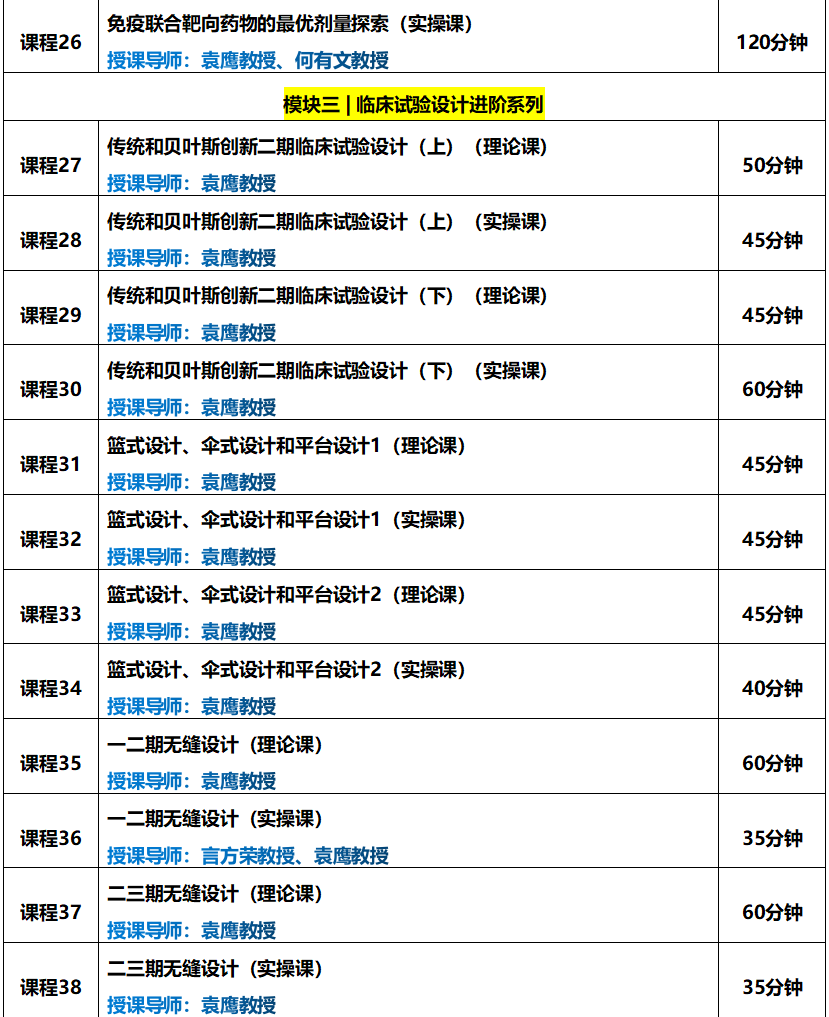
本期,我们聚焦《临床试验前沿设计实操训练营》模块三的最后一课:《自适应临床试验设计》。 2021年1月国家药品监督管理局药品审评中心官网发布《药物临床试验适应性设计指导原则(试行)》,自发布之日2021年1月29日起实施。此指南为规范和统一国内对适应性设计的认识,促进适应性设计的应用和理解以提高研发效率,该指导原则的正式实施将助力国内新药质量的进一步提升,《自适应性临床试验设计》的课程,继续由大家非常熟悉的美国安德森癌症中心的袁鹰教授讲解。《孙子兵法》曰:兵无常势,水无常形,想要克敌制胜,就要学会随机应变;同样,药物的研发往往九死一生,失败才是常态。在临床试验过程中,如何根据数据进行自适应的调整,尽可能的打赢这一仗?《自适应临床试验设计》这一课,你必须好好补一补。
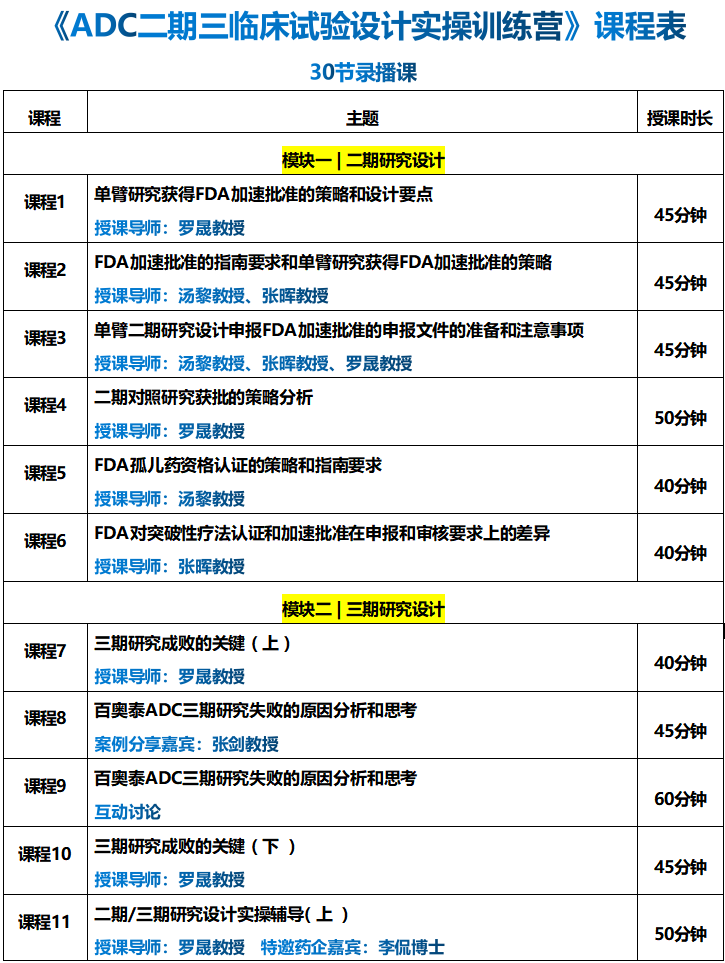
2021年1月国家药品监督管理局药品审评中心官网发布《药物临床试验适应性设计指导原则(试行)》,自发布之日2021年1月29日起实施。此指南为规范和统一国内对适应性设计的认识,促进适应性设计的应用和理解以提高研发效率,该指导原则的正式实施将助力国内新药质量的进一步提升,《自适应性临床试验设计》的课程,继续由大家非常熟悉的美国安德森癌症中心的袁鹰教授讲解。《孙子兵法》曰:兵无常势,水无常形,想要克敌制胜,就要学会随机应变;同样,药物的研发往往九死一生,失败才是常态。在临床试验过程中,如何根据数据进行自适应的调整,尽可能的打赢这一仗?《自适应临床试验设计》这一课,你必须好好补一补。1. 自适应临床试验设计的定义
2. 如何根据试验前的数据进行相关预测
3. 根据外界的数据对现有的方案进行调整
4. Keynote-355研究获批背后的原因分析
5. II/III期无缝设计的期中分析设计策略
6. 自适应设计有什么优点
7. 临床试验样本量的重新计算
8. 不同的自适应方法的选择及应用
9. 自适应性设计的局限性
10.自适应设计若干统计学思考
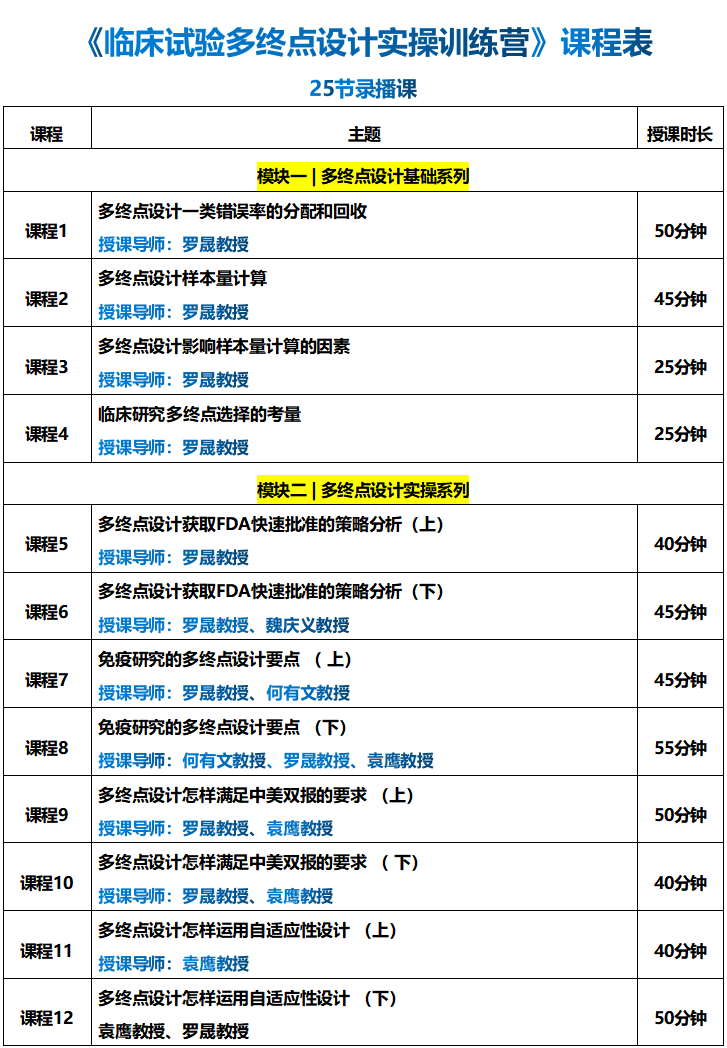
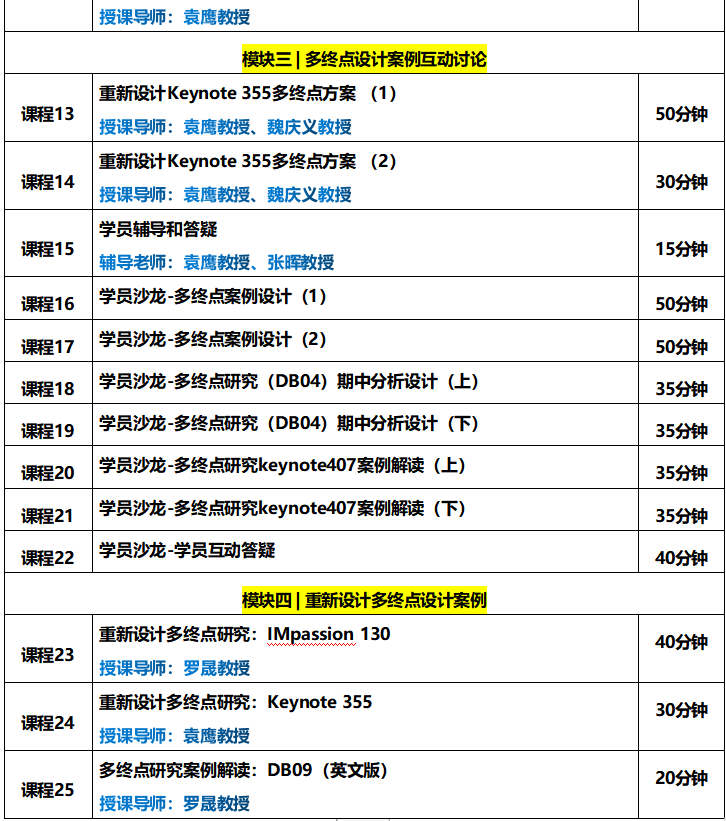
2. Group sequential design的应用和注意事项3. 重新计算样本量的注意事项及2种常用方法的介绍:(1) Combine test statistics or p-values;(2) Promising zone based on conditional power4. Adaptive enrichment的基本思想,应用场景和注意事项5. Adaptive treatment arm selection概述
6. Adaptive randomization概述7. Adaptive endpoint selection概述8. Trial integrity的基本思想,应用场景和注意事项介绍
9. 自适应临床试验设计未来的发展趋势
为提高我国糖尿病医生科研水平与科研能力,促进医学研究成果转化,提高医生科研综合水平,北京康盟慈善基金会发起并设立了“医学与健康事业研究发展基金项目”,以“科研浩海,盟动助力”为主题,科研技能培训系列课程由医微客(北京)提供技术支持,于2021年5月正式启动。
科研资讯(站内):
百度浏览
来源 : 国际临研
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。























发表评论
注册或登后即可发表评论
登录注册
全部评论(0)