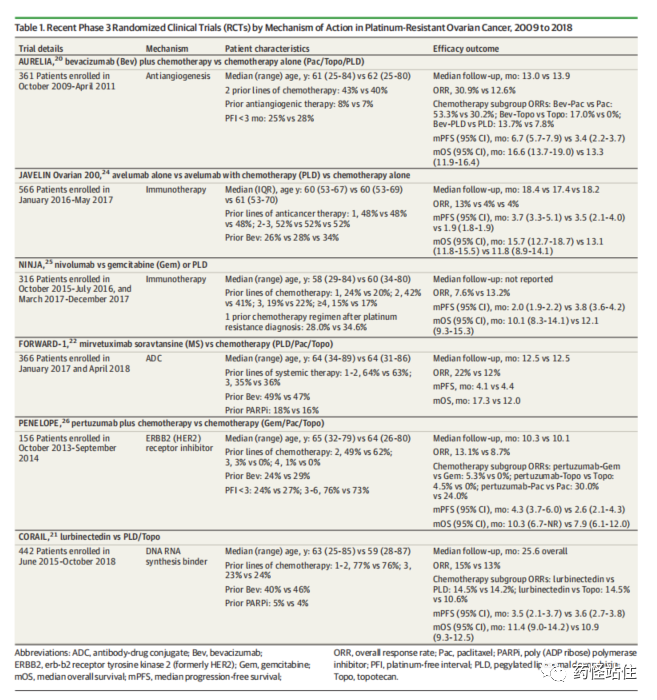
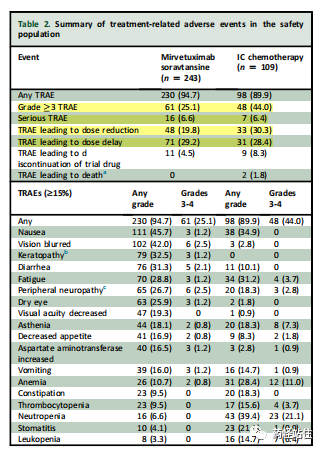
卵巢癌是全球第三常见、致死率排名第一的妇科肿瘤,2020年,全球新发32万患者,死亡21万。其中上皮性卵巢癌是最常见的卵巢癌亚型,可分为高级别浆液性卵巢癌 (HGSOC)、子宫内膜样癌、透明细胞癌、粘液性癌和低级别浆液性癌,其中HGSOC最常见,与70%-80%卵巢癌死因相关,平均5年生存率低于50%,中位总生存期 (OS) 为40.7个月。过去的三十年间,HGSOC治疗手段有限,自1990s,“铂类+紫杉类”一直作为一线治疗的backbone。然而随着PARPi和抗血管生成药物III期成功,强势跻身权威指南维持治疗优先推荐。在美国和欧洲,铂敏感卵巢癌使用“维持治疗”的比例正逐年上升,尤其是PARPi代表的维持治疗新时代,显著延长PFI(无铂间期)。研究显示,卵巢癌一线治疗的缓解率为75%-80%。然而70%的肿瘤会复发,并最终进展为铂耐药卵巢癌,通常定义为末次铂类给药后6个月内疾病复发;进一步讲,约20%的患者对一线铂类药物治疗无应答,被称为原发性铂类药物难治(铂难治),定义为末次铂类给药后1个月内疾病进展。不幸的是,至今我们仍用PFI来区隔铂耐药、铂难治和铂敏感,和SCLC、头颈鳞癌有相似之处,至今仍缺少验证的、形成共识的、可预测铂类药物耐药性的生物标志物,有证据显示部分疾病特征可能与铂耐药及PFI相关,包括HRR高功能评分、缺乏BRCA1/2变异性、CA-125高清除率、CCEN1基因扩增、高水平的循环CTC、较少的TIL等。虽然已提出几种铂耐药机制,包括药物外排改变、细胞内蛋白隔离铂类药物、铂类药物诱导的 DNA 损伤修复以及生存蛋白表达改变,然而,具体机制尚不明确,铂类药物耐药是晚期卵巢癌死亡的主要原因。目前PROC(铂耐药卵巢癌)的标准治疗是单药非铂类化疗药或临床研究,通常非铂类化疗的客观缓解率ORR< 12%、中位无进展生存期mPFS < 4个月和mOS < 12个月,疗效不容乐观,还会引起显著的不良反应,如中性粒细胞减少症、脱发、神经病变和掌跖红肿疼痛,严重损害患者生活质量。抗血管生成药物-贝伐珠单抗于2014年在美国和欧洲获批用于治疗PROC,这是第一种获批用于PROC的非细胞毒药物,关键注册研究AURELIA 评估了在单药化疗的基础上加上贝伐珠单抗用于PROC的疗效和安全性。值得注意的是,AURELIA排除了经>2线系统治疗的受试者,同时试验中的大多数患者 (58%) 既往接受过1线治疗,且既往用过抗血管治疗的比例低于10%,比较符合当时的临床实践,换到现在,可能就不一定成功了,现在的PROC大部分都是经PARPi治疗,更后线,更难治。结果显示,相比化疗,“贝伐珠单抗+化疗”可以显著改善ORR(30.9% vs 12.6%),显著改善主要终点mPFS至6.7m(vs 3.4m),遗憾没能在OS终点上取得统计学获益,可能与对照组后线高比例使用贝伐珠单抗有关,进一步分析显示,相比未使用贝伐珠单抗的患者,使用贝伐珠单抗可降低32%-40%的死亡风险。尽管取得耀眼成就,贝伐珠单抗也带来了很多治疗相关不良反应,包括高血压、蛋白尿、出血、血栓形成和肠穿孔,成为部分患者的禁忌症。9%-11%的复发性卵巢癌患者可发生贝伐珠单抗诱导的肠穿孔。进一步讲,由于贝伐珠单抗被推荐用于铂类药物敏感性卵巢癌的一线诱导和维持治疗,换句话说,多数患者在PROC前已经接受过贝伐珠单抗,可能疗效会有减弱,但也是一种选择,目前抗血管治疗可以在OC里跨线。基于良好的ORR数据(33%-41%),多款PARPi加速获批用于治疗PROC,主要用于携带 BRCA 突变和/或同源重组缺陷的患者。然而SOLO3事后分析显示,相比化疗,奥拉帕利竟然折损OS获益(经≥3线mOS折损近10个月),同样地,另一种PARPi尼拉帕利也显示出同样结论,不同PARPi都显示出损害PROC OS获益,促进三款PARPi(奥拉帕利、尼拉帕利、rucaparib)在>经2线OC治疗适应症的撤回,所以OC里,目前PARPi都地位仅限于“维持”。Elahere(Mirvetuximab soravtansine)是由ImmunoGen 开发的一款FRαADC,由一个binding叶酸受体的抗体+可裂解连接子+高效微观抑制剂DM4构成,是全球第一款该靶点上市的药物,单药用于治疗FRa高表达的铂耐药卵巢癌(PROC)。其它在研适应症包络:子宫内膜癌(含中国多国III期),输卵管癌(含中国多国III期),腹膜癌(含中国多国III期)。从2012.05.30进入临床I期至2022.11.14首次全球获批(FDA)虽历经十年起伏,终修成正果,随着MIRASOL III期验证成功,Elahere成为首个也是目前唯一一个在FRa高表达PROC种同时取得OS、PFS和ORR获益的药物,有理由相信它将成为这类患者治疗新标准,有望改写指南,同时拉开卵巢癌(OC)生物标志物指导下的治疗序幕。Elahere的成功非常值得学习,体现了一种进步,临床研究的进步,坚持的力量。在MIRASOL前,Elahere先经历了III期FORWARD-1 的失败。FORWARD-1是一项随机、开放标签III期,探索相比研究选择的化疗,Elahere(MIRV)用于铂耐药上皮性卵巢癌的疗效和安全性。研究纳入既往经1-3线系统治疗且FRα阳性的受试者,按照2:1随机分配至Elahere(6 mpk)或对照组,主要终点为BICR评估的FRα高表达和ITT人群的PFS。研究共纳入366例铂耐药OC受试者,试验组和对照组分别纳入243例和109例受试者。既往至少经过一线系统治疗,FRα阳性是使用anti-FOLR1 2.1抗体经过Ventana Medical system评估的(在<10×视野下,FRα膜染色≥50%,其中高中表达分别定义为膜染色≥75%、50-74%),所有受试者入组前都要求提供肿瘤组织(新鲜或留存)用于用于检测FRα。所有接受Elahere治疗前都基于三联用药预防输液反应,同时给药后d1-d4使用糖皮质激素滴眼液(每日六次),d5-d8(每日四次),可使用无防腐剂的人工泪液。对照组化疗在随机化前已经选择好治疗方案紫杉醇、PLD或topotecan。在发生92个PFS事件时,IDMC会进行无效,如果ITT和阳性人群HR都<1则试验继续进行;发生244个PFS事件时,会进行最终分析。使用 The Hochberg procedure控制I类错误(如果两个终点p都<0.05,则拒绝全部零假设,否则,如较小的p<0.025则拒绝相应的零假设)。做第一个吃螃蟹的人,就比较惨,换到现在,确认高表达获益确实高而且与中表达(研究定义的)获益相反,那做fix-sequence test更好,把所有的把握度先给到高表达人群,直接在0.05水平上检验FRα高表达人群PFS获益。(马后炮,失败后信心满满继续重开III期值得信赖)。基线特征:既往经PARPi治疗比例不足20%,既往贝伐珠单抗治疗比例近50%,FRα高表达比例占比近60%遗憾的是,无论是FRα高表达还是ITT人群都没能实现PFS统计学显著性,注意这里是统计学获益,HR分别为0.98(p=0.897)和0.69(p=0.049);进一步分析显示,在FRα高表达人群中,相比对照组,Elahere在ORR(24% vs 10%)、CA-125响应率(53% vs 25%)、PRO结局(27% vs 13%)都有更好的改善。同时,相比化疗,Elahere≥3级TRAE发生率(25.1% vs 44%)、减量比例(19.8% vs 30.3%)、停药率更低(4.5% vs 8.3%)。
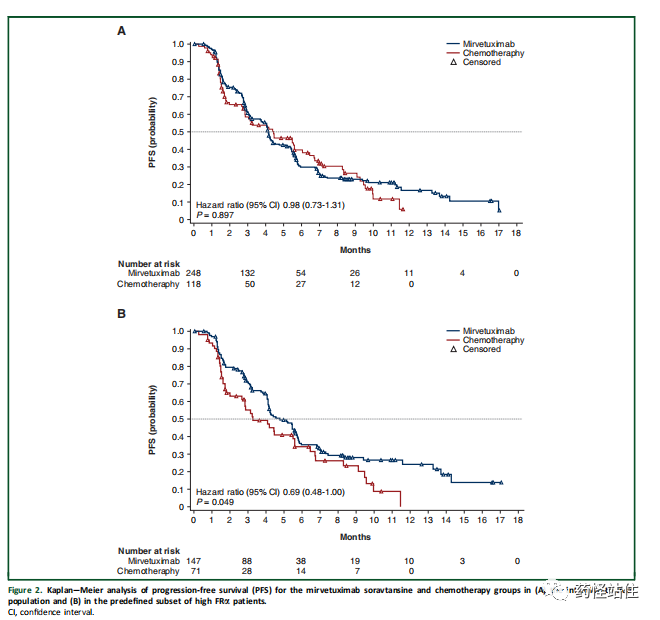
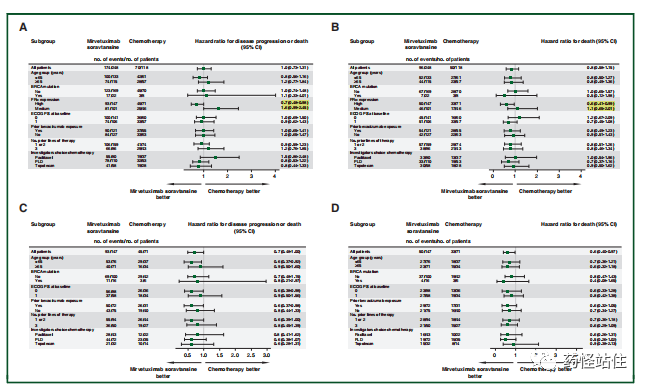
ITT人群PFS交叉在一起,但尾部试验组挑上来了;高表达人群试验组始终hold住了,在对照组上方。HR分别为0.98和0.69。对比这两个图,无论是对照组还是试验组,相比于FRα中表达,高表达的mPFS都更低,说明FRα可能是预后因素。ABCD图分别为ITT人群PFS和OS,FRα高表达人群PFS和OS。惊奇的发现,ITT人群中FRα中表达和高表达PFS获益是相反的(95% CI完全不重合),点估计分列chemo better侧及MIRV侧,OS获益点估计获益也是如此(一致趋势,高表达人群值得)。同时我们可以发现在这个研究里,几乎在全部亚组里,OS获益HR都是<PFS获益HR,这就是安全性好带来的力量(相对的,主要是相对于对照组),还记得我们经常说一般PFS获益会高于OS,PFS在0.7左右,OS一般会损失0.1-0.2,这里直接相反。如果说ITT人群代表的AB图亚组分析点估计左右随机分布,那么FRα高表达代表的CD图可以清楚看到所有点估计都落在左侧(MIRV更好)。预设亚组,统计学效力较高,但由于power不够,所以遗憾没能达到统计学上的显著性。ABCD图分别为ITT人群和FRα高表达人群首次数据截至时间及最终OS分析。首次分析的OS,无论是ITT人群还是高表达人群(AC),MRVI都在对照组上方,HR分别为0.82和0.62,分别高于PFS的0.98和0.69,这个研究充分说明了安全性对于OS的影响,直接可能逆转PFS获益结论,至少比PFS更强。全部分析数据后,发现FORWARD I FRα检测手段可能不合适,稀释了疗效,呼吁检测标准化。同时,基于FORWARD的失败,指导公司设计接下来两个注册研究,探索MIRV用于铂耐药、FRα高表达(PS2+评分)的单臂研究SORAYA(支持加速审批),和随机对照III期MIRASOL(确证试验),进一步讲,相比于FORWARD I的2:1,MIRASOL按照随机1:1,这是一种更保守和高效的统计学设计。可以看到在SORAYA开始时候,贝伐珠单抗已经成为前线治疗的标准,100%受试者都经贝伐珠单抗治疗(FORWARD I年代这个比例只有一半),近50%的人都经PARPi治疗(FORWARD I不足20%),可以说这是更难治的一群人,即便如此MIRV ORR也能达到31.7%(远高于历史对照),mDoR为6.9m,是一份很出色的成绩了。By the way,以奥拉帕利为例,在OC里的适应症都为铂敏感人群,针对初治的铂敏感人群限定了BRCA状态,对于复发铂敏感并无限定BRCA。这也好理解,其实本身对于铂敏感的OC来说,本身就是一种人群选择,对DNA损伤化疗敏感的一群人,理论上对作用于DDR通路药物敏感,换句话说,DDR通路抑制剂可以增效铂类DNA损伤作用、抗肿瘤作用。也就难怪,PARP会i折戟PROC人群,但这也与安全性不好有关。还没有这个试验的详细数据。我们来看看公司5.3号给出的新闻稿。无论是ORR、PFS还是OS,MIRV都完胜IC。公司计划2023下半年提交欧盟MAA和美国sBLA。截至2023.05.23,Informa数据库显示共有15项临床研究状态处于on-going或planed,其中有两项III期指的注意,一项是在贝伐珠单抗的基础上做联合探索铂敏感人群维持治疗、另一项是中国的单臂桥接试验(和华东医药合作的)。多项II期联合铂类探索铂敏感人群疗效,以及联合PD-1单抗用于MSS 复发EC疗效等。在向前线推进。
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。











发表评论
注册或登后即可发表评论
登录注册
全部评论(0)