7月3日,AZ与Daiichi Sankyo联合宣布了合作开发的TROP2 ADC药物Dato-Dxd(DS-1062)在肺癌的首个三期临床结果,其中喜忧参半,因而AZ股价开盘大跌了8%以上(市值损失超过160亿、比买这个产品花的钱都多)。
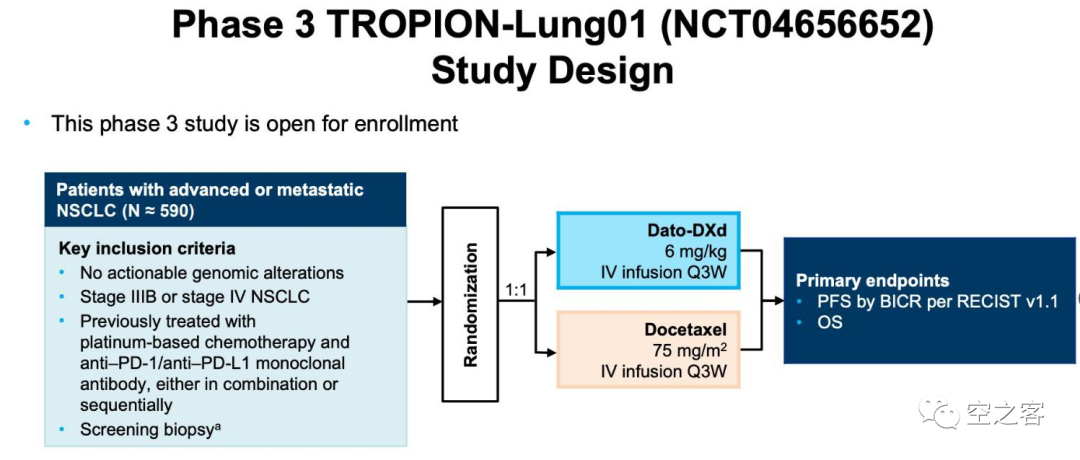
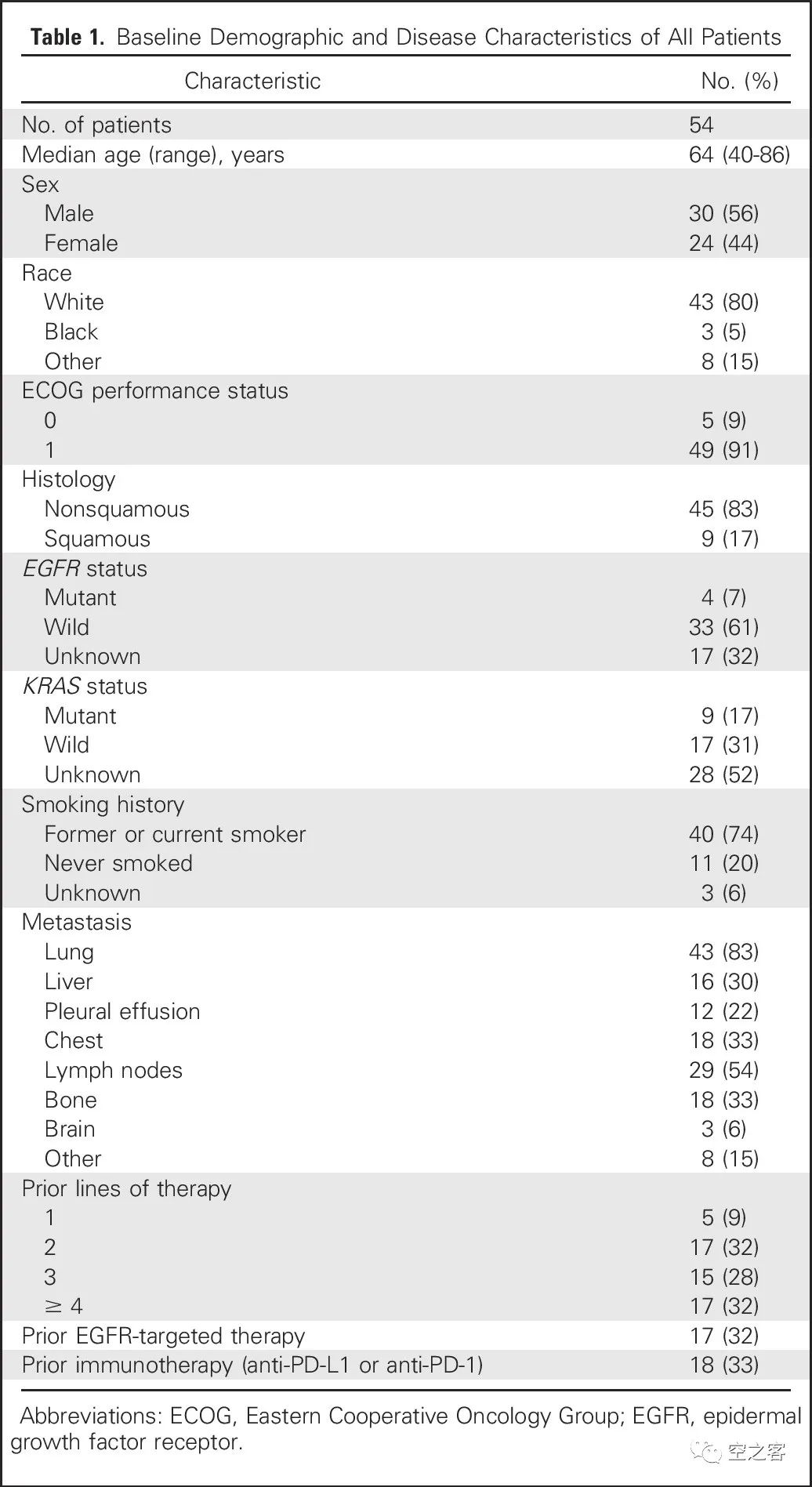
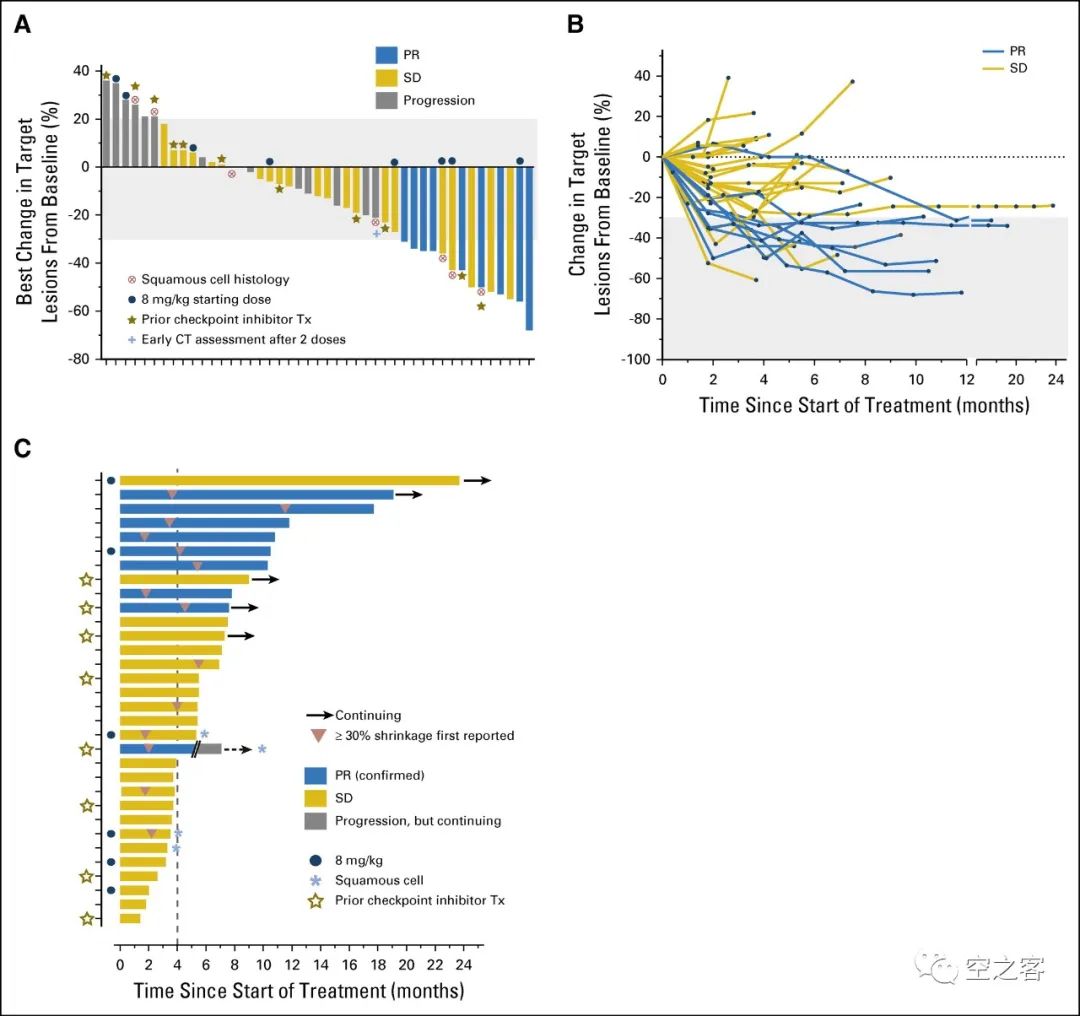
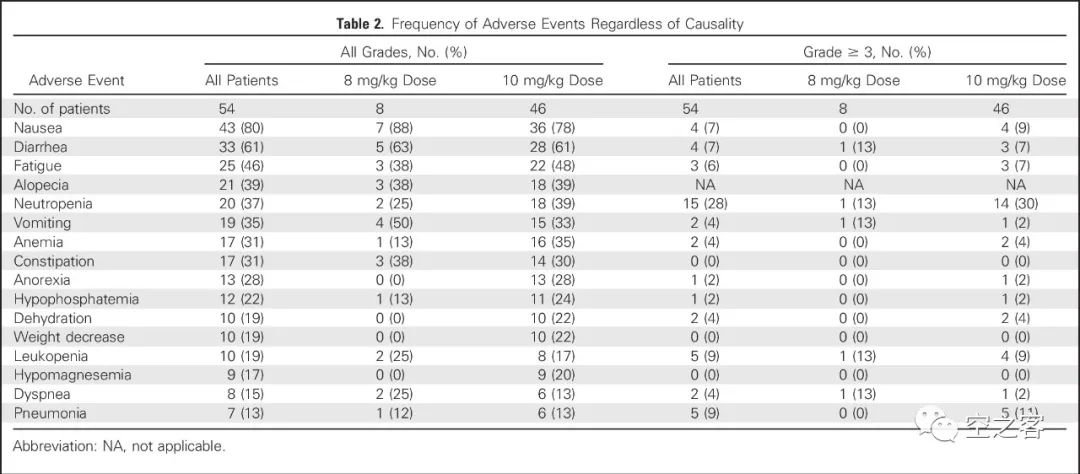
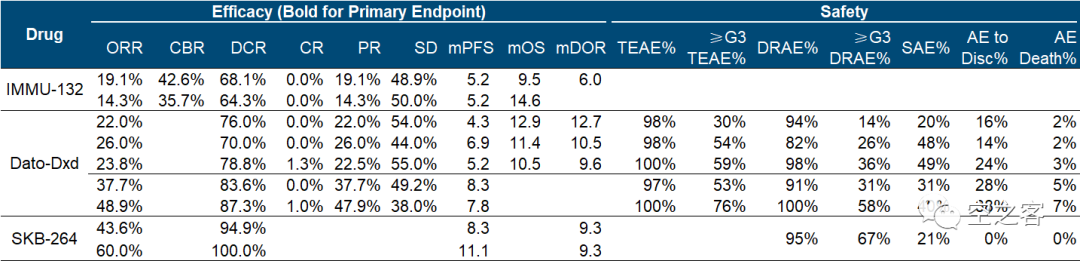
https://www.astrazeneca.com/media-centre/press-releases/2023/datopotamab-deruxtecan-met-dual-primary-endpoint-of-progression-free-survival-in-patients-with-advanced-non-small-cell-lung-cancer.html在代号为TROPION-Lung01的全球多中心随机开放三期临床试验中(NCT04656652),约入组了600例接受过至少一线治疗的NSCLC患者,6mpk剂量的Dato-Dxd对比75mg/㎡剂量的多西他赛。在两个主要临床终点中的PFS上有显著改善,而另一个临床终点OS的结果尚未能达到预设统计学显著性、将维持盲态继续随访;并且比较要命的问题是,不仅ILD又被提及,而且明确有因不良反应而死亡的病例。作为已经被全球药企追寻的热门靶点,TROP2显然不能仅满足于屈居三阴性乳腺癌、甚至是乳腺癌这一隅,能否成功向肺癌这第一大癌种进军,决定了是否能扛得起在HER2之后的ADC领域第二杆大旗。然而近来TROP2 ADC在NSCLC适应症的临床结果,包括上周DS这一更新,还是有些让人心里打鼓。Trodelvy作为TROP2 ADC的带头大哥,在NSCLC上也较早开始了探索,早在2017年ASCO上就公布了单药治疗2L NSCLC结果。在代号为IMMU-132-01(NCT01631552)的临床1/2期试验中,共入组了54例经治NSCLC患者(中位数接受过3线的治疗),其中各有1/3接受过EGFR靶向药或免疫治疗。https://ascopubs.org/doi/10.1200/JCO.2016.72.1894在21天给药周期的第1和第8天给药8或10mpk后,ITT所有患者中的ORR为19%(9例PR)、mDOR为6.0个月、mPFS为5.2个月、mOS为9.5个月,而经过免疫治疗患者中的ORR为14%(2例PR)、mPFS为5.2个月、mOS为14.6个月。安全性方面也延续着Trodelvy此前的表现,血液毒性仍无法避免,最典型的是10mpk剂量组出现了30%的3级以上中性白细胞减少。或许是早期的这些临床数据并不十分令人鼓舞,Gilead收购后对Trodelvy在NSCLC上的拓展热情似乎不高,单药治疗2L+ NSCLC的三期注册性临床(NCT05089734)直到2021年启动,拟入组520例患者,与多西他赛进行对照,预计2024年才会有数据读出。2. Daiichi Sankyo/Astra Zeneca:Dato-Dxd
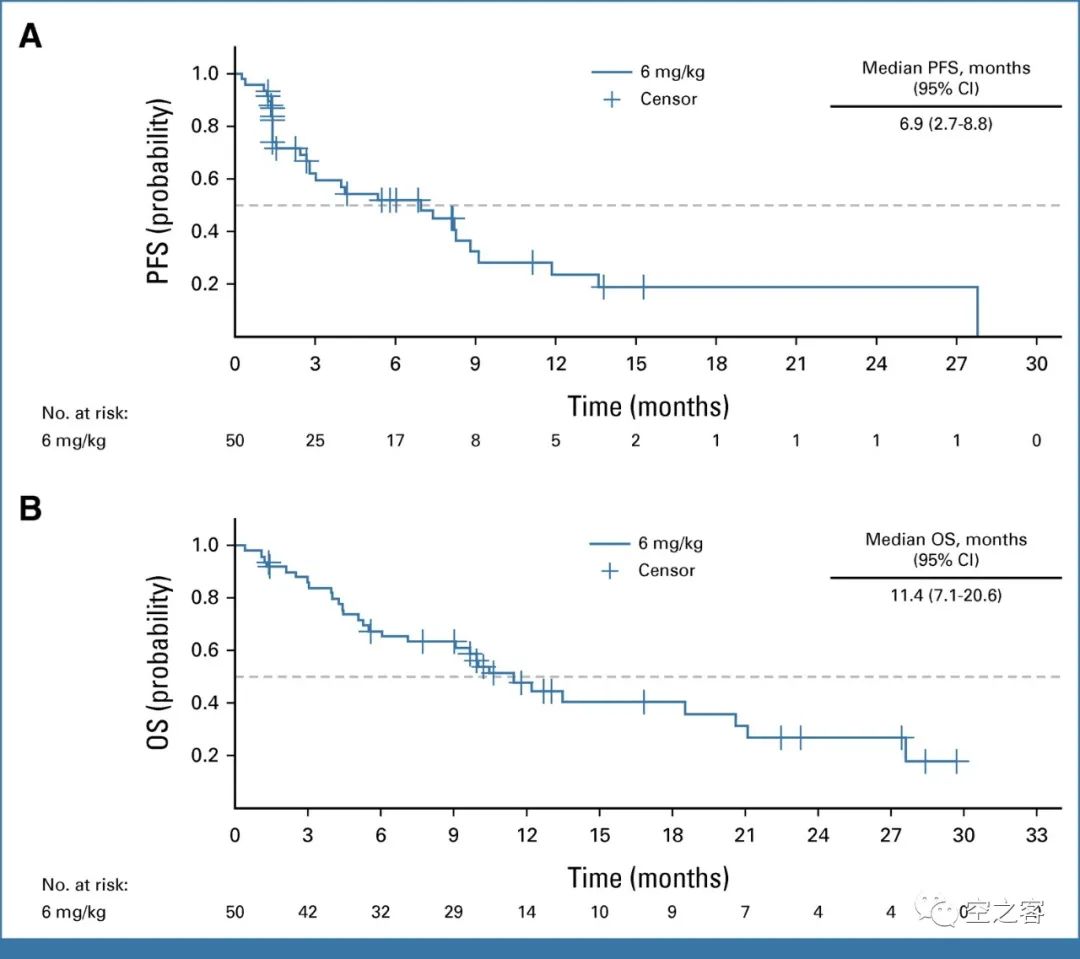
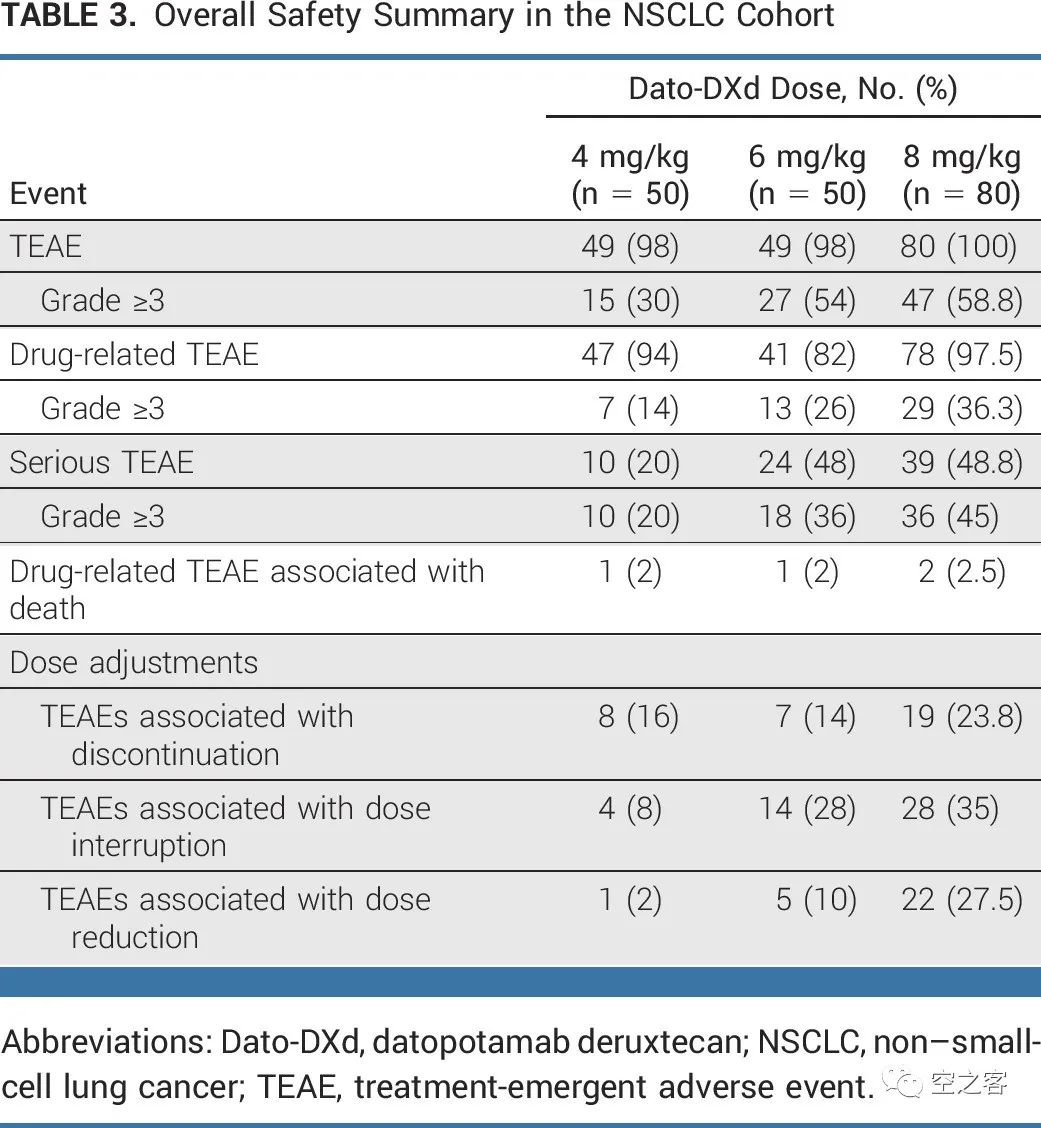
在此次公布三期临床结果之前,Dato-Dxd单药在NSCLC适应症最重要的支撑就来自于今年ASCO上公布的结果。在代号为TROPION-PanTumor01的一期临床的扩展试验中(NCT03401385),共入组了180例NSCLC患者,50%以上接受过3线以上治疗、20%以上接受过5线以上治疗,其中包括80%左右的免疫治疗和接近100%的铂类化疗。https://ascopubs.org/doi/10.1200/JCO.23.00059在每三周一次给药后,4mpk剂量组的ORR为22%(11例PR)、mDOR为12.7个月、mPFS为4.3个月、mOS为12.9个月,6mpk剂量组的ORR为26%(13例PR)、mDOR为10.5个月、mPFS为6.9个月、mOS为11.4个月,8mpk剂量组的ORR为24%(1例CR+18例PR)、mDOR为9.6个月、mPFS为5.2个月、mOS为10.5个月。8mpk更高剂量组的有效性明显倒挂,也是比较蹊跷的一件事。安全性方面,就为后面三期临床埋下了伏笔,不仅总的药物相关不良反应偏高(三级以上药物相关AE在14%/26%/36%),而且ILD在三个剂量组都出现了,三级以上ILD的发生率为6%/8%/8%。除了Dato-Dxd单药治疗2L+ NSCLC以外,DS和AZ还在同步推进联用K药以及卡铂等治疗1L NSCLC的三期临床。
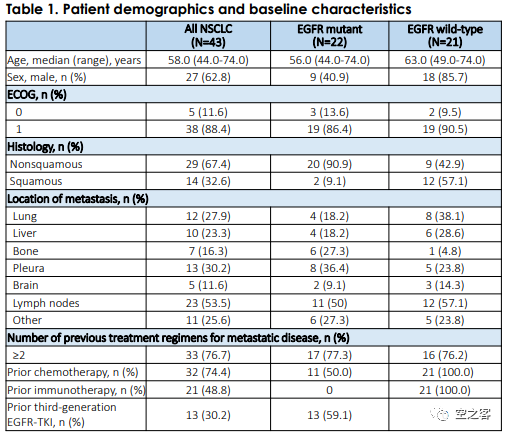
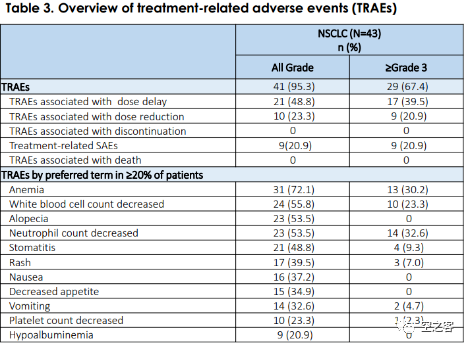
https://www.astrazeneca.com/content/dam/az/Investor_Relations/events/ASCO-IR-deck-June-2023.pdf科伦与MSD合作开发的SKB-264也紧随其后进入了三期临床,而同样在2023年ASCO上公布了早期结果。在1/2期临床中(NCT04152499),共入组了43例NSCLC患者,其中76%接受过2线以上治疗,包括74%的化疗、49%的免疫治疗和30%的三代EGFR TKI。
https://meetings.asco.org/abstracts-presentations/218898在39例可评估疗效的患者中,ORR为43.6%、mDOR为9.3个月、mOS尚未达到(中位随访时间11.5个月);在20例EGFR突变患者中,ORR为60%、mDOR为9.3个月、mPFS为11.1个月。
安全性还是集中在血液毒性上,三级以上的药物相关不良反应居然高达67%,包括30%以上的三季贫血、中性粒细胞减少等,好在是规避了ILD或眼毒性、神经毒性等,最终能把因不良反应而停药或死亡的人数全都摁在0上实属不易。这三个已经进入三期临床的TROP2 ADC品种,面前都横亘着2L+ NSCLC的标准疗法多西他赛这投拦路虎,在历次试验中多西他赛针对2L NSCLC患者的PFS大约在4.5个月、OS大约在10个月以上。
1)Trodelvy并没有展现出mPFS上比多西他赛的显著优势,而在免疫治疗经治患者里面mOS优势比较明显,这可能是它在三期为什么直接赌mOS单终点的原因。2)Dato-Dxd在6mpk剂量组确实能比多西他赛提供至少2个月以上的mPFS,最新的三期临床也在这个终点上给出了显著性;然而mOS的纸面数据确实没有什么优势,果不其然现在似乎有点卡在这个终点上了;另外安全性上出现的ILD以及死亡案例,在早期临床也有预兆。
3)SKB-264的早期有效性数字显著高于两位先驱,尤其是EGFR突变患者群体更是做到了60%的ORR和11.1个月的mPFS,这可能就是MSD决定解囊的重要动力;安全性上虽然血液毒性依旧且三级以上不良反应发生率奇高,但至少没有因不良反应引起停药或死亡,也算是基本让人满意了。在TROP2 ADC对NSCLC桂冠的争夺战中,虽然Dato-Dxd率先跻身决赛圈,但似乎几位争冠者之间还仍难言胜负。
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。
















发表评论
注册或登后即可发表评论
登录注册
全部评论(0)