2023-08-29

2017年发表在JCO上的一项Pooled分析(Pooled Analysis,PA),回顾性地分析评估了武利尤单抗(Nivolumab)单药治疗晚期黑色素瘤患者的安全性。
研究人员评估了576名患者治疗相关的不良事件率、发病时间和Select AEs(那些具有潜在的免疫学病因的不良事件)的分辨率,以及Select AEs和抑制性免疫调节剂(IMs)在抗肿瘤效果方面的影响。

结果发现,有71%的患者(95% CI,67%-75%)出现了不同等级的治疗相关的不良事件,Select AEs发病的中位时间从5周(皮肤出现不良反应)至15周(肾脏出现不良反应)。
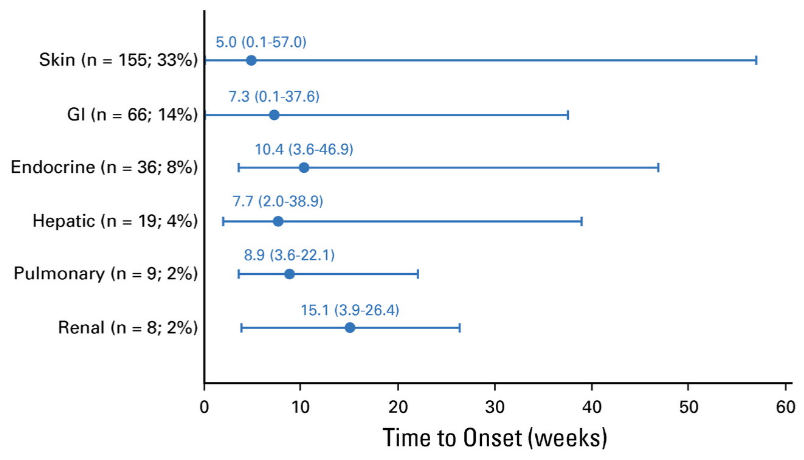
可见,药物延迟毒性在免疫治疗研究中非常常见;ADC药物,靶向药物同样具有毒性延迟发生的情况。那么,这类药物的一期临床设计的要点和难点有哪些?该如何应对?
案例1:DS-8201的一期临床试验(采用CRM设计)



案例2:IMMU-132一期临床试验(传统3+3设计)


以上两个ADC热点案例对于限制性毒性(DLT)观察周期并没有因为药物的延迟毒性而拉长,这令学员们感到困惑,对此,袁鹰教授在课程中做出了回答。

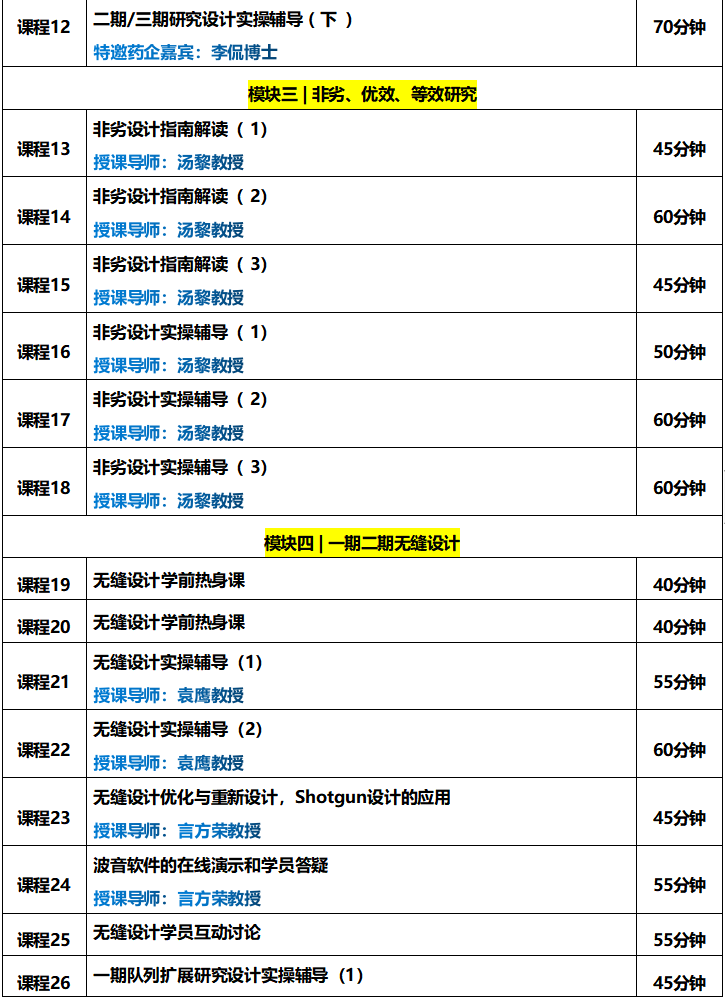
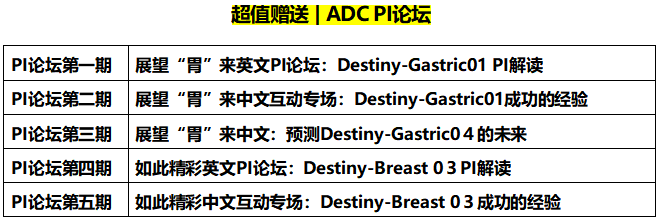
本课程源自《ADC一期临床试验设计实操训练营》
课程内容聚焦具有延迟毒性的药物,在一期临床试验探索最优剂量过程中,如何严格的执行FDA的要求,不仅要考虑最大化药物疗效,同时还要最大限度提高患者的安全性和耐受性;哪些前沿的方法是可以帮助我们高效且精准的找到这类药物的最优剂量。
课程内容:

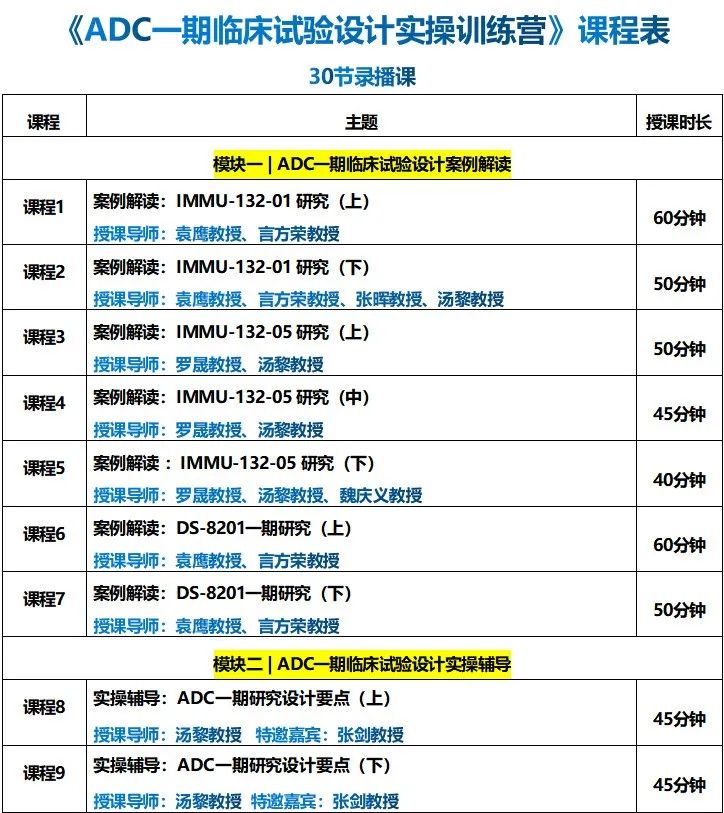

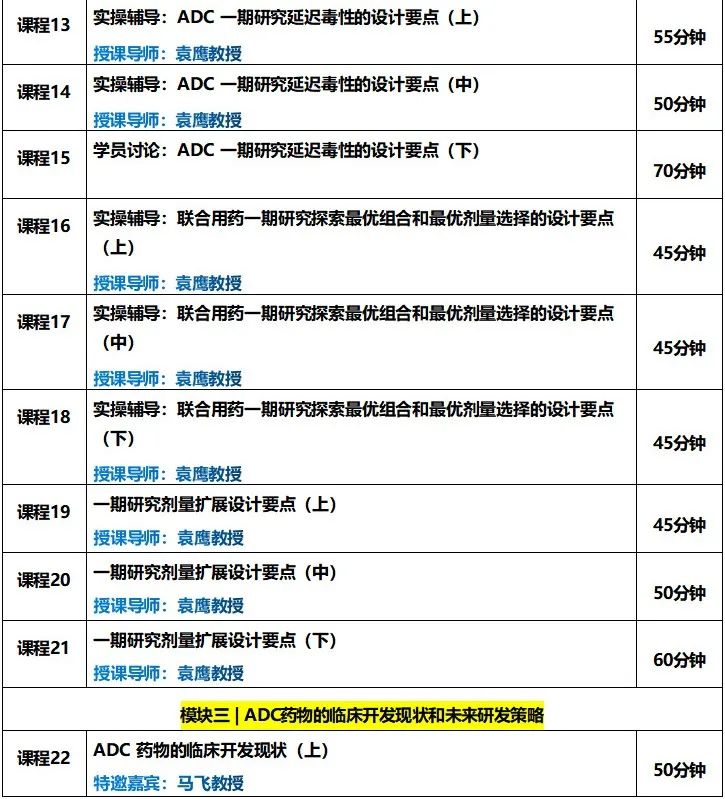

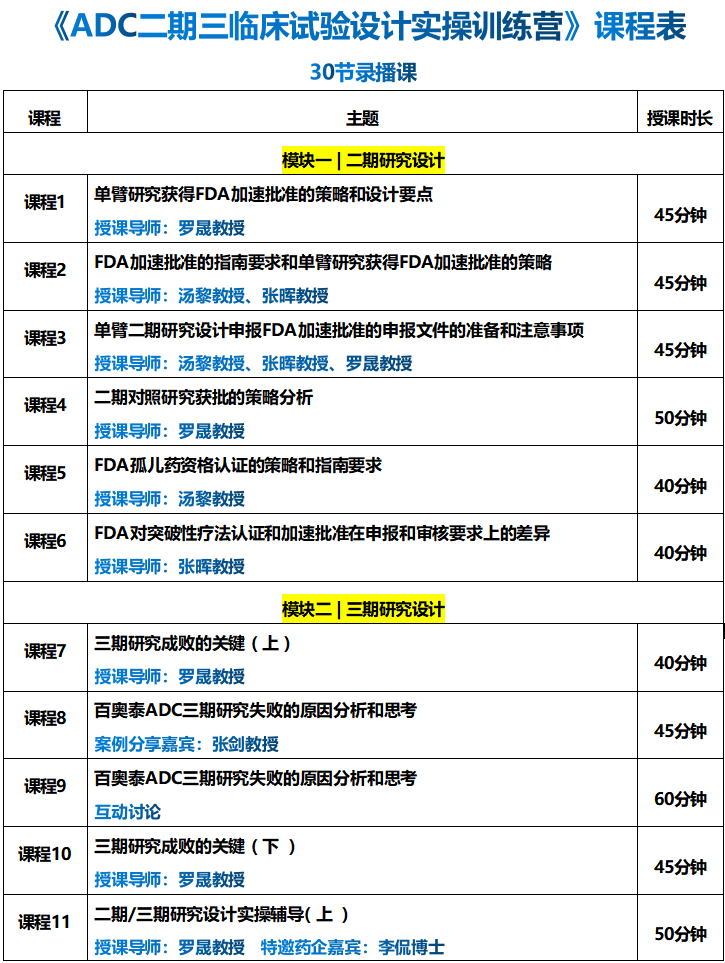

添加小编微信

百度浏览 来源 : 国际临研
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。




发表评论
注册或登后即可发表评论
登录注册
全部评论(0)