
已经是最好的命运了
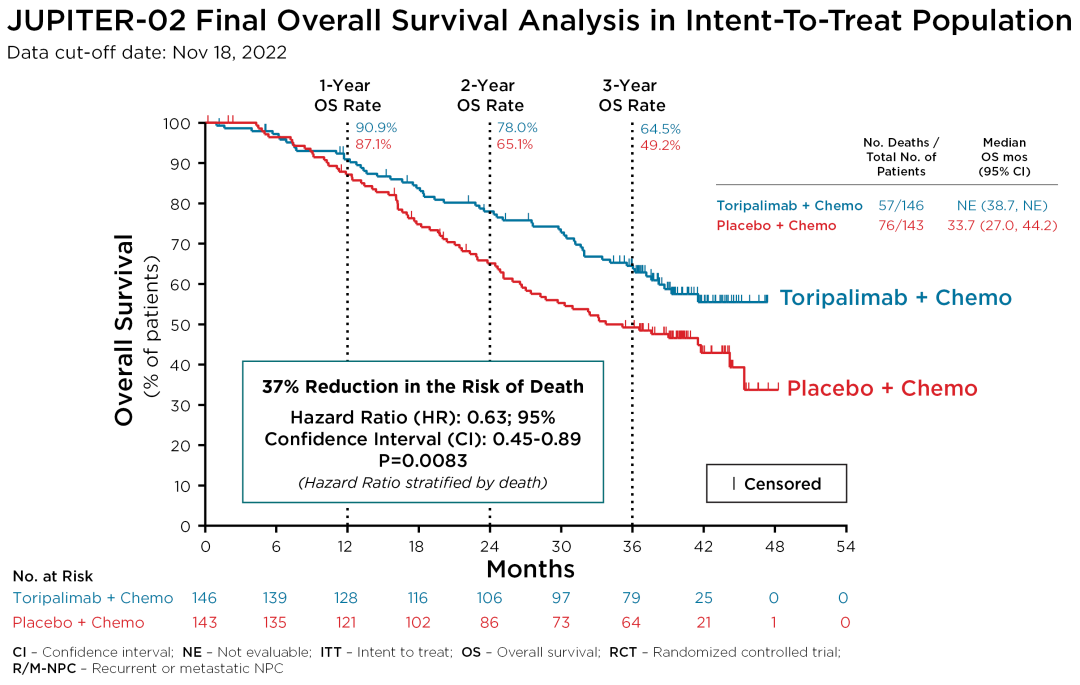
过去几年里,君实可能说过很多没法兑现的大话。但这一次真的很实在。10月30日,君实生物召开的媒体沟通会上高级副总裁姚盛对媒体表示:合作伙伴Coherus估算,美国每年新发鼻咽癌患者2000人,实际测算君实PD-1在美国的销售额峰值大约为:君实生物的确创造了历史,在美国市场获批了第一个产自中国的生物创新药PD-1。要知道2021年药明生物被美国列入UVL清单,主要原因就是美国卖给你中国企业的生物反应器、过滤器等生物药生产设备都是受管制的。FDA对海外生物制药企业都很不信任,不仅是中国。君实能抢到FDA的批文,很大程度是因为鼻咽癌这个病上美国没什么好药,特瑞普利单抗算是最对症的。但是从商业角度看,君实PD-1出海的价值基本也就限于获批了。有传言称,特瑞普利单抗在美国的定价将高达年费用300万元人民币,这显然是高估的。Coherus估算的销售峰值,是在充分考虑特瑞普利单抗疗效情况下做出的。按照君实JUPITER-02试验披露的数据,主要研究重点中位PFS是21.4月;3年总生存率OS达到64.5%。两年左右覆盖尽可能多的患者,达到销售峰值2亿美元,这是Coherus能预期的最好结果。这样算下来,君实生物实际能分到的销售分成不会太多。当时双方谈定的比例是净销售额的20%,预计君实每年能拿到2亿元人民币的分成也就是极限。这一金额远不足以弥补目前君实PD-1在国内市场上的劣势。在中国,君实PD-1价格已降到谷底。这还可能给Coherus在美国和加拿大定价带来一些障碍。欧洲市场是君实自己去申报的,目前鼻咽癌和食管癌两个适应症已经报到了欧盟和英国,相信会很快获批。不过,欧洲市场整体不如美国。以默沙东今年Q2财报为例,K药今年前9个月在美国销售额73.48亿美元,其余所有市场销售额47.18亿美元。单算欧洲市场,可能不到美国的一半。而且,默沙东在全球铺有销售成熟的网络;Coherus在美国市场上算是个新手,君实在欧洲市场也是新手。三个臭皮匠加一起成不了一个诸葛亮。退一万步讲,就算以默沙东的销售能力去打个样,特瑞普利单抗一个适应症在全球市场总销售额也是非常有限的。特瑞普利单抗的尴尬之处业界公认:获批都以小适应症为主。而且优势适应症如黑色素瘤、尿路上皮癌等,前头都有K药的无情阻拦,再度拿到FDA批文的难度可想而知。君实在默沙东编织的PD-1大网中好不容易找到一个缝隙,就像海底总动员里面的尼莫一样,一个人面对无尽的深海。目前两大真正出海的创新药几乎都是如此。百济神州花了极大的代价,证明自己的BTK比伊布替尼更好,加上高投入的全美式自营团队,才勉强抢下强生/艾伯维的一个墙角。君实摸到了美国的门槛,有机会与真正的巨头较量,只是明确表示友谊第一、比赛第二。中国创新药企的出海梦一直没停止过,仿佛拿到FDA的批文就能雄霸天下。其实,自己从头开始做全球临床到拿到FDA批文的百里无一,绝大部分biotech的出海就是拿到一个首付款而已,距离里程碑付款都非常遥远。SRS Acquiom最新发布的数据称,2023年以来拿到里程碑付款的BD总金额只占到计划金额的9%。对大药企来说,动辄给个10亿20亿美元的总里程碑是很合适的,因为它们只要付出不到十分之一的价格,就能锁定它们认为好的品种。目前来看,拿到首付款是最重要的,几十上百亿的总付款都是空中楼阁。想拿到后面的里程碑付款靠实力更要靠命,这就是绝大部分中国创新药出海的结局。从这个角度说,君实生物这次做得很实在,该多少就是多少,不玩虚的。也希望其他biotech企业今后在介绍BD项目时也实在一些。
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。







发表评论
注册或登后即可发表评论
登录注册
全部评论(0)