2023-12-13


1
Hemgenix
我价格高,但我为医保体系省了钱


2
Skysona
因为有效,价格才高

除了研究和开发基因疗法的成本外,制造这种疗法本身也很昂贵。从患者身上采集细胞后,需要55到60天才能产生一剂Skysona。
但是高昂的价格,令绝大多数的患者望而却步,虽然Blubirdbio表示如果疗效不佳可提供80%的退款,但是Skysona在欧洲上市不到3个月,就宣布由于商业策略原因退出欧洲市场,其根本都与价格有关。

3
Zynteglo
欧洲人嫌贵,我在美国卖,无效退款受ICER表扬
Zynteglo适用于需要定期输注红细胞的β地中海贫血患者。这种疾病是遗传性的,会导致血液中含氧量不足,每21000例新生儿中就有一例发生这种疾病。美国有1300至1500人患有这种疾病。

4
Zolgensma
贴着竞争对手定价,可以分期付款
与此列表中的其他基因疗法一样,诺华的Zolgensma是一种一次性疗法,旨在一次治疗,持续终生。虽然它的价格很高,但带来的临床收益持续时间也相应很长。
相比之下,第一种被批准用于治疗脊髓性肌萎缩症(SMA)的药物Biogen的Spinraza的年成本首年为75万美元,之后为每年37.5万美元。
如果不算与Spinraza注射相关的额外费用,从第五年开始,Biogen药物的累积成本将高于Zolgensma。
诺华公司发言人在声明中表示,Zolgensma的定价是反映了基因疗法的变革性质和益处,以及它所能提供的长期价值。
SMA是由SMNA1基因突变引起的罕见遗传疾病。在美国,每年约有500名婴儿出生时患有SMA。
Zolgensma使用腺相关病毒作为载体,将人SMN基因的功能性拷贝传递到靶运动神经元细胞中,从而产生正常的SMN蛋白以支持肌肉功能。
Zolgensma于2019年被批准用于患有1型SMA的婴儿,是一种开创性的治疗方法。最初的212.5万美元的定价略高于美国药物成本监管机构,临床与经济审查研究所(Institute for Clinical and Economic Review)进行的一项成本效益分析的阈值。
但诺华试图通过提供灵活的支付模式来抵消监管部门对价格的不满。
这些措施包括将付款分散在五年内,只有在药物持续起效的情况下才需继续付款。这种方法使得Zolgensma的年成本基本与Spinraza持平。
同时,该药物继续产生长期数据,显示其持久作用。在3月份的最新更新中,所有参加了一项持续15年的观察性研究的10名1期试验患者之前都到达了里程碑,最长的随访时间达到了7年半。此外,在随访期间,三名患者可以在帮助下站立。

5
Myalept
患者唯一选择,贵也得用
公司:Chiesi Farmaceutici

2014年2月24日,美国FDA批准Myalept(注射用美曲普汀)作为替代治疗药物结合饮食用于治疗先天性或获得性全身脂肪代谢障碍患者的瘦素缺乏症。
Myalept由Amryt公司研发,是一款重组人瘦素蛋白类似物。多年来,直到基因疗法出现前,Myalept在全球最昂贵药物年度排名中一直处于榜首。该产品的年用药成本约为126万美元。根据Chiesi的数据,这种药一瓶药物的价格为5867.52美元,患者平均每月使用18瓶,为105615美元。所用瓶数可能因患者而异。
脂肪营养不良是一组罕见疾病,其特征是皮肤下脂肪组织大量丧失,导致瘦素激素缺乏并导致代谢异常状况。Myalept是人类瘦素的重组形式,用于治疗先天性或后天性全身性脂肪营养不良患者的瘦素缺乏症。
2021年初,Myalept从每瓶5093美元跃升至5297美元,当时年治疗价格升至114万美元。它的价格多年来已被多次提高。
这种药物是唯一被批准用于治疗这种罕见疾病的药物,因此没有更便宜的选择。2021年,Myalept全年收入1.41亿美元。

6
Zokinvy
曾经免费,再不收高价就没机会了
公司:Eiger BioPharmaceuticals
Zokinvy是于2020年获得批准的一款孤儿药,是美国第一个用于治疗Hutchinson-Gilford早衰综合征和1岁及以上患者的早衰样核纤层蛋白病的药物。Zokinvy的本质是一种法尼基转移酶抑制剂,也是之前研发的一类分子靶向的抗肿瘤药物。如今的研究显示,它还能阻止细胞产生过多的早衰蛋白。
Hutchinson-Gilford早衰症和早衰样核纤层蛋白病是两种不同的致命疾病,其特征是过早衰老。
据估计,全世界有400人患有Hutchinson-Gilford早衰症,而早衰样核纤层蛋白病约有200人。大多数患者在15岁之前死于心脏病或中风。
与榜单中同样高价的基因疗法不同,Zokinvy并不是一种治愈方法,需要持续给药。Zokinvy的剂量取决于体表面积,它每年的平均价格约为107万美元。
Zokinvy是由默沙东和Eiger于2018年开发的。
Zokinvy上市时获得了罕见病药物的加速审查。同年晚些时候,Eiger筹集了9500万美元,并与帮助开发该药物的Progeria研究基金会分享了收益。

7
Denyelza
准备在华上市
Danyelza—准备在华上市
Y-mAbs Therapeutics在市场上只有一种批准的产品—Danyelza。
Danyelza是一种靶向神经节苷脂GD2的人源化单克隆抗体,GD2抗原在各种神经外胚层来源的肿瘤和肉瘤中呈现高表达,包括神经母细胞瘤、黑色素瘤和骨肉瘤等肿瘤。Danyelza通过与肿瘤细胞表面的GD2抗原结合,能够触发抗体介导的细胞毒性反应并激活免疫系统中的补体系统,从而达到杀伤肿瘤的效果。目前,Danyelza也正被开发用于治疗骨肉瘤以及其他GD2阳性肿瘤。
Danyelza于2020年获得FDA批准,用于治疗某些1岁及以上的复发或难治性高危神经母细胞瘤患者。具体而言,FDA批准该药物与粒细胞-巨噬细胞集落刺激因子联合用于表现出部分反应,轻微反应或先前治疗后疾病稳定的患者。
根据GoodRx 2022年的统计,该药每瓶售价超过21000美元,每位患者每年的费用约为101万美元。据GoodRx称,2021年12月,Y-mAbs Therapeutics将药物价格提高了3.5%。
Y-mAbs在3月份表示,2022年该药物收入4930万美元,与2021年相比增长了50%。该公司预计今年将从该产品中获得6000万至6500万美元。
FDA已授予了Danyelza优先审查资格、孤儿药资格(ODD)、突破性药物资格(BTD)、罕见儿科疾病资格(RPDD)。该药物的两项单臂开放标签试验结果显示,总体反应率分别为40%和34%,不仅为“加速批准”提供了证据支持,也向监管部门合和公众证明其“货真价实”。
2021年7月初,赛生药业与Y-mAbs宣布向NMPA正式递交Danyelza的上市许可申请(BLA),计划于2023年上半年在中国上市。

8
Kimmtrak
多个“第一”头衔加身,总可以卖贵点吧
公司:Immunocore

Immunocore的Kimmtrak于2022年1月获得FDA批准,是第一种治疗不可切除或转移性葡萄膜黑色素瘤的疗法,也是第一种治疗葡萄膜黑色素瘤的T细胞受体疗法,更是第一个获得FDA监管批准的TCR疗法。
葡萄膜黑色素瘤是一种眼癌,是一种罕见的恶性肿瘤,在美国每年约有1700例诊断。局部放疗通常用于预防转移,但大约一半的患者会发生转移,且此后预后不良。
Kimmtrak是一种新型T细胞受体(TCR)双特异性免疫疗法,由可溶性TCR与抗CD3免疫效应器结构域融合而成。Kimmtrak专门靶向Gp100阳性细胞,这是一种在黑色素细胞和黑色素瘤中广泛表达的谱系抗原。
Kimmtrak通过静脉输注给药,每周一次。Immunocore以每瓶18760美元的价格推出该药物,这意味着患者每年的用药成本为975520美元。但大多数患者无法接受那么长时间的药物治疗。
在3期IMCgp100-202试验中有31%的患者在6个月时仍然存活且没有疾病进展。相比之下,对照组的这一比例为19%,其接受了研究人员选择的疗法,包括默沙东公司的Keytruda、百时美施贵宝公司的Yervoy或化疗药物--达卡巴嗪。
基于“中位治疗时间为5.3个月”的研究结果,Immunocore最初估算Kimmtrak的平均费用为40万美元/人。但Immunocore在3月份的一次投资者更新中表示,现实中的治疗时间已经增长到9个月,这意味着每位患者的平均费用约为675000美元。
公司已经建立了一个名为Kimmtrak Connect的患者支持计划,向符合条件的患者免费提供Kimmtrak。
2022年,Kimmtrak给Immunocore带来了1.17亿英镑(1.41亿美元)的业绩,其中8000万英镑来自美国。英国生物技术公司正在进行一项2/3期临床试验,旨在评估Kimmtrak单药或与PD-1抑制剂联合用于先前治疗过的晚期黑色素瘤(不包括葡萄膜黑色素瘤)患者的有效性和安全性。

9
Luxturna
患者唯一选择,贵也得用不起效就退款,但还是被认为太贵
适应症:双等位基因RPE65介导的遗传性视网膜疾病
领域:基因疗法
每次治疗费用:850000美元
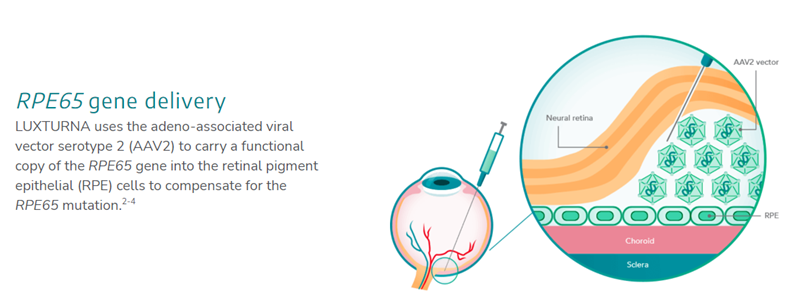
Luxturna于2017年12月获得批准,是业界首批通过监管机构审查的基因疗法之一。这种一次性疗法旨在治疗可导致失明的遗传性视力丧失。打折前,Luxturna售价85万美元,即每只眼睛425000美元。
在该药物获得批准之前,Spark认为该药物的价值超过100万美元。
早在2018年初公布时,Luxturna以85万美元的标价登上了用药成本排行榜的榜首。Spark推出Luxturna之时,恰逢公众对罕见病药品价格广泛质疑和批评,出于对这种情况的考量,Spark宣布如果药物不起作用,则不会收取全额款项。
然而并不是每个人都对Spark的定价感到满意。平价药物患者协会主席David Mitchell在用药成本公开后不久表示:“大众无法接受这样不合理的价格,今天宣布的新支付模式只是掩盖过高价格的一种方式。”
另一方面,Spark与瑞士制药公司诺华(Novartis)合作推广其基因疗法。欧洲对定价也很敏感。诺华此前表示“创新”付款模式旨在帮助降低Luxturna的成本。诺华的努力取得了回报,英国药品成本监管机构NICE于2019年末推出了该疗法。
与此同时,在美国,临床与经济评论研究所(Institute for Clinical and Economic Review)认为,Luxturna的成本应降低50%至57%,才能被认为具有成本效益。

10
Folotyn
目前独此一家,仿制药即将面世
公司:Acrotech Biopharma
Acrotech Biopharma的Folotyn在2009年已获得FDA批准,它的批准日期之早使其成为天价药名单上停留最久的药物。
Folotyn是Acrotech公司开发的一款二氢叶酸还原酶抑制剂,2009年在美获批上市,治疗复发或难治性周围T细胞淋巴瘤。根据2022年GoodRx的数据,该药物被批准用于治疗复发或难治性外周T细胞淋巴瘤,每年的费用超过84万美元。
患者通常每年服用约135瓶Folotyn。由于折扣之前的每瓶价格超过6200美元,因此即使基因疗法和其他较新产品进入市场,Folotyn仍能在世界上最昂贵的药物中保持一席之地。
值得患者庆幸的是,去年12月,Fresenius Kabi推出了该药的仿制药版本。一位发言人表示,这家仿制药制造商不对特定产品的定价发表评论。
外周T细胞淋巴瘤是非霍奇金淋巴瘤的一种亚型,在淋巴组织中形成,被认为是侵袭性的或快速生长的。除了Folotyn,其他治疗方法包括CHOP化疗方案和针对某些患者的Seagend的Adcetris。
Folotyn在2009年获得批准后立即受到了价格审查。那一年,《纽约时报》重点报道了该药物当时每月3万美元的标价,包括引用了一位United Healthcare高管的话,他称其“不合情理”。
当时,公司通过指出其开发成本以及患者对侵袭性癌症没有其他治疗选择这一事实为价格辩护。
公司在今年第四季度财报电话会议上表示,预计该药物的销售额将达到15亿美元。
百度浏览 来源 : 细胞王国
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。




发表评论
注册或登后即可发表评论
登录注册
全部评论(2)
拾陸.
2023-12-14 09:42顶1
小飞哥
2023-12-15 00:35顶1