2022-12-29 来源 : 医瑞贝生物
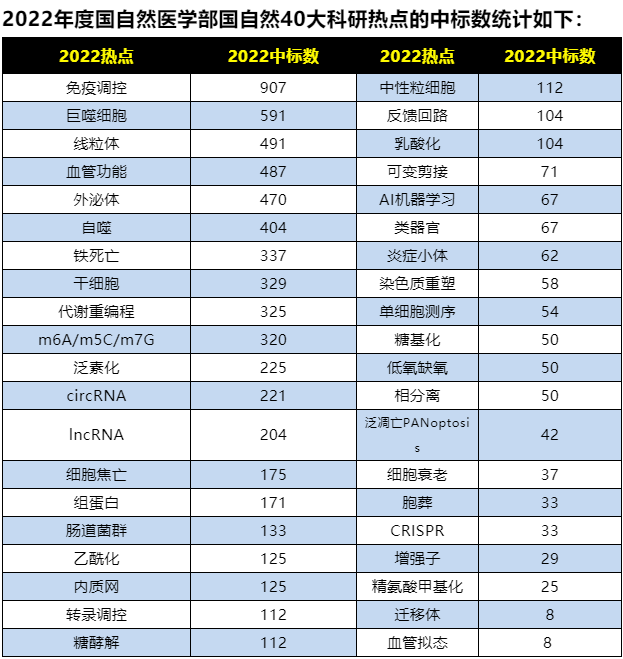
关于巨噬细胞有什么新的研究思路呢?跟着小瑞,和你一起具体分析一下~
巨噬细胞——人类免疫系统的“精灵”
巨噬细胞(macrophage),是一种位于组织内的白血球,源自单核细胞,而单核细胞又来源于骨髓中的前体细胞,是人类免疫系统的精灵。既能“上天”吞噬和杀灭胞内寄生虫、细菌等外来侵略者;又能“入地”吞噬和消灭肿瘤细胞、自身衰老和死亡的细胞,并能发挥机体的免疫防御、免疫自稳、免疫监视功能的抗原递呈细胞。
巨噬细胞是机体对病原体反应、炎症调节和组织再生的重要参与者,能够快速感知来自周围环境的多种信号,并整合信号做出相关反应从而参与机体稳态的维持。它具有两种发挥不同功能的亚型,分别是具有促炎作用的M1型和具有抗炎作用的M2型,它们在机体的某些器官或代谢反应中可能发挥相反的作用。因此巨噬细胞的代谢与功能的变化对多种疾病或者肿瘤的发生或治疗有着不可或缺的影响。
近年来,有关巨噬细胞的研究已经成为热点之一,并得到大量国家基金资助。对巨噬细胞进行相关研究的高分文献也层出不穷,这说明巨噬细胞的研究越来越受到学术界及医学界的重视。
巨噬细胞与肿瘤免疫治疗
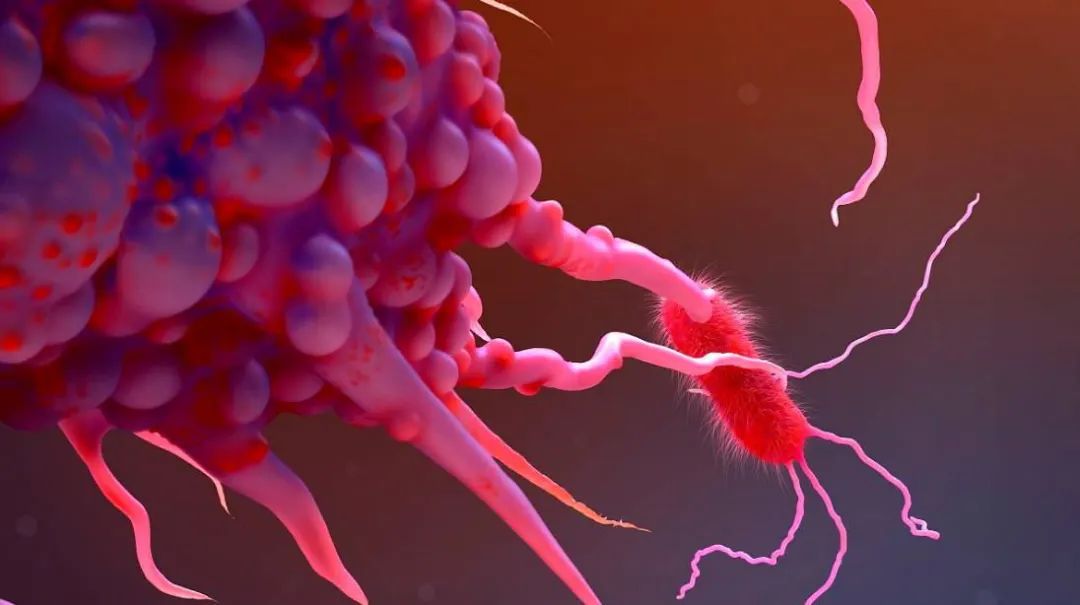
肿瘤相关巨噬细胞(Tumour-associated macrophages, TAM)是肿瘤微环境的重要组成部分。第一方面,巨噬细胞在血管生成、细胞外基质重塑、癌细胞增殖、转移和免疫抑制以及对化疗药物和检查点阻断免疫治疗的抵抗中发挥作用。另一方面,当巨噬细胞被恰当地激活时,其可以介导对癌细胞的吞噬作用和细胞毒性杀伤,并与先天性和适应性免疫系统的成分进行有效的双向相互作用。因此,巨噬细胞已成为癌症治疗中的重要治疗靶点。
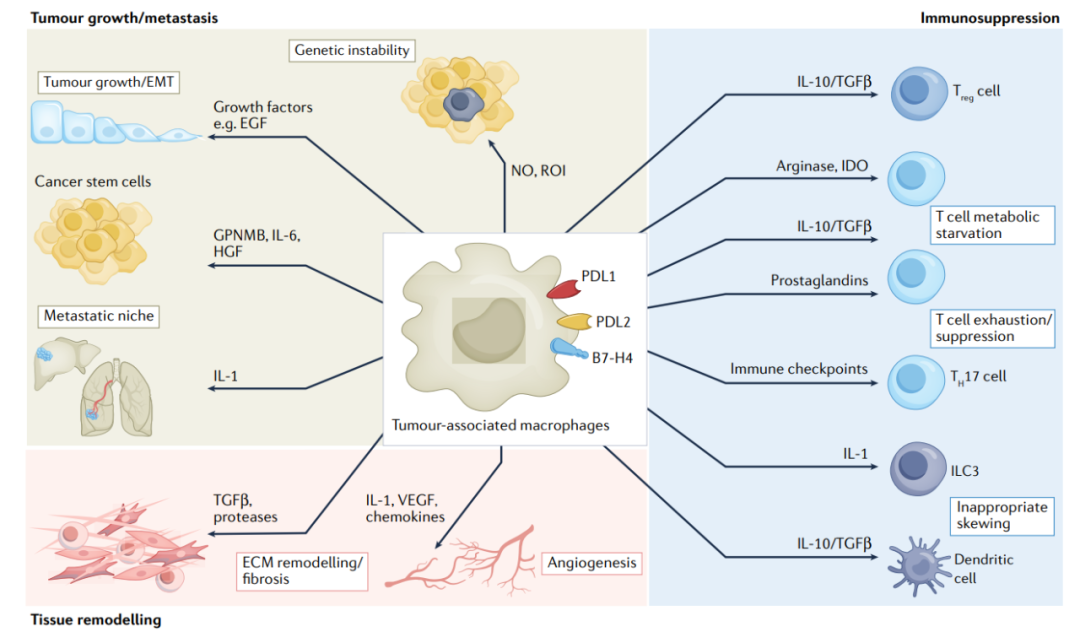
巨噬细胞靶向策略,包括促进髓系细胞募集和极化的细胞因子和趋化因子的抑制剂,以及其抗肿瘤和免疫刺激功能的激活剂。此外,早期临床试验表明,针对髓系细胞功能的免疫检查点具有很好的抗肿瘤潜力。
巨噬细胞也是细胞治疗的优良候选,嵌合抗原受体巨噬细胞(CAR-M)已进入临床评估。巨噬细胞靶向治疗有望成为肿瘤免疫治疗的下一个前沿。
巨噬细胞参与免疫逃避的机制
1、巨噬细胞参与形成抑制性髓系微环境
TME中的各种介质参与调节MDSC和单核细胞的募集,并通过不同的信号通路极化巨噬细胞,从而促进免疫抑制髓系微环境的形成。
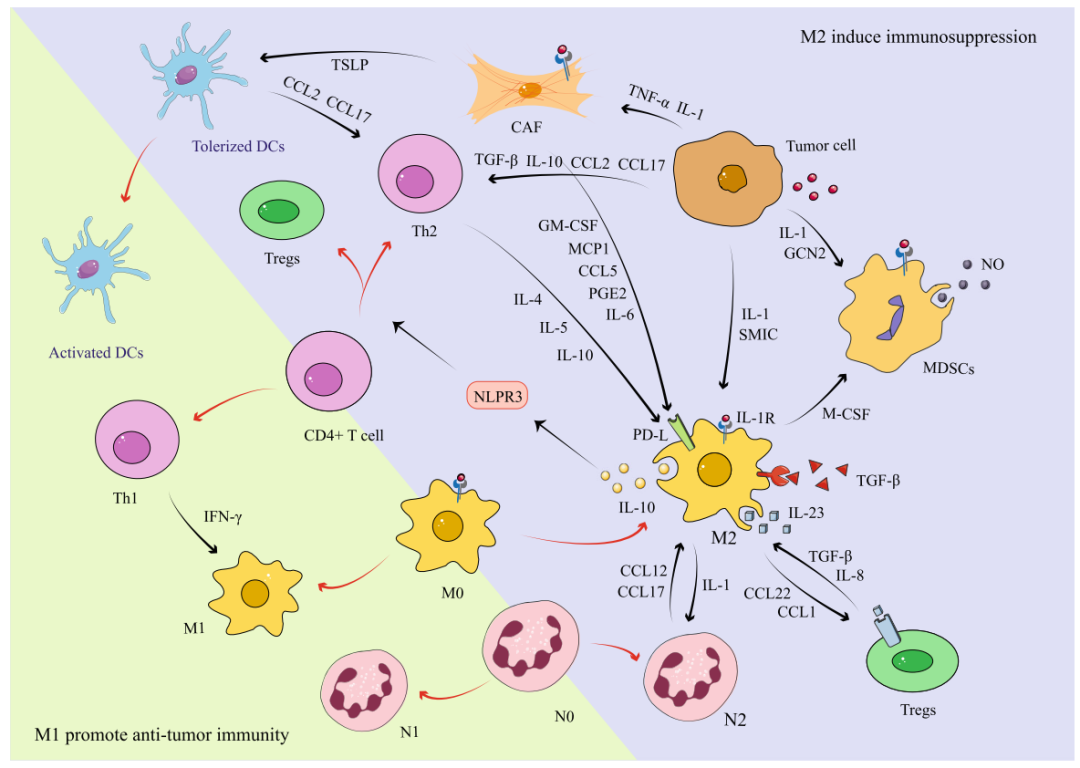
此外,巨噬细胞、MDSC和树突状细胞之间的串扰进一步形成免疫抑制髓系微环境。卵巢癌细胞高表达CD39和CD73,有助于催化细胞外ATP转化为腺苷,腺苷可以招募单核细胞并诱导它们分化为分泌IL-10的TAM。TAM表达CD39和CD73,进一步增加MDSC和TAM的浸润,从而形成一种自我放大机制,促进局部免疫逃逸。
肿瘤相关中性粒细胞(TAN)也是免疫抑制髓系微环境的重要组成部分。与巨噬细胞一样,中性粒细胞可以被描述为两个亚群,N1和N2,N1表现出抗肿瘤活性,N2被认为能促进肿瘤转移。在乳腺癌模型中,TAMs分泌的IL-1β诱导γδT细胞释放IL-17以调节G-CSF的释放并促进中性粒细胞的募集以刺激转移,表明TANs在肿瘤进展中与TAMs密切相关。然而,TAN和TAM在肿瘤发生和免疫逃逸中的特异性相互作用机制尚不清楚。
2、巨噬细胞影响Th细胞
巨噬细胞和辅助性T细胞之间存在相互调节作用。巨噬细胞依赖TGF-β和IL-10将Th1细胞转化为Th2细胞,以逆转CD8+细胞毒性T细胞和CD4+Th1细胞的抗肿瘤作用,这被认为是一种肿瘤免疫逃逸机制。
而Th细胞通过改变巨噬细胞的极化方向影响肿瘤TME。Th1细胞分泌IFN-γ以诱导M1极化,而Th2细胞可分泌IL-4、IL-5和IL-10以促进M2巨噬细胞的生成。此外,Treg表型和功能对免疫抑制性TME发挥重要作用。最近的研究表明,巨噬细胞可以通过各种途径影响Treg的增殖、迁移和功能。首先,TAMs可分泌IL-23,促进Treg的增殖以及IL-10和TGF-β的表达,抑制CTL杀伤肿瘤细胞;其次,巨噬细胞过度表达CCL1,即Treg上表达的CCR8的配体,以吸引Treg进入肿瘤区域;类似地,巨噬细胞分泌CCL22以诱导Treg迁移到卵巢癌的肿瘤区域,抑制T细胞免疫并促进肿瘤生长。
3、巨噬细胞与CAF 的相互作用
CAF是TME中最丰富的基质细胞,可释放大量细胞因子,合成和重塑细胞外基质,形成促瘤纤维微环境。CAF可分泌IL-6、M-CSF、MCP-1和基质细胞衍生因子-1,以促进巨噬细胞的浸润和分化。而M2可分泌TGF-β,以促进内皮细胞向间质细胞的转化,并增加CAF的反应性,从而增强癌细胞的侵袭性。
4、巨噬细胞通过PD-1/PD-L1轴介导免疫逃逸
TAMs调节肿瘤细胞上PD-L1和CD8+T细胞上PD-1的表达。PD-L1在多种肿瘤组织中高表达,可被TAM衍生的TNF-α上调,并与肿瘤基质中的巨噬细胞浸润呈正相关。在TME中,PD-L1在TAMs上的表达也受到许多因素的影响。IL-27/STAT3轴在淋巴瘤浸润巨噬细胞中诱导PD-L1/2过表达。Progranulin可以通过STAT3途径上调TAMs上的PD-L1,从而促进乳腺癌的免疫逃避。
同时,PD-1/PD-L1轴对巨噬细胞功能有着深刻的影响。TAMs上PD-1表达的增加可抑制其吞噬作用,并在结构上作用于mTOR途径,对巨噬细胞的增殖和活化起负调节作用。因此,PD-1/PD-L1阻断也可直接影响巨噬细胞。
PD-1/PD-L1阻断剂可促进巨噬细胞的促炎极化,增强效应T细胞的活性,并与其他免疫检查点抑制剂合作限制肿瘤扩散。除了PD-1/PD-L1轴外,一些实验结果表明TAM还可以与其他免疫检查点(如CTLA/CD86轴和TIM3/galectin-9轴)一起诱导免疫逃逸,但仍缺乏确切的证据。巨噬细胞与这些免疫检查点在免疫逃逸中的相互作用值得进一步研究。
5、巨噬细胞有助于形成免疫无反应部位
免疫无应答是肿瘤组织逃避免疫监视的重要原因,巨噬细胞可能通过以下机制参与肿瘤组织的免疫豁免。首先,巨噬细胞可以通过聚集CAF到肿瘤区域,CAF沉积纤维胶原、透明质酸、纤维连接蛋白和其他物质,并分泌赖氨酰氧化酶刺激I型胶原交联,从而形成物理屏障。
其次,与肿瘤细胞类似,诱导的TAM可表达Fas-L并释放活性可溶性Fas-L,诱导Fas+淋巴细胞凋亡,而CAF可通过MHC-1抗原交叉呈递上调Fas-L和PD-L2,抑制CD8+T细胞的活性,从而形成缺乏淋巴细胞浸润的TME。
此外,肿瘤细胞分泌的透明质酸可与巨噬细胞表面的TLR4结合,诱导TAM迁移至肿瘤相关区域,并通过miR935抑制C/EBPβ的表达,促进巨噬细胞向M2表型的分化,从而促进恶性肿瘤细胞逃避免疫监视并“冷却”免疫反应。
巨噬细胞免疫治疗的临床进展
1、靶向TAM
越来越多的证据表明TAM有助于化疗耐药性,以TAM为靶点的单一疗法或联合化疗的治疗方法正在临床前和临床中进行试验。
TAM被CSF-1招募到TME中,促进乳腺癌的发展和转移。因此,用单克隆抗体或小分子化合物靶向CSF-1/CSF-1R轴的治疗方法正在试验中。RG7155是一种靶向CSF-1R的单克隆抗体,在一项1期临床试验(NCT01494688)中对7名诊断为弥漫型巨细胞瘤的患者进行治疗,所有患者均出现PR,2名患者出现CR。此外,在RG7155治疗的患者肿瘤活检中,CD68+CD163+巨噬细胞的数量减少,表明TAM向TME的募集减少。
靶向CSF-1R、c-Kit和Flt3的酪氨酸激酶抑制剂PLX3397通过使TAM的M2表型去极化来阻断肿瘤进展。PLX3397正在包括黑色素瘤(NCT02071940、NCT02975700)、前列腺癌(NCT0149043)和胶质母细胞瘤(NCT01349036)患者中进行临床试验。其他CSF-1R抑制剂,如ARRY-382(NCT01316822)、BLZ945(NCT02829723)、AMG820(NCT01444404)和IMC-CS4(NCT01346358)也正在各种实体瘤患者中进行测试。
除了单药治疗外,针对CSF-1或CSF-1R的抑制剂还与化疗联合进行测试。例如,PLX3397与紫杉醇联合用于晚期实体瘤患者(NCT01525602);PLX3397与eribulin联合用于乳腺癌患者的试验(NCT01596751);PLX3397与vemurafenib用于BRAF突变黑色素瘤患者(NCT01826448);PLX3397联合sirolimus用于晚期肉瘤患者( NCT02584647)等。
此外,TAM的靶向剂和免疫检查点抑制剂的联合应用也在开发中。IMC-CS4与durvalumab或tremelimumab联合用于实体瘤患者的临床试验(NCT02718911)正在进行中。还有PLX3397与pembrolizumab联合用于各种肿瘤患者的1期临床试验(NCT02452424),ARRY-382与pembrolizumab的联合试验(NCT02880371),BLZ945与PDR001(一种针对PD-1的单克隆抗体)的联合试验(NCT02829723),RG7155与atezolizumab的联合试验(NCT02323191),以及AMG820与使用pembrolizumab的联合试验(NCT02713529)。
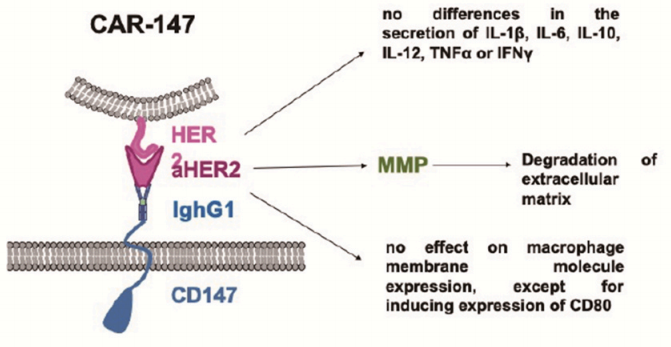
2、CAR-巨噬细胞
直到2020年11月,两个基于CAR-M策略的临床试验已经获得FDA的批准。第一个是来自CARISMA Therapeutics的候选药物CT-0508,它用抗HER2的CAR-M治疗复发/难治性HER2过度表达的肿瘤患者(I期临床试验)。另一个是Maxyte的MCY-M11,它利用mRNA转染PBMC表达靶向间皮素的CAR(包括CAR-M),治疗复发/难治性卵巢癌和腹膜间皮瘤患者,目前正在招募志愿者进行I期临床试验。
巨噬细胞最新的9大研究思路
01
Mouse pulmonary interstitial macrophages mediate the pro-tumorigenic effects of IL-9
期刊:Nat Commun 影响因子: 17.694
研究思路:
尽管 IL-9 在过继性细胞转移治疗中具有强大的抗肿瘤活性,但一些模型表明它可以促进肿瘤生长。在这里,我们表明 IL-9 信号传导与各种形式的肺癌患者的不良预后相关,并且是多种小鼠模型中肺肿瘤生长所必需的。CD4+ T 细胞衍生的 IL-9 促进肺肿瘤模型中 CD11c+ 和 CD11c- 间质巨噬细胞群的扩增。从机制上讲,IL-9/巨噬细胞轴需要精氨酸酶 1 (Arg1) 来介导肿瘤生长。
事实上,Arg1+ 而不是 Arg1- 肺巨噬细胞向 Il9r-/- 小鼠的过继转移促进了肿瘤生长。此外,使用巨噬细胞特异性纳米颗粒靶向 IL-9 信号可以限制小鼠肺肿瘤的生长。最后,肿瘤病灶中 IL-9R 和 Arg1 表达升高与肺癌患者预后不良有关。因此,我们的研究表明 IL-9/巨噬细胞/Arg1 轴是肺癌治疗的潜在治疗靶点。
02
Microbe capture by splenic macrophages triggers sepsis via T cell-death-dependent neutrophil lifespan shortening
期刊:Nat Commun 影响因子: 17.694
研究思路:
在败血症中,将全身感染与高炎症和免疫功能障碍联系起来的机制尚不清楚。细胞外组蛋白促进败血症病理,但其来源和作用机制尚不清楚。
本研究表明,中性粒细胞来源的髓过氧化物酶通过抑制组蛋白的释放来控制被脾巨噬细胞捕获的真菌和细菌,从而减弱败血症。在系统性念珠菌病中,通过吞噬受体SIGNR1捕获的微生物通过促进边缘区浸润和T细胞死亡依赖性组蛋白释放来中和髓过氧化物酶。组蛋白和菌丝在邻近的CD169巨噬细胞中诱导细胞因子,包括G-CSF,通过缩短成熟Ly6Ghigh中性粒细胞的寿命,选择性地消耗成熟Ly6Ghigh中性粒细胞,以支持具有缺陷氧化爆发的未成熟Ly6Glow中性粒细胞。在脓毒症患者血浆中,这些介质缩短了成熟中性粒细胞的寿命,并与中性粒细胞死亡标志物相关。因此,高G-CSF水平和中性粒细胞寿命缩短活性与败血症患者死亡率相关。因此,通过利用吞噬受体,病原体通过下游效应物对中性粒细胞寿命的有害影响,降低先天和适应性免疫。
03
Mouse Modeling Dissecting Macrophage-Breast Cancer Communication Uncovered Roles of PYK2 in Macrophage Recruitment and Breast Tumorigenesis
期刊:Adv Sci (Weinh) 影响因子: 17.521
研究思路:
乳腺肿瘤中的巨噬细胞浸润与增强的肿瘤进展、转移和不良临床结果相关,并被认为是治疗干预的目标。通过使用不同的遗传小鼠模型,作者表明,消融酪氨酸激酶 PYK2,无论是在乳腺癌细胞中、仅在肿瘤微环境中还是在两者中,都可以显着减少浸润性肿瘤巨噬细胞的数量,同时抑制肿瘤血管生成和肿瘤生长。
引人注目的是,仅在巨噬细胞中消融 PYK2 就足以引起类似的效果。这些表型变化与单核细胞募集减少和肿瘤相关巨噬细胞 (TAM) 的大量减少有关。从机制上讲,作者表明 PYK2 通过对关键受体信号传导的关键作用介导乳腺癌细胞和巨噬细胞之间的相互交流。具体来说,PYK2 消融抑制 Notch1 信号传导,从而减少乳腺癌细胞分泌 CCL2,同时降低巨噬细胞中 CCR2、CXCR4、IL-4Rα 和 Stat6 的活化水平。这些双向效应调节单核细胞募集、巨噬细胞极化和肿瘤血管生成。PYK2 的表达与乳腺癌患者浸润的巨噬细胞相关,其对巨噬细胞浸润和促致肿瘤表型的影响表明 PYK2 靶向可作为调节 TAM 的有效策略,并可能使乳腺癌对免疫治疗敏感。
04
Macrophage NOX2 NADPH oxidase maintains alveolar homeostasis in mice
期刊:Blood 影响因子: 25.476
研究思路:
白细胞 NADPH 氧化酶 2 (NOX2) 在病原体杀伤和免疫调节中起关键作用。NOX2 的遗传缺陷导致慢性肉芽肿病 (CGD),与微生物感染和炎症性疾病相关,通常涉及肺部。肺泡巨噬细胞 (AMs) 是稳定状态下气道中的主要免疫细胞,鉴于不断暴露于吸入物质,限制其活化很重要,但 NOX2 在此过程中的重要性尚不清楚。
在这项研究中,我们通过抑制 AM 激活,在 CGD 小鼠或 NOX2 优先在巨噬细胞中选择性丧失的小鼠中,显示了 NOX2 在维持肺稳态中的先前未描述的作用。缺乏 NOX2 的 AMs 对 Toll 样受体 2 (TLR2) 和离体 TLR4 刺激的细胞因子反应增加。此外,在 4 至 12 周龄之间,与 WT AMs 相比,具有全局 NOX2 缺失的小鼠产生了激活的 CD11bhigh AMs 子集,其表观遗传和转录谱反映了免疫激活。CGD 小鼠中 CD11bhigh AMs 的存在与稳态时肺泡中性粒细胞和促炎细胞因子数量增加以及损伤后肺部炎症增加相关。此外,优先在巨噬细胞中删除 NOX2 足以使小鼠产生活化的 CD11bhigh AM 亚群和伴随的促炎后遗症。此外,我们发现在没有 NOX2 的情况下改变的常驻巨噬细胞转录谱是组织特异性的,因为在常驻腹膜巨噬细胞中没有看到这些变化。
因此,这些数据表明肺泡巨噬细胞中 NOX2 的缺失导致其促炎性重塑和肺泡稳态失调。
05
An IL-9-pulmonary macrophage axis defines the allergic lung inflammatory environment
期刊:Sci Immunol 影响因子: 30.63
研究思路:
尽管 IL-9 在黏膜环境中发挥多效性细胞因子的作用,但 IL-9 反应性细胞库仍然没有明确定义。
在这里,我们发现 IL-9 通过靶向肺巨噬细胞介导肺中的促过敏活动。IL-9 抑制肺泡巨噬细胞扩增并促进单核细胞的募集,这些单核细胞发育成 CD11c+ 和 CD11c- 间质巨噬细胞群。IL-9 依赖性过敏反应需要间质巨噬细胞。从机制上讲,IL-9 通过诱导 Arg1 活性影响肺巨噬细胞的功能。与缺乏 Arg1 的肺巨噬细胞相比,表达 Arg1 的巨噬细胞表达更多的 CCL5。Arg1+ 肺巨噬细胞而不是 Arg1- 肺巨噬细胞的过继转移促进了 Il9r-/- 小鼠受到保护的过敏性炎症。同时,IL-9、IL-9R、Arg1 和 CCL5 的表达升高与哮喘患者的疾病相关。因此,我们的研究揭示了 IL-9/巨噬细胞/Arg1 轴作为过敏性气道炎症的潜在治疗靶点。
06
Macrophage-specific FGF12 promotes liver fibrosis progression in mice
期刊:Hepatology 影响因子: 17.298
研究思路:
#背景和目标#慢性肝病与肝纤维化的发展有关。如果不进行治疗,肝纤维化通常会导致肝硬化和 HCC。FGF12 是一种属于 FGF 超家族的内分泌因子,但它在肝脏稳态中的作用在很大程度上是未知的。本研究旨在探讨 FGF12 在调节肝纤维化中的作用。
#方法和结果#FGF12 在胆管结扎 (BDL) 诱导和 CCL4 诱导的肝纤维化小鼠模型中上调。FGF12 的表达在非实质肝细胞中特异性上调,特别是在肝巨噬细胞中。通过构建骨髓特异性 FGF12 敲除小鼠,我们发现巨噬细胞中 FGF12 的缺失可防止 BDL 诱导和 CCL4 诱导的肝纤维化。进一步的结果表明,FGF12 缺失显着减少了小鼠纤维化肝组织中淋巴细胞抗原 6 复合基因座 C 高巨噬细胞的数量,并降低了促炎细胞因子和趋化因子的表达。
同时,功能丧失和功能获得方法表明 FGF12 促进巨噬细胞的促炎活化,从而主要通过单核细胞趋化蛋白-1/趋化因子(CC 基序)受体 2 轴诱导 HSC 活化。进一步的实验表明,FGF12对巨噬细胞活化的调节主要是通过Janus激酶-转录途径激活剂的信号转导介导的。最后,结果表明,FGF12 的表达与人类肝脏样本中整个纤维化谱中的纤维化严重程度相关。CONCLUSIONS#FGF12 促进肝纤维化进展。抑制巨噬细胞 FGF12 的治疗方法可能在未来用于对抗肝纤维化。
07
Transcriptional switch of hepatocytes initiates macrophage recruitment and T-cell suppression in endotoxemia
期刊:J Hepatol 影响因子: 30.083
研究思路:
#背景与目标#肝脏在急性全身感染期间的免疫防御调节中起着至关重要的作用。然而,肝细胞簇和细胞间通讯在内毒素血症进展中的作用尚未得到很好的表征。
进行单细胞RNA测序分析,并对来自健康和内毒素小鼠的19,795个单肝细胞的转录组进行了研究。异形。通过多重免疫荧光染色、批量转录组测序或流式细胞术验证肝细胞和非实质细胞类型的空间和时间变化。此外,我们使用腺相关病毒递送系统来确认在脓毒症小鼠肝脏中介导骨髓细胞浸润和 T 细胞抑制的主要机制。
我们确定了一个主要由门静脉周围肝细胞和在较小程度上来自中央周围肝细胞,在内毒素血症中起关键的免疫调节作用。配体-受体相互作用的多细胞簇模型显示,PIHs 通过 CCL2-CCR2 相互作用在巨噬细胞的募集中起关键作用。招募的巨噬细胞 (RM) 释放细胞因子(例如,IL6、TNFα 和 IL17)以诱导抑制性配体(例如 PD-L1)在肝细胞上的表达。随后,RM 刺激的肝细胞通过内毒素血症中的 PD-1/PD-L1 相互作用部分导致 CD4+ 和记忆 T 细胞亚群的抑制。此外,血窦内皮细胞在门静脉周围区域表达最高水平的促凋亡和炎症基因。这种基因表达模式促进了门静脉区开窗数量和免疫细胞浸润的增加。~#结论#我们的研究阐明了内毒素血症在单细胞水平上对肝细胞的细胞和分子影响的意想不到的方面,并提供了开发急性感染新治疗方法的概念框架。
肝脏在急性全身感染期间的免疫防御调节中起着至关重要的作用。我们确定了一个促炎性肝细胞亚群,并证明该亚群与募集的巨噬细胞的相互作用在内毒素血症期间的免疫反应中至关重要。这些新发现为在急性感染中发现合理的治疗靶点提供了一个概念框架。
08
FSTL1 promotes liver fibrosis by reprogramming macrophage function through modulating the intracellular function of PKM2
期刊:Gut 影响因子: 31.793
研究思路:
Follistatin 样蛋白 1 (FSTL1) 被广泛认为是一种分泌型糖蛋白,但其在肝纤维化期间调节巨噬细胞相关炎症的作用尚未得到证实。在这里,我们旨在表征巨噬细胞 FSTL1 在肝纤维化发展中的作用。
对来自 33 名肝纤维化患者和 18 名无肝纤维化患者的人类肝脏样本作为对照进行表达分析。构建骨髓特异性 FSTL1 敲除 (FSTL1M-KO) 小鼠,探讨巨噬细胞 FSTL1 在四氯化碳注射、胆管结扎或蛋氨酸缺乏和胆碱缺乏饮食诱导的 3 种肝纤维化小鼠模型中的功能和机制。FSTL1 表达在人和小鼠纤维化肝脏的巨噬细胞中显着升高。骨髓特异性 FSTL1 缺乏有效地减缓了肝纤维化的进展。在 FSTL1M-KO 小鼠中,肝纤维化期间形成的微环境显示出相对较少的炎症,这可以通过单核细胞/巨噬细胞和中性粒细胞的浸润减弱和促炎因子的表达减少来证明。FSTL1M-KO 巨噬细胞在体内和体外表现出抑制的促炎性 M1 极化和核因子 kappa B 通路激活。此外,这项研究表明,通过其 FK 结构域,FSTL1 直接与丙酮酸激酶 M2 (PKM2) 结合。有趣的是,FSTL1 促进 PKM2 磷酸化和核转位,减少 PKM2 泛素化以增强 PKM2 依赖性糖酵解并增加 M1 极化。PKM2 (DASA-58) 的药理激活部分抵消了 FSTL1 介导的糖酵解和炎症。
巨噬细胞 FSTL1 基于巨噬细胞的细胞内 PKM2 重编程功能,通过诱导 M1 极化和炎症来促进肝纤维化的进展。
09
Lung emphysema and impaired macrophage elastase clearance in mucolipin 3 deficient mice
期刊:Nat Commun 影响因子: 17.694
研究思路:
肺气肿和慢性支气管炎是慢性阻塞性肺疾病的两个最常见原因。已知过量的巨噬细胞弹性蛋白酶 MMP-12 主要由肺泡巨噬细胞分泌,可介导肺损伤和肺气肿的发展。在这里,我们发现内溶酶体阳离子通道粘磷脂 3 (TRPML3) 作为 MMP-12 从支气管肺泡液中再摄取的调节剂,在两个独立产生的 Trpml3-/- 小鼠模型中驱动肺损伤扩大,在弹性蛋白酶或烟草后进一步加剧烟雾处理。
从机制上讲,使用 Trpml3IRES-Cre/eR26-τGFP 报告小鼠模型、转录组学和内溶酶体膜片钳实验,我们表明在肺中 TRPML3 几乎完全在肺泡巨噬细胞中表达,其丢失导致早期内体运输缺陷和MMP-12 的内吞作用。我们的研究结果表明,TRPML3 是肺泡巨噬细胞清除 MMP-12 的关键调节因子,可作为肺气肿和慢性阻塞性肺疾病的治疗靶点。
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。





发表评论
注册或登后即可发表评论
登录注册
全部评论(0)