2021-08-20 来源 : 生物制药小编
自SARS-CoV-2大流行爆发以来,出现了多种变异株。近期在国内爆发的疫情中以Delta突变株为主,与此同时,在南美大陆Lambda突变株正在快速传播并且已经扩散到全球四十余国家;8月10日,据《医疗新闻》杂志报道,美国纽约卫生部门研究团队判断,纽约发现的新冠病毒变异株Iota (B.1.526)致死率大幅提高。
这些突变株究竟有何异同?
现在的疫苗还能起效吗?
突变株抵抗力与传染力变化
假病毒中和实验,验证突变株对BNT162b2(辉瑞-BioNTech),mRNA-1273(moderna),Ad26.COV2.S(强生)疫苗的中和抵抗力。
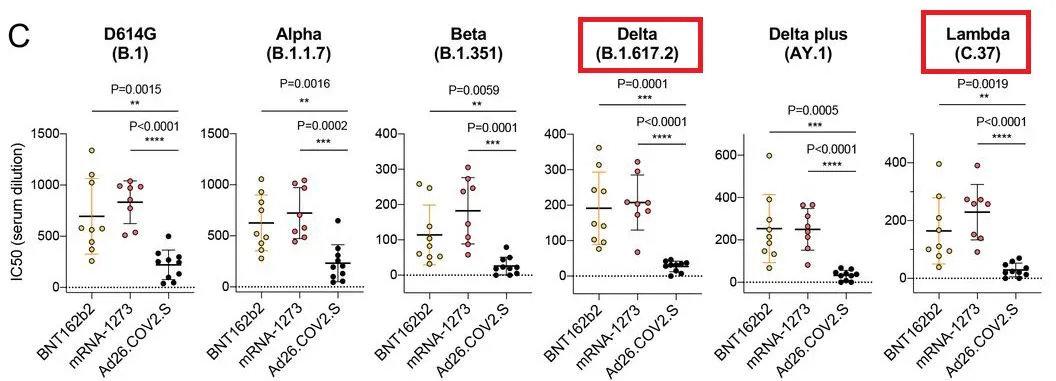
纵坐标是中和抗体滴度(IC50),上图每一个小圆点代表一次中和试验结果,小圆点中间的那条短横线是若干次中和试验结果的中位数。短横线的位置越高代表疫苗产生的中和抗体对毒株的中和效果越好。可以通过比较不同抗体短横线的位置来初步了解对应毒株的免疫逃逸能力。
如图所示,Lambda株对疫苗抵抗力超过Delta株。
假病毒中和实验,验证突变株对科兴疫苗的中和抵抗力。
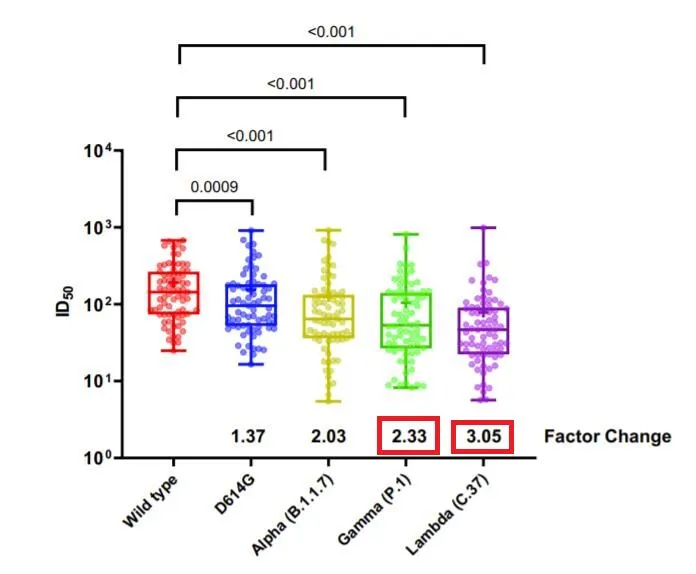
原理和上图差不多,比较短横线的高度可。下方标的数字是抗体中和能力下降倍数。lambda的3.05就是说接种科兴疫苗后产生的中和抗体对lambda的效果相对武汉株的效果下降了3.05倍。
Delta之所以能席卷全球,是因为传染性超越了Alpha,而Lambda的传染性同样超越了alpha。

全球42个国家各种病毒株流行率增长速度做的元数据分析,中间的标杆(黑色虚线)代表Alpha,其他毒株则用黑点表示。黑点上面的黑色线段代表了置信区间。黑点越靠右,就意味着传染性相对alpha越强。如图所示,Delta传染力第一,B.1.621传染力第二,Lambda第三。
新冠突变株简介
疾病预防控制中心和世界卫生组织建立了区分新出现的SARS-CoV-2变体的分类系统:Variants of Concern (VOCs)和Variants of interest(VOIs)。如Alpha (B.1.1.7)、Beta (B.1.351)、Gamma (P.1)和Delta (B.1.617.2),均与传播性和毒力增强有关,被列为VOCs;如Eta(B.1.525)、Iota (B.1.526)、Kappa(B.1.617.1)和Zeta (P.2)等被列为VOIs。
SARS-CoV-2 Variants of Concern (VOCs)
Alpha (B.1.1.7 lineage)
Alpha(B.1.1.7)突变株于2020年12月底,在英国报告的新突变体。此毒株在2020年底迅速扩散,2021年1月初仅占美国过去两周内新冠感染病例的0.2%;2月底,占比上升至11.4%;而到了4月,占比上升至66%;到5月8日已升至72.4%,成为主流变异毒株。
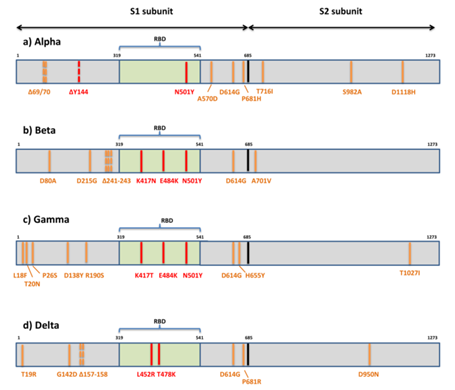
Alpha株包含17个突变,其中有8个突变(Δ69-70 deletion, Δ144 deletion, N501Y, A570D,P681H, T716I, S982A, D1118H) 位于Spike 蛋白(S蛋白,病毒入侵关键蛋白)中。N501Y突变表现出Spike蛋白与ACE2受体亲和力提高,增强了病毒附着并随后进入宿主细胞。
Beta(B.1.351 lineage)
Beta(B.1.351)突变株,Tegally等报道的一种新变体。该病毒于2020年10月在南非纳尔逊·曼德拉湾引发了第二波新冠病毒感染。
Beta株的Spike蛋白包含9个突变 (L18F、D80A、D215G、R246I、K417N、E484K、N501Y、D614G、A701V),其中3个突变 (K417N、E484K、N501Y) 位于RBD区域(S蛋白上与ACE2受体结合关键区域),提高了与ACE2受体的结合亲和力。据报道,该变体具有较高的传播风险,并降低了单克隆抗体治疗、恢复期血清和疫苗接种后血清的中和作用。
Gamma (P.1 lineage)
Gamma(P.1)突变株于2020年12月在巴西被确认,并于2021年1月在美国首次发现。根据世卫组织2021年3月30日发布的最新流行病学信息,该变体已蔓延至45个国家。
Gamma株的Spike蛋白有10个突变 (L18F、T20N、P26S、D138Y、R190S、H655Y、T1027IV1176、K417T、E484K和N501Y),有三个突变(L18F、K417T、E484K)位于RBD区域,与Beta株相似。重要的是,这种变体可能降低单克隆抗体治疗、恢复期血清和接种后血清的中和作用。
Delta(B.1.617.2 lineage)
Delta(B.1.617.2)突变株,最初于2020年12月在印度发现,是导致2021年4月印度出现第二波致命COVID-19感染的原因。在美国,这种变体于2021年3月首次发现,并成为美国未来几周最主要的SARS-CoV-2毒株。2021年7月,南京爆发的新冠疫情,通过对疫情中的病例基因组测序结果显示,毒株为delta突变株。
Delta株的Spike蛋白含有10个突变(T19R, (G142D*), 156del, 157del, R158G,L452R, T478K, D614G, P681R, D950N),具有对人体适应性更强、传播速度更快、病毒载量更高、治疗所需时间更长、更容易发展成重症等特点。此外,Delta突变株能够逃避免疫系统产生的中和抗体的中和能力,Moderna公司发布的研究显示,与含有D614G变异的野生型新冠病毒株相比,mRNA-1273新冠疫苗接种者血清对Delta突变株的中和能力降低了2.1倍。
SARS-CoV-2 Variants of interest (VOIs)
Epsilon (B.1.427 and B.1.429)
Epsilon (B.1.427和B.1.429)突变株,于2020年6月左右在美国出现,从2020年9月1日至2021年1月29日,在测序病例中从0%增至50%,与野生型流行毒株相比传播性增加了18.6-24%。
Epsilon株带有以下突变 (B.1.427: L452R, D614G; B.1.429:S13I, W152C, L452R, D614G)。由于其传播能力增强,美国疾病控制与预防中心将该毒株列为VOI(Variants of Interest,关注变种)。
Zeta (P.2)
Zeta (P.2)突变株于2020年4月在巴西首次发现。其Spike蛋白具有关键突变 (L18F; T20N; P26S; F157L; E484K; D614G; S929I; V1176F) ,由于此变体对于抗体治疗和疫苗血清的中和作用可能降低,被世界卫生组织和美国疾病控制与预防中心列为VOI。
Eta (B.1.525)与Lota(B.1.526)
Eta (B.1.525)和Lota (B.1.526)突变株于2020年11月在纽约首次发现,由于此突变株对于抗体治疗和疫苗血清中和作用可能降低,CDC和世卫组织将其列为VOI。8月10日,据《医疗新闻》杂志报道,美国纽约卫生部门研究团队判断,在美国纽约发现的新冠病毒变异株Iota (B.1.526)致死率显著提高。在研究期间,与其他新冠变异毒株相比,45~65岁、65~74岁以及75岁以上的感染人群死亡率分别提高46%、82%和62%。
其Spike蛋白具有关键突变 (B.1.525: A67V, Δ69/70, Δ144,E484K, D614G, Q677H, F888L; B.1.526: (L5F*), T95I, D253G, (S477N*), (E484K*),D614G, (A701V*))。
Theta (P.3)
Theta (P.3)突变株,其Spike蛋白携带关键突变(141-143 deletion E484K; N501Y; P681H),并于2021年2月在菲律宾和日本首次发现。曾经是VOI,后来因为这些突变株的病例数不断减少,对疫情影响越来越低,现在已被降级为 “需要进一步监控的突变株”(alerts for further monitoring)
Kappa(B.1.617.1)
Kappa(B.1.617.1)突变株携带关键突变((T95I)、G142D、E154K、L452R、E484Q、D614G、P681R和Q1071H),于2020年12月在印度首次发现。与Delta突变株同属于印度变异病毒的亚种之一。Spike蛋白发生重大突变的特性使得Kappa病毒跟Delta一样,更易感染细胞并避开免疫系统的抗体反应。
Lambda(C.37)
Lambda(C.37)突变株最初在秘鲁发现。医学界首次注意到Lambda时,200个受检样本仅能检出1例。到2021年3月,秘鲁首都利马约50%新冠病例源于该变异株感染。WHO数据表明,今年五六月间,秘鲁82%的新增病例源于Lambda变异株感染,人均新冠死亡率飙升至世界第一。目前,该突变株已经在包括秘鲁、智利、阿根廷和厄瓜多尔在内的数十个南美国家传播,英国等国家也已经发现Lambda突变株感染者。
Lambda株在Spike蛋白上发生多处变异,主要包括G75V、T76I、del247/253、L452Q、F490S、D614G和T859N。其中RSYLTPGD246-253N、L452Q和F490S突变,导致其对免疫抵抗力增强;并且T76I和L452Q突变,导致其传染性增强。这让Lambda毒株同时具备了传染性增加和免疫逃逸能力增加的能力,从而获得了大规模传播的潜力。
从假病毒中和实验可以看得,并不是所有疫苗都对突变株有好的保护效果,而且从原理上来说,疫苗不会达到100%的保护效果,个体免疫反应一定会有差异。因此必须对疫苗进行突变株保护率的效价评估,用以指导疫苗接种、疫情防控和疾病治疗。
评估疫苗诱导中和抗体常用假病毒系统和免疫阻断法。
文末可见近岸蛋白质提供的假病毒、Spike突变蛋白、RBD突变蛋白等产品清单。
新冠疫苗评估方法
假病毒侵染验证
中和抗体可阻止病毒侵染细胞,在病毒感染细胞系统中加入中和抗体(注射疫苗后的血清/中和抗体阳性对照),检测被侵染细胞减少情况,计算其阻断效果。
因新冠病毒的高传染性及致病性,使用新冠活病毒进行侵染验证必须在生物安全三级以上实验室进行,受实验室条件和病毒来源的限制。另外,由于病毒株、培养条件以及对结果的评估标准不同,不同实验室的活病毒检测结果常存在一些差异。从安全性以及可操作性,使用假病毒更方便,且假病毒易于实现标准化,利于评估临床前及临床阶段的疫苗的抗病毒效果。通过对比不同的突变株假病毒株对免疫后的血清样本进行中和抗体的检测,可以有效的评估该疫苗对突变株的中和效果。
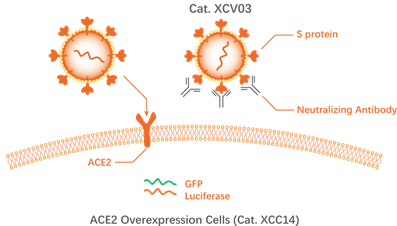
中和抗体抑制新冠假病毒侵染细胞(来源:www.novoprotein.com.cn)
假病毒检测系统:新冠假病毒(Novoprotein Cat.XCV03)无自我复制能力,其表面表达S全长蛋白,内含绿色荧光蛋白(GFP)和荧光素酶(Luciferase)报告基因,可以特异性侵染表达ACE-2的细胞(Novoprotein Cat.XCC14)。被病毒侵染后的细胞即表达GFP和Luciferase,发出荧光,从而可以便捷观察结果,并通过化学发光酶标仪检测,实现定量分析。假病毒测定法可通过进一步优化实现高通量检测和标准化检测。通过替换S蛋白表达质粒(蛋白质编码基因),可以研究抗S蛋白抗体针对不同突变株的交叉中和作用。
小结
1、假病毒检测系统病毒滴度高,检测精度和重复性好;
2、假病毒含荧光报告基因,利于定量和标准化;
3、假病毒无自我复制能力,只侵染表达ACE-2的细胞,更加安全。
免疫阻断验证
病毒侵染验证法是从细胞水平来验证中和抗体的效用,适用于疫苗研发阶段。利用突变株的蛋白,针对大规模疫苗接种后的人群,可快速评估每个人的中和抗体对突变株的保护效果,可使用更简单快捷的免疫阻断验证法。
免疫阻断验证利用中和抗体阻断S-RBD蛋白与ACE-2结合的原理,通过加入中和抗体后,检测结合在ACE-2上S-RBD蛋白的减少量来计算中和抗体的滴度。
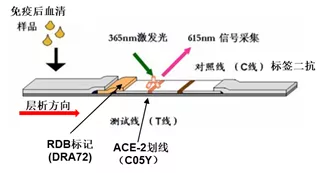
时间分辨荧光免疫层析检测中和抗体竞争性抑制S-RBD结合ACE-2 (来源:www.novoprotein.com.cn)
使用同样的免疫阻断原理,也可采取ELISA或者侧向层析胶体金法检测中和抗体。
ELISA,中和抗体阻断S蛋白与ACE-2结合,IC50为25ng/ml (来源:www.novoprotein.com.cn)
小结
1、操作简便,检测时间短(<30min),可用于现场筛查和大规模检测;
2、成本低,性价比高,利于大规模检测;
3、结果直观,可应用于接种疫苗后的快速检测。
T细胞免疫应答评估
目前一些研究表明,在抵抗新冠时,仅靠诱导中和抗体应答并不能充分保护机体,T细胞的免疫应答也具有非常重要的作用。有研究表明,所有完全康复的个体都能检测到中和抗体、辅助T细胞和杀伤T细胞,总体而言,具有广泛、协调良好的免疫反应的人,其病症较轻,特别的,强烈的新冠病毒特异性T细胞反应是较轻症状的前兆。一些轻症患者即使没有检测到病毒特异性抗体反应,也会触发强烈的记忆T细胞反应。65岁以上的人更有可能出现T细胞反应不良和免疫反应不协调的情况,因此会出现更严重或更致命的COVID-19。老年人对COVID-19的大量易感性部分似乎是一种较弱的适应性免疫反应,这可能是因为老年人的初始T细胞较少。另外,疫苗接种后的记忆T细胞更是会持续性保护机体,所以,评估疫苗诱导的T细胞免疫反应至关重要。
有研究发现在未感染新冠的人群中也检测到了新冠病毒N蛋白特异性T细胞,而且SARS康复患者中的特异T细胞与SARS-CoV-2 具有强大交叉反应性。这表明,常见的β冠状病毒感染可诱导人体产生对冠状病毒结构蛋白NP的多特异性和持久的T细胞免疫。所以验证疫苗所诱导的特异性T细胞应使用新冠特异性的S-trimer Protein(Novoprotein Cat. DRA49)为主。
评估疫苗引发的T细胞免疫反应,金标准是IFN-γ ELISpot检测PBMC(外周血单核细胞)的免疫应答,即使用S蛋白分别刺激疫苗接种前后同一志愿者体内的PBMC,接种后T细胞分泌的IFN-γ程度应该是接种前数倍。
酶联免疫斑点技术(Enzyme-Linked Immunospot Assay,ELISpot)可从单细胞水平检测分泌抗体细胞或分泌细胞因子细胞。IFN-γ作为免疫活性细胞分泌的细胞因子在诱导抗病毒免疫中起着重要的免疫调理作用,包括激活细胞毒性T淋巴细胞(cytotoxic lymphocyte,CTL)、自然杀伤细胞(natural killer cell,NK)细胞和吞噬细胞等,而在疫苗免疫后机体产生IFN-γ的水平实际上反映辅助性T细胞的活动。因此,使用ELISpot检测IFN-γ的水平就是间接地检测辅助性T细胞活性。
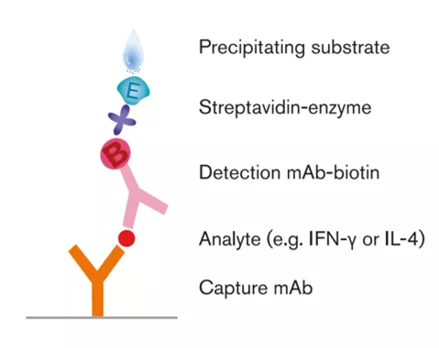
ELISpot检测PBMC分泌IFN-γ
IFN-γ ELISpot操作流程
1、用抗IFN-γ的单克隆抗体包被在检测孔的底部;
2、分离待检测样本PBMC;
3、将待测PBMC放入检测孔,同时加入刺激物S-trimer Protein(Novoprotein Cat.DRA49)。在培养期间,对S蛋白有反应的T淋巴细胞就会被激活,开始分泌特定的细胞因子IFN-γ,这些细胞因子同时被板底的单克隆抗体捕获;对S蛋白没有反应的细胞则不受刺激,也不分泌特定的细胞因子IFN-γ;
4、移出细胞,板底留下细胞因子的潜在“影像”;
5、加入生物素标记的检测抗体,检测抗体与“影像”上的细胞因子结合,形成“抗体-抗原-抗体”的夹心结构;
6、加入链霉亲和素标记的酶溶液,通过链霉亲和素与检测抗体上标记生物素结合,形成复合物;
7、加入显色底物,在酶的催化分解下,生成不可溶的色素,就近沉淀在局部的膜上形成斑点并计数。
每一个斑点代表了一个对特异抗原有反应的特异性T淋巴细胞。通过使用不同的突变株蛋白,可评估T细胞对突变株的免疫反应,从而评估该疫苗对突变株的保护效果。斑点的数目多少就反映了样本的细胞免疫的识别状态:斑点多说明免疫识别状态好,斑点少说明免疫识别状态差或者出现免疫耐受。
小结
1、ELISpot灵敏度高,在一百万个阴性细胞中只要有一个分泌细胞因子的阳性细胞即可被检测出来。
2、ELISpot检测的是单个细胞分泌,而非细胞群体的平均分泌。
3、ELISpot检测到的细胞因子不是在细胞正常状态下就存在的,而是在检测的过程中活细胞受到刺激物的刺激后分泌出来的。斑点的强弱和数量直接反映了细胞对刺激物的反应能力和分泌细胞因子的能力。
4、结果直观,一个阳性细胞对应一个斑点。
近岸蛋白质Alpha突变假病毒及S蛋白
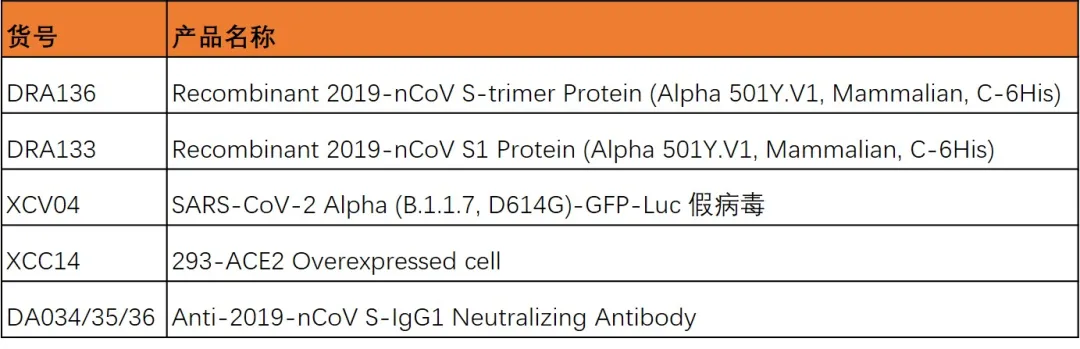
Beta突变假病毒及S蛋白
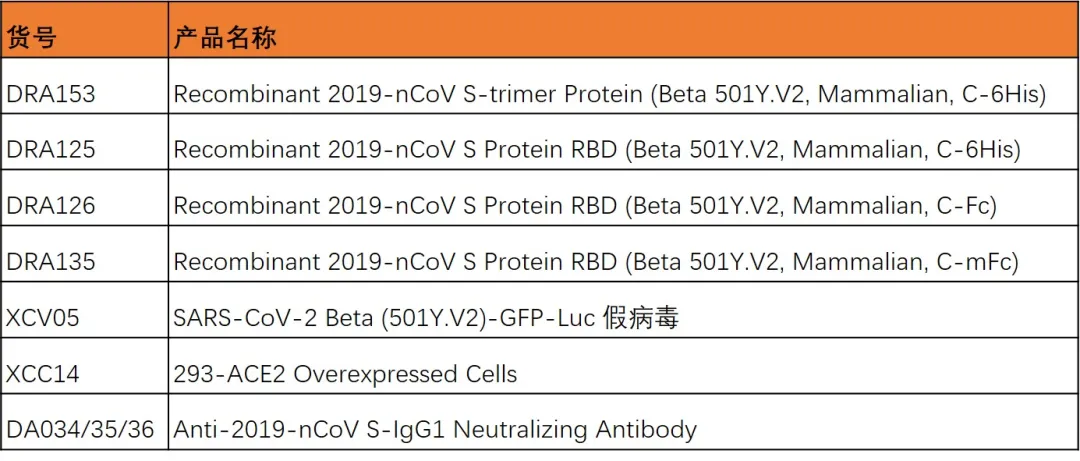
Gamma突变假病毒及S蛋白
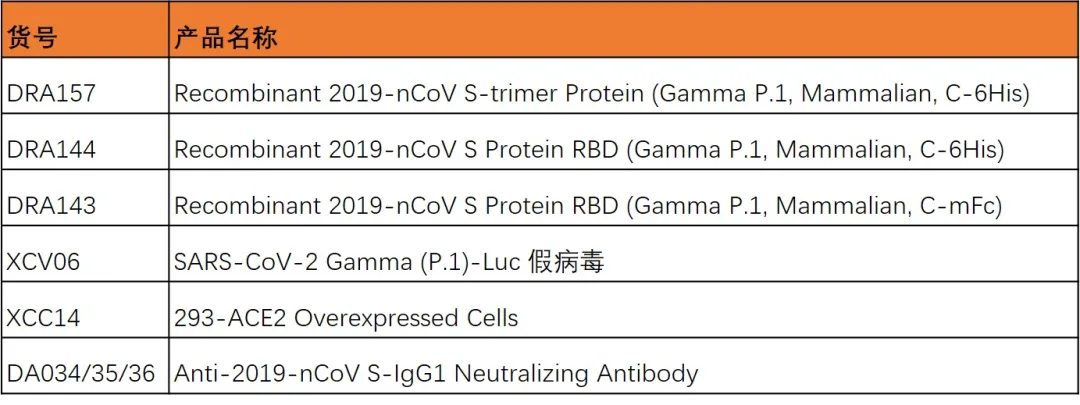
Delta突变假病毒及S蛋白。
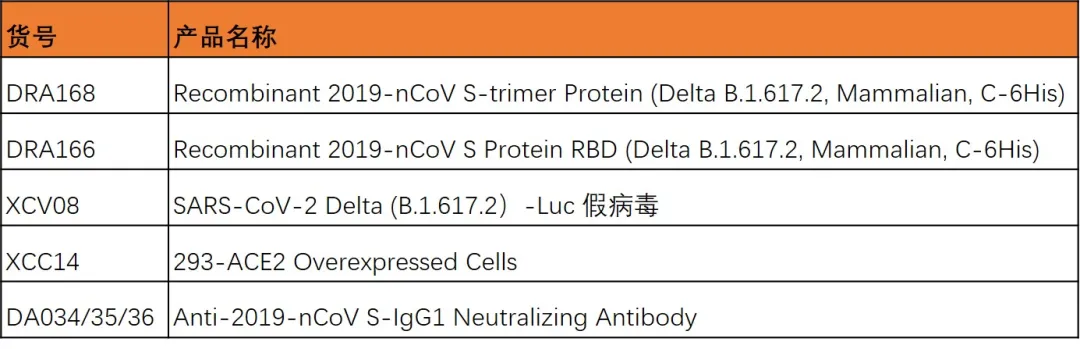
Epsilon突变假病毒及S蛋白。
Eta突变S蛋白。

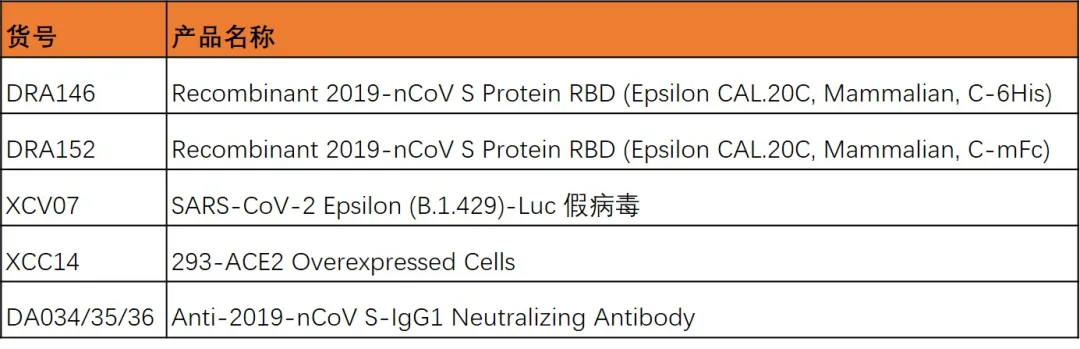
Kappa突变假病毒及蛋白。
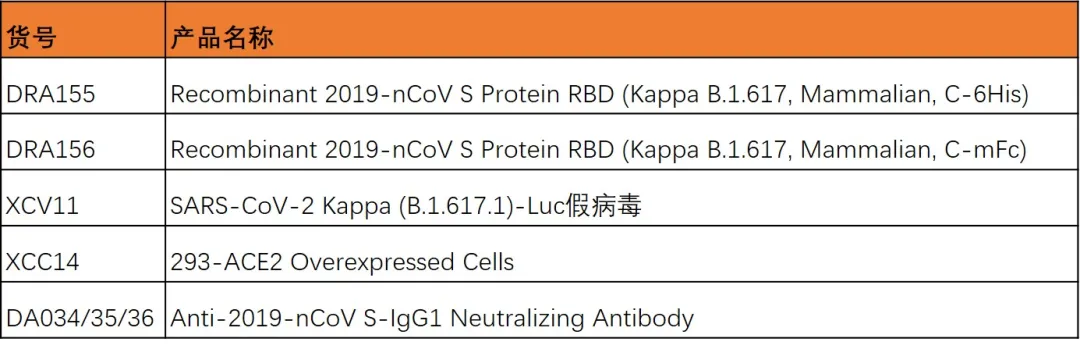
Lambda突变假病毒及蛋白。
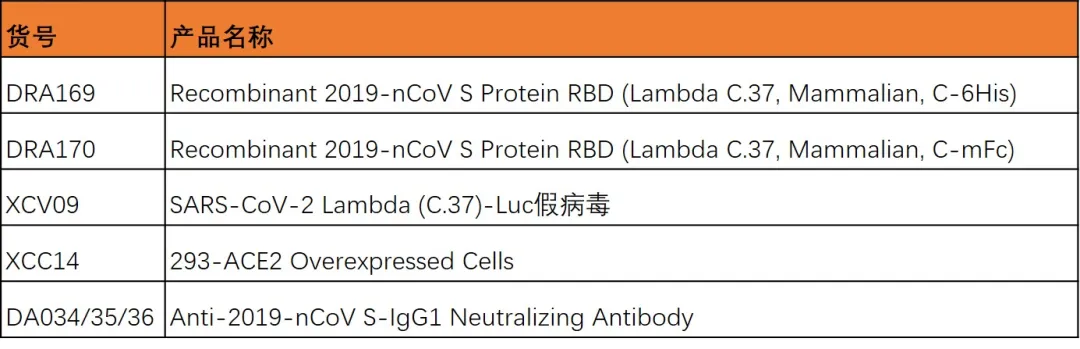
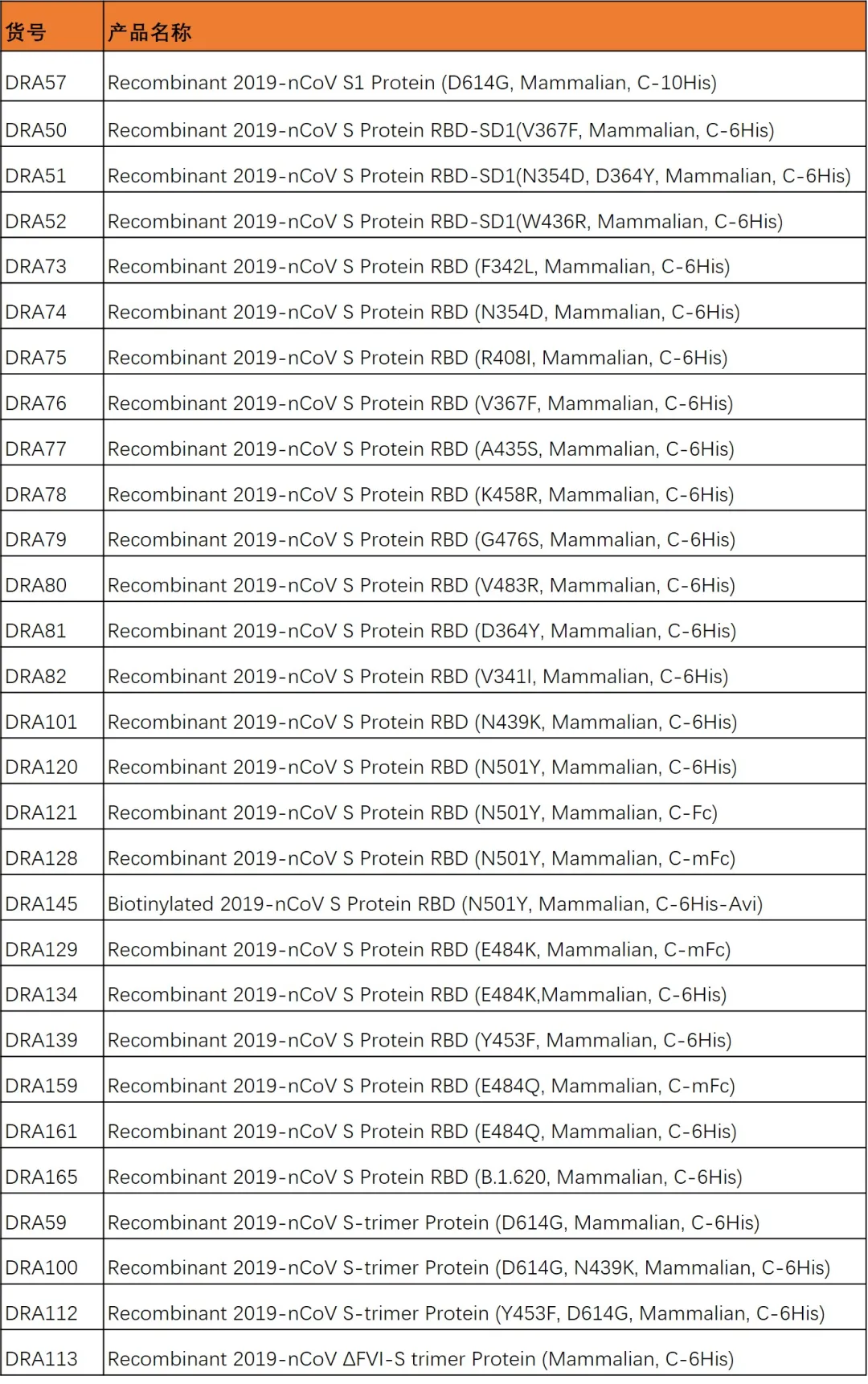
其他突变体蛋白详见下表。
参考文献:
https://www.biorxiv.org/content/10.1101/2021.07.19.452771v1.full
https://www.medrxiv.org/content/10.1101/2021.06.28.21259673v1.full.pdf
疫苗的研发阶段验证,临床实验验证加上接种后的中和抗体检测,构筑起整个疫苗效价评估体系。
随着疫苗实验进展频繁出现好消息,隧道的尽头已然出现曙光,未来会有不同种类的新冠疫苗可供世界选择,不久的将来我们会迎来不需要口罩的晴天。
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。





发表评论
注册或登后即可发表评论
登录注册
全部评论(0)