2022-06-10 来源 : Claudisiran药药 ,作者机车宝贝

AZ整个肿瘤管线的布局
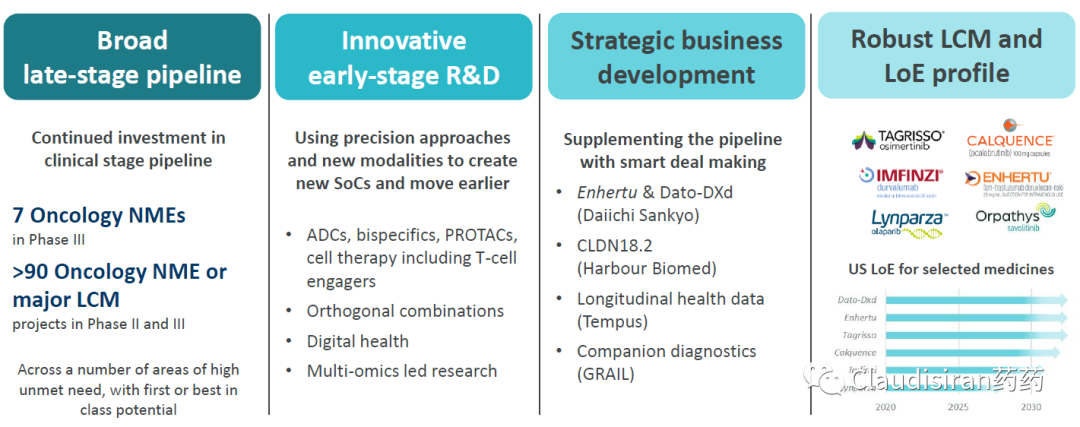
合计18个品种(在研+已上市),全面铺开各种modality,包括双抗、Protac、CAR-T等;已上市品种大部分都会在2030年之后才过期,除了Lynparza,所以未来几年的增长一定是稳稳的!
ASCO会议:AZ已经连续做了4年的Plenary Presentation,分别是
1)POLO研究:olaparib治疗1L BRCA胰腺癌;
2)ADAURA研究:Osimertinib治疗EGFR肺癌辅助疗法;
3)OlympiA研究:olaparib治疗早期高风险乳腺癌;
4)Destiny-Breast04:HER2-low乳腺癌(FIC适应症);
ESMO会议:连续5年持续同样的荣耀,特别是去年的Destiny-Breast03(与T-DM1头对头治疗复发乳腺癌)

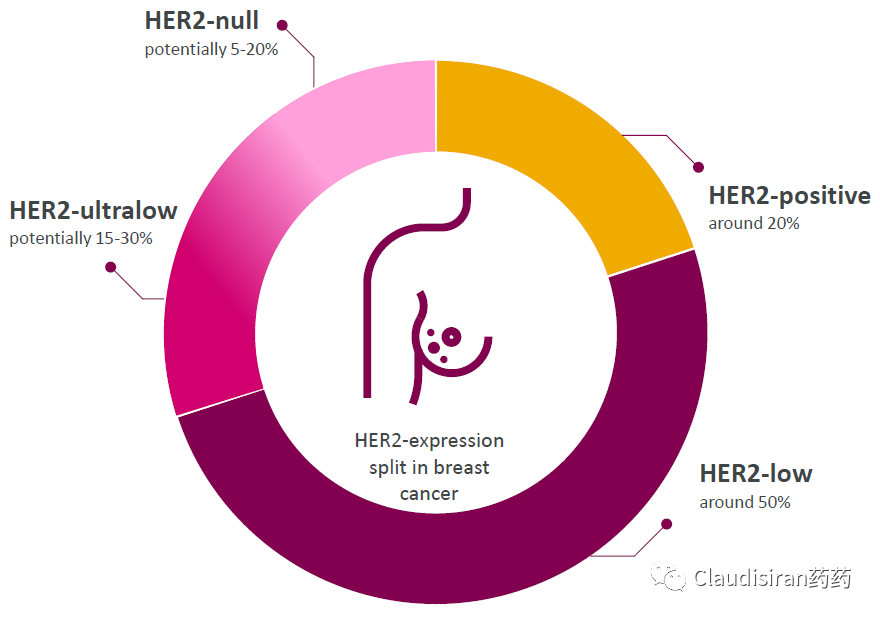
HER2-low 乳腺癌流行病学
Destiny-Breast04这项研究的重大意义在于它重新定义了乳腺癌该怎么分类
以前只有HER2+或者HER2-,而介于中间的HER2-low(低表达)是没有单独被定义/划分的,因此也没有一套专属于他们的标准疗法的。
HER2-low的定义
HER2 status为 IHC 1+/2+,ISH-,是近几年来的一个新定义,这类患者以前是被归纳到HER2-的范围内,治疗方案主要看HR的情况。
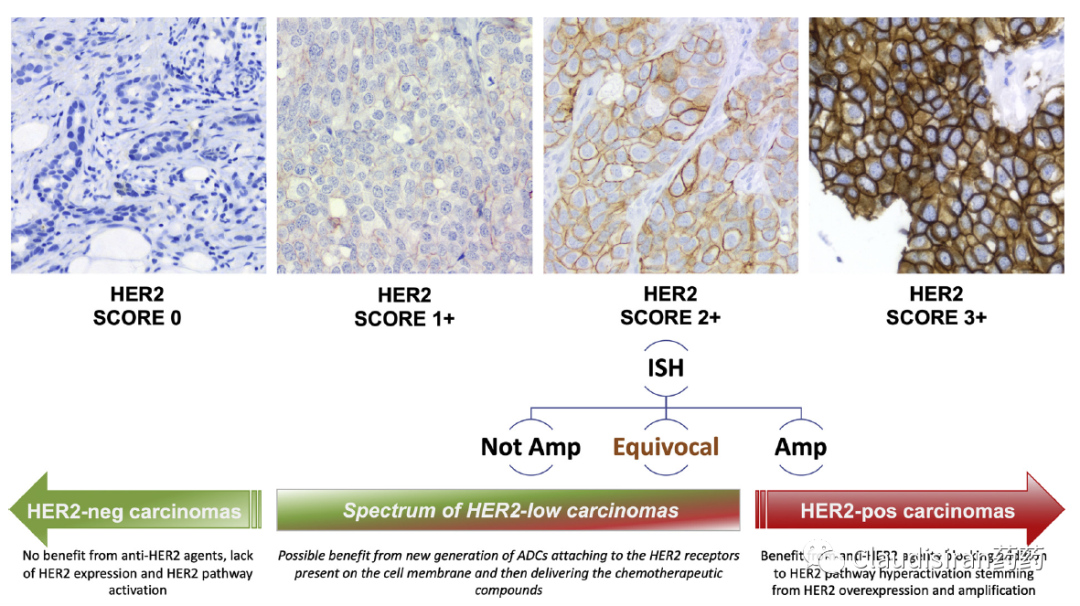
HER表达量根据IHC来划分
IHC3+:HER2+ or HER2-high,每个细胞大约有200w个HER2;
IHC2+:HER2-low,约20w~50w个;
IHC1+:HER2-low,约10w~20w个;
IHC0~1+:HER2-ultralow/超低,约2w~10w个;
IHC0:HER2-null,约2w个。
两个知识点
1)HER2-low~HER2-null细胞表达的TROP2是HER2的5倍,所以这里就需要Dato-DXd(TROP2 ADC)。
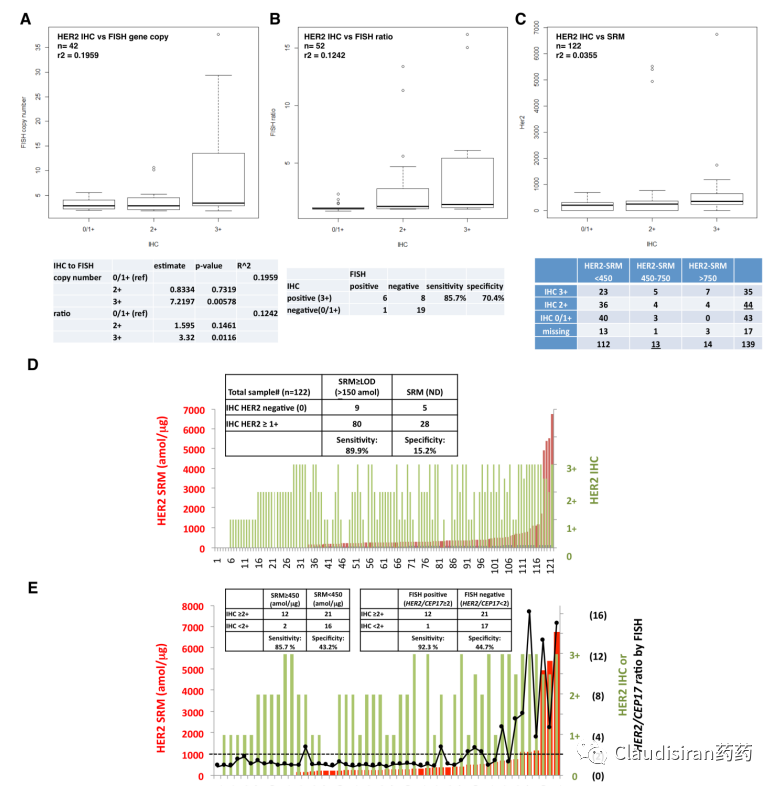
2)How low can we go?新定义的疾病需要有新的伴随诊断来捕获更多的患者。Destiny-Breast06研究将会告诉我们这个答案,因为它纳入了曾有过IHC0的患者;现在对于HER2表达量的测量是基于IHC,化学染色法。在HER2表达非常低的一个范围内(即IHC0),IHC精确度/敏感度还是有一定限制的,所以可能需要更高的科技,例如 mass spectrometry,如下图。
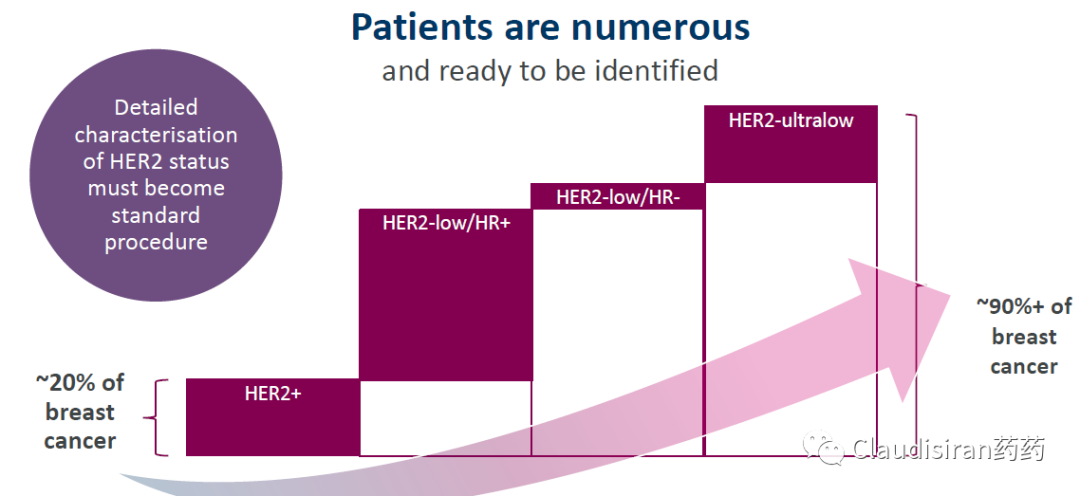
患者数量/市场空间
按以前的HER2+或者HER2-来划分,HER2+仅占20%,其余80%是以前的HER2靶向药没法治疗的患者(如果是HR+,那么CDK4/6+ET可以治疗1~2年,然后就会出现耐药的问题)。
现在将HER2-low划分出来,占比高达50%,是HER2+的2.5倍,也就是说T-DXd在以前的“曲妥珠类药物”的基础上开辟了一个2.5倍新的市场空间。按照NIH估算,2022年预计会有29万新发乳腺癌患者,以此为基础,对应HER2-low大约15万。
When all subtypes are combined, female breast cancer is fairly common. In 2022, it is estimated that there will be 287,850 new cases of female breast cancer.
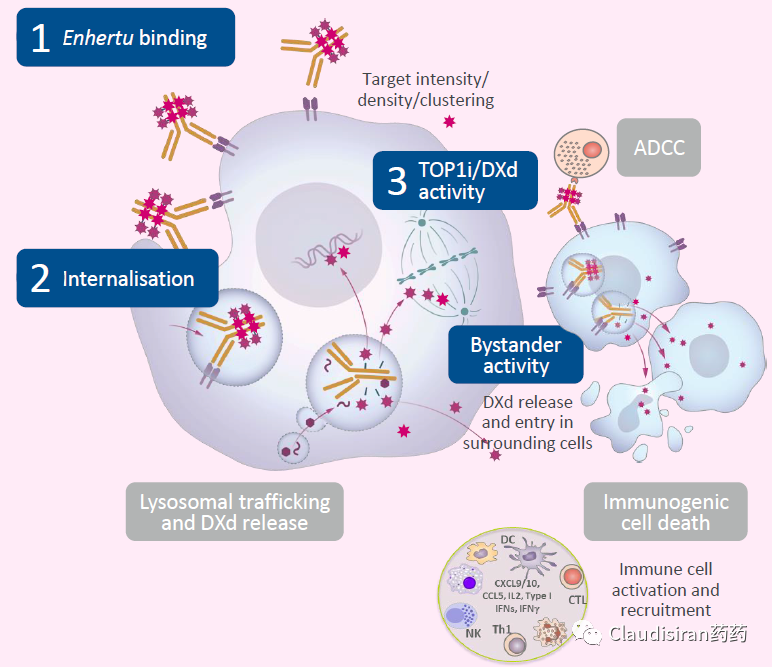
T-DXd治疗HER2-low的优势
之所以T-DXd对于HER2-low有如此好的效果得归因于它的毒素Dxd比较容易穿透diffuse细胞膜,也就是说即便在细胞裂解之前,就已经开始产生“旁观者效应”。
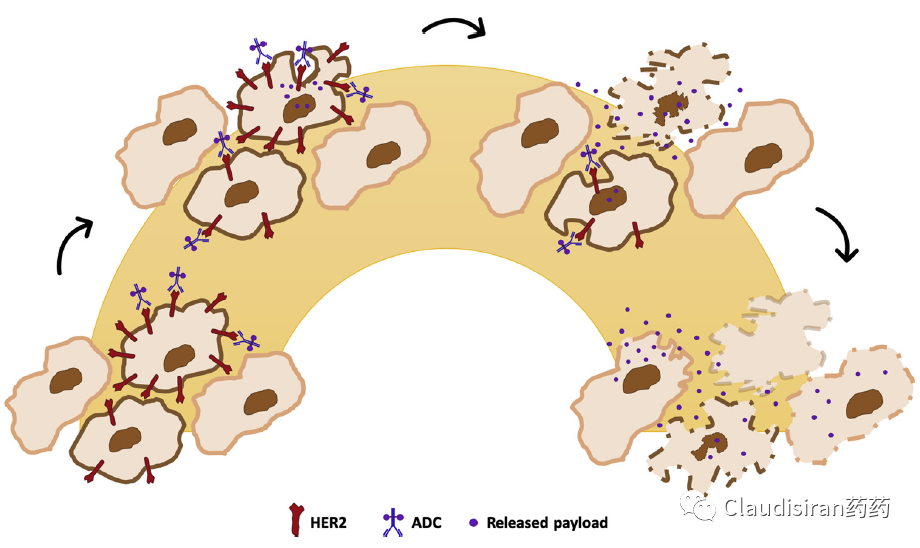
事实上所有的肿瘤都有一定的heterogeneity,即一坨肿瘤里的细胞们HER2以及其他靶向标志物的表达量往往是不一样的,所以抗体无法精准锁定每一个癌细胞。
理论上来讲,在特异性非常强的情况下,如果不靠by-standard effect,有可能疗效还会有一定的打折。
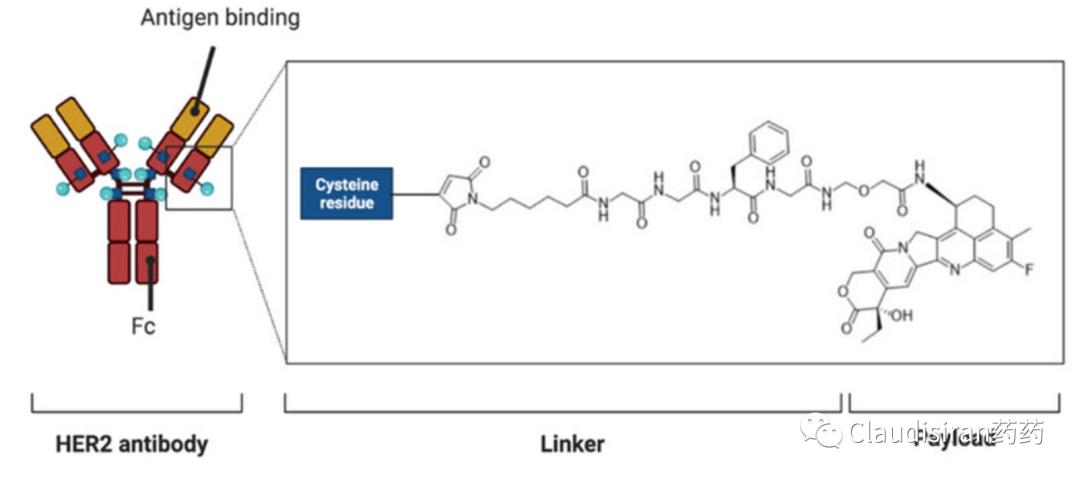
安全性的把控
由于T-DXd选用的4肽linker(glycine–glycine–phenylalanine–glycine tetrapeptide-based linker)在外周循环系统(可以理解为没有肿瘤的血液系统里)非常稳定,不会释放毒素,所以进一步控制了毒性(毕竟是一个DAR~8:1的品种)。
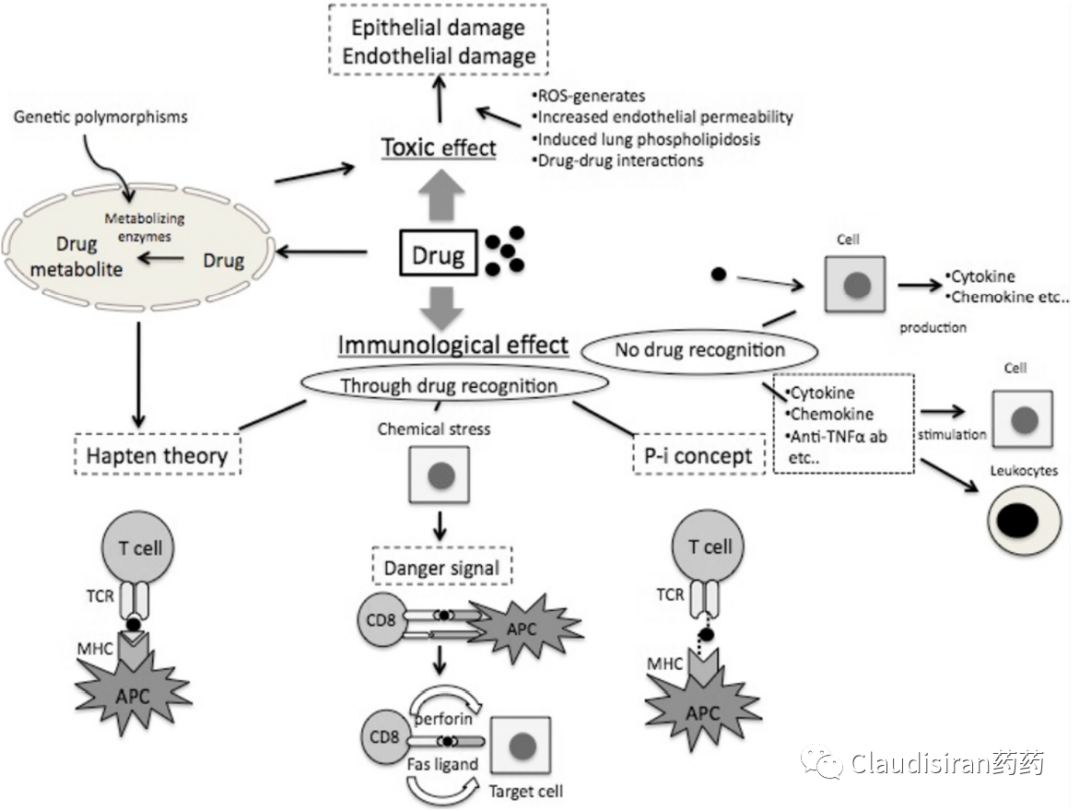
可能有人会问:那为什么T-DXd会有ILD(间质性肺病,interstitial lung disease)这个比较常见的副作用呢?
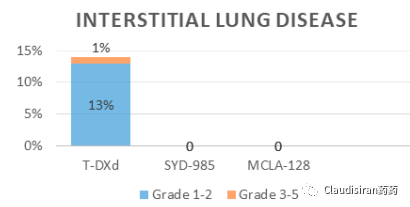
这个可能跟它的linker design没有太大的关系。
首先很多药物都会引起ILD,特别是抗肿瘤的药物。
其次肺部的上皮细胞也会表达HER2,因此也解释了为什么很多曲妥珠单抗相关药物都会引起ILD。
最后,与DXd(Deruxtecan)相关的药物也是与ILD的发生有比较强的相关性。Dato-DXd也是用的一样的linker,就没有看到过ILD。
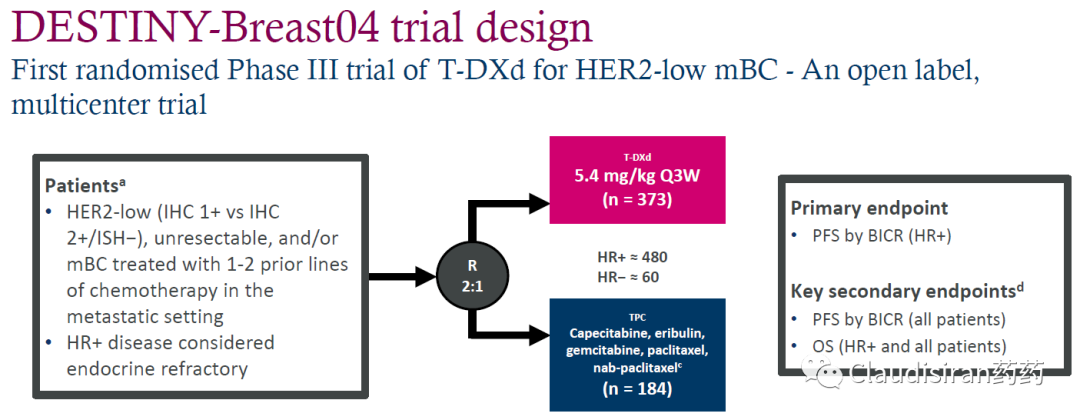
DB04 数据解读
实验设计如下:
3L+(经CDK4/6、化疗、ET治疗),约90%为HR+(符合真实世界实际比例),与一系列医生自己选择的化疗做对照;中位随访时间约18个月。
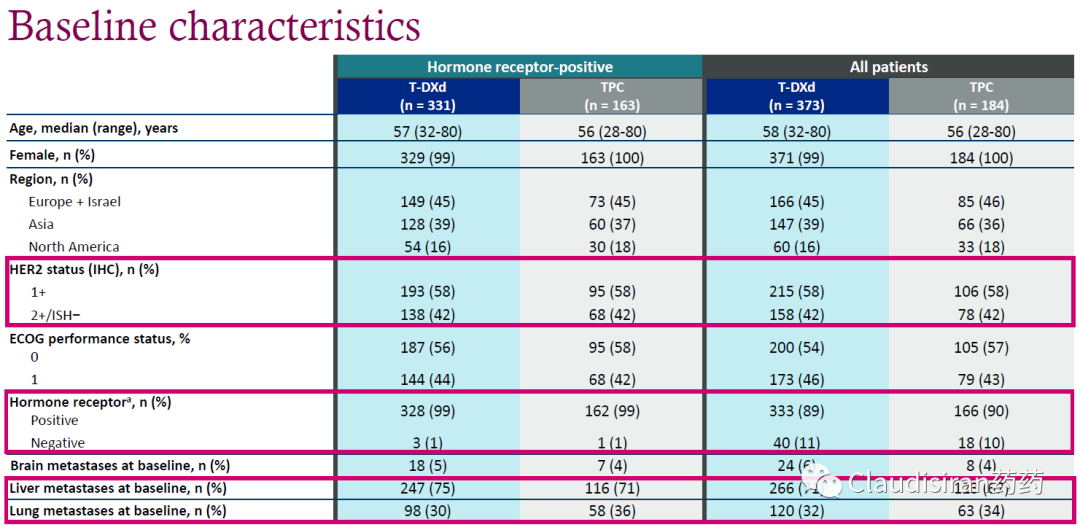
患者基线情况如下:
IHC1+和IHC2+患者比例约58%:42%。
疗效数据PFS(AZ原版PPT有误,下图来自NEJM)
HR+:mPFS=10.1m,比chemo多4.7m,HR=0.51,p<0.0001;
HR-/TNBC:mPFS=8.5m,比chemo多5.6m,HR=0.46;最难治的患者,chemo的mPFS只有3个月,同时也是疗效差异最明显的一组;
ITT:mPFS=9.9m,比chemo多4.8m,HR=0.50,p<0.0001。
结论:大体上,不管HR-status如何,T-Dxd效果都很明显。
注:Hazard Ratio和Risk的关系:风险降低率=1-HR。
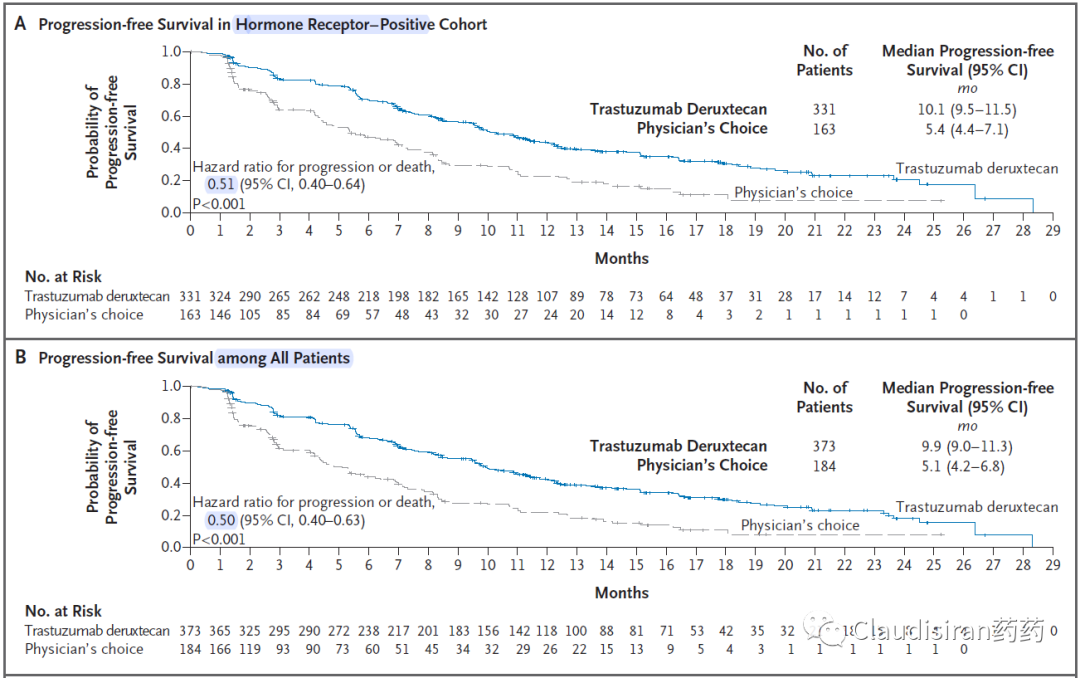
非常值得注意的两点是:
1)对于HR+的患者,Destiny-Breast04的生存曲线在很早的阶段就分开了。
对比一下我们之前看到过一些口服SERD临床研究,有一部分患者因某些原因对内分泌疗法应答非常有限,KMcurve在早期阶段重合度比较高。
说明T-Dxd可以在SERD的基础上突破了这类内分泌疗法低应答的患者。
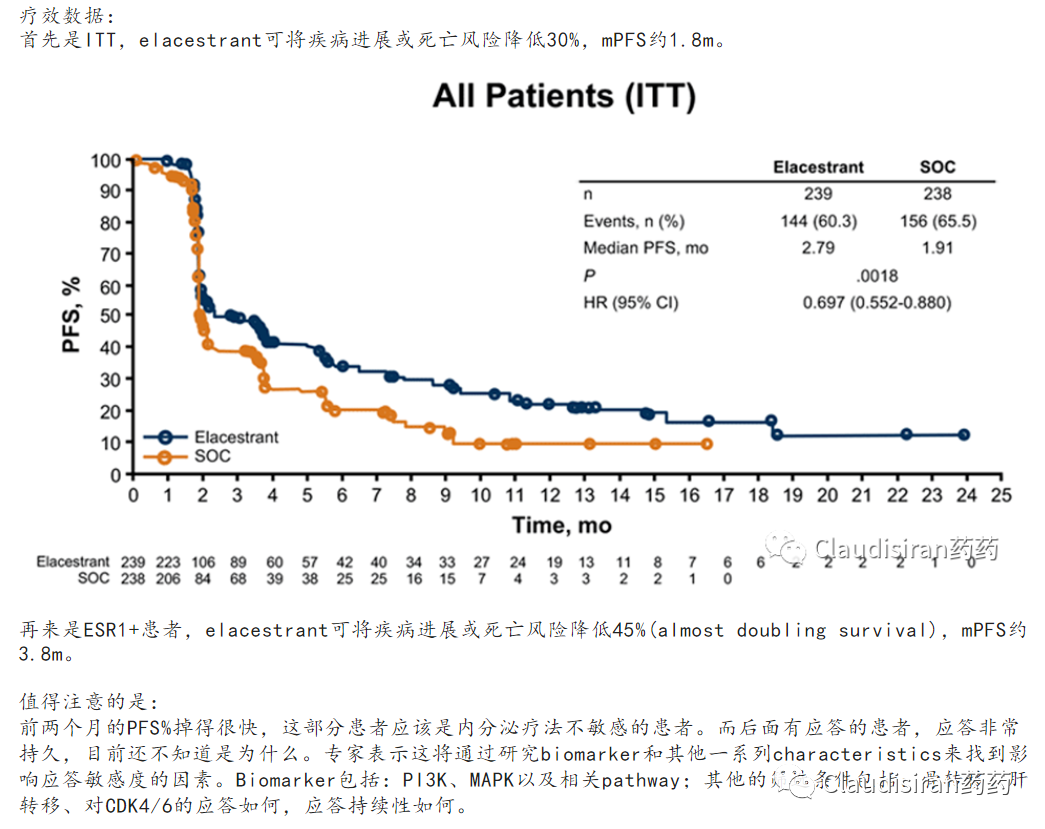
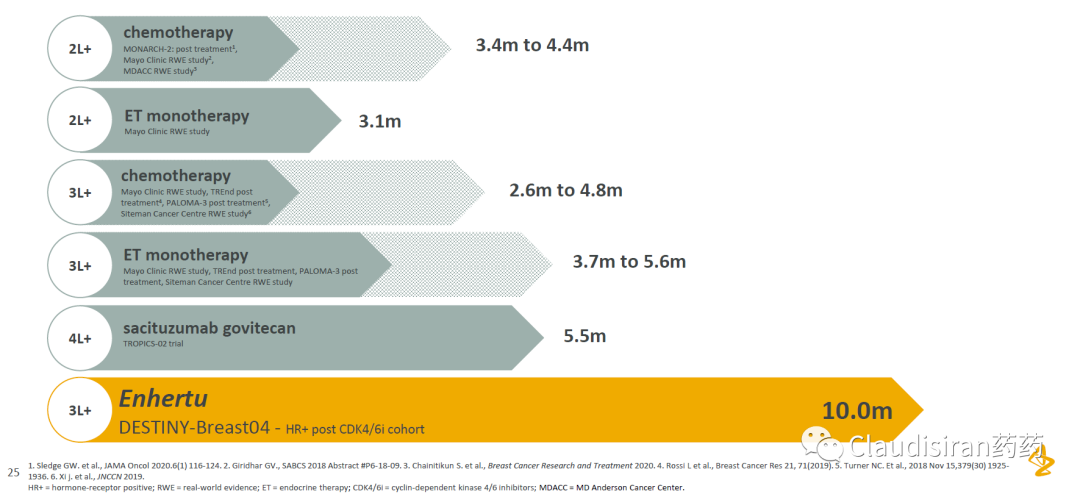
2)吉利德的之前公布的TROPICS-02研究显示Trodelvy(TROP2 ADC)对HR+的患者mPFS只有5.5m,差不多只有T-DXd的一半,不过TROPICS-02是4L+,Destiny-Breast04是3L+。
疗效数据OS:
本来在乳腺癌领域OS做出显著性就比较难,特别是在HER2-群体中更难。
HR+:mOS=23.9m,比chemo多6.4m,HR=0.64,p=0.0028;
HR-/TNBC:mOS=18.2m,比chemo多9.9m,HR=0.48;
ITT:mOS=23.4m,比chemo多6.6m,HR=0.64,p<0.001;
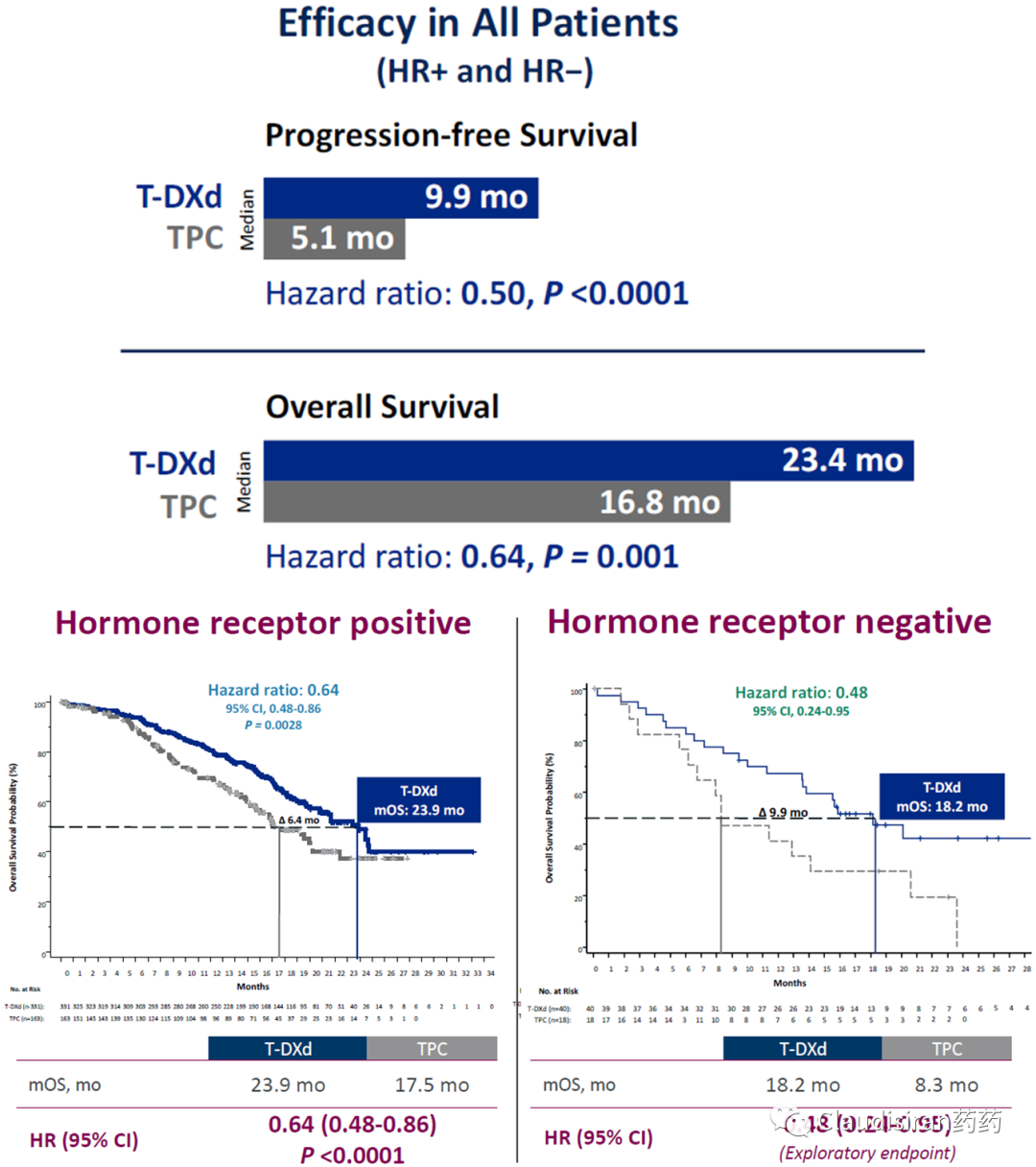
通过以上数据看到了IHC0的希望
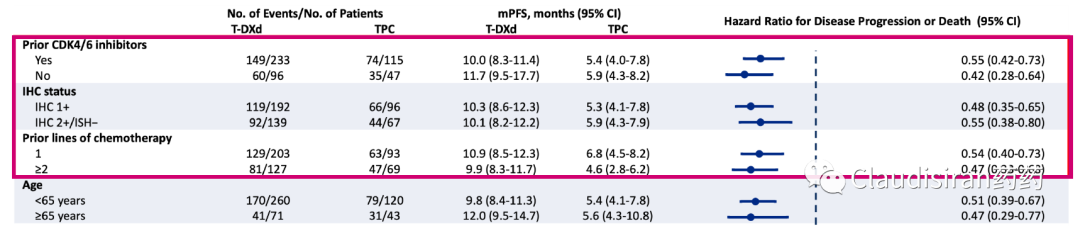
其实不只是HR-status,其他的很多要素,包括之前是否用过CDK4/6、接受过几次化疗、HER2实际表达量、年纪、ECOG、是否转移至其他内脏等等,这些基本上都不影响T-DXd的疗效(大家的疗效都一样好)。
其中IHC1+和IHC2+的hazard ratio非常接近,IHC1+甚至还更小一些,说明HER2的表达量在一定范围内疗效并不会因其下降而减弱T-DXd的疗效。
通过这一点我们似乎可以推断出Destiny-Breast06中 IHC0组或许也能做出显著差异。
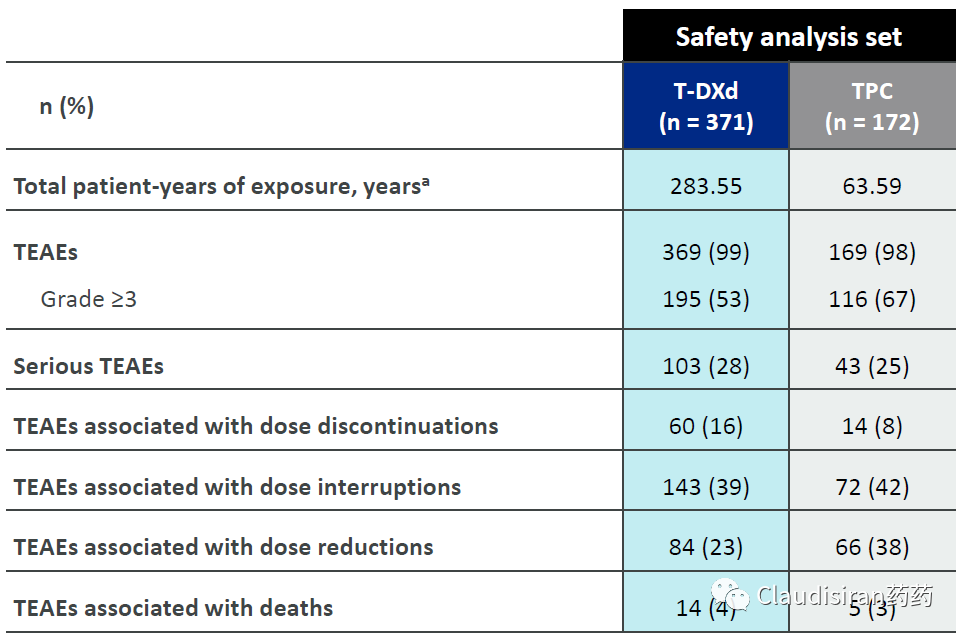
安全性
这次是跟化疗做对照,可想而知靶向性更强的T-DXd耐受性肯定会好很多,T-DXd平均持续用药时间更长,约8个月,而化疗只有3.5个月。
不过T-DXd始终逃不过ILD这个硬伤,大约有8.2%因TEAE导致停药的案例都和ILD有关。
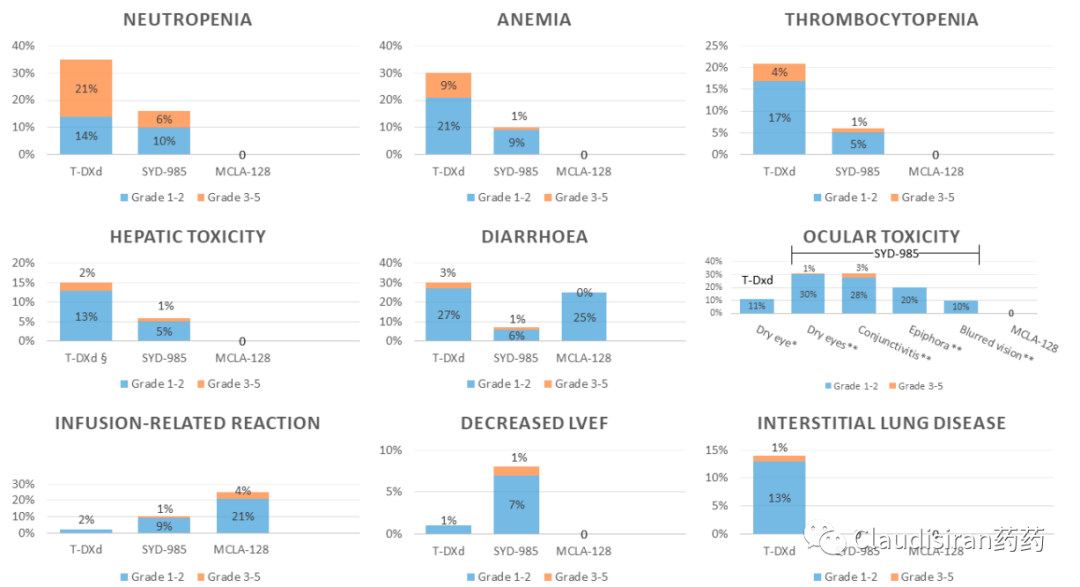
安全性问题会影响早期疗法吗?
如果公司要将T-DXd推向辅助/新辅助/1L等前线疗法,就意味着患者用药时间延长,所有的安全耐受性问题也将被放大,影响“风险获益”比例。
然而让人感到意外的是:专家表示越早治疗,ILD的发生率就越低,一般来说治疗第一年没有发生过ILD,那几乎就是以后也不会发生,所以至少ILD这一点并不会阻止T-DXd往前线推进的步伐。
Enhertu的战略版图
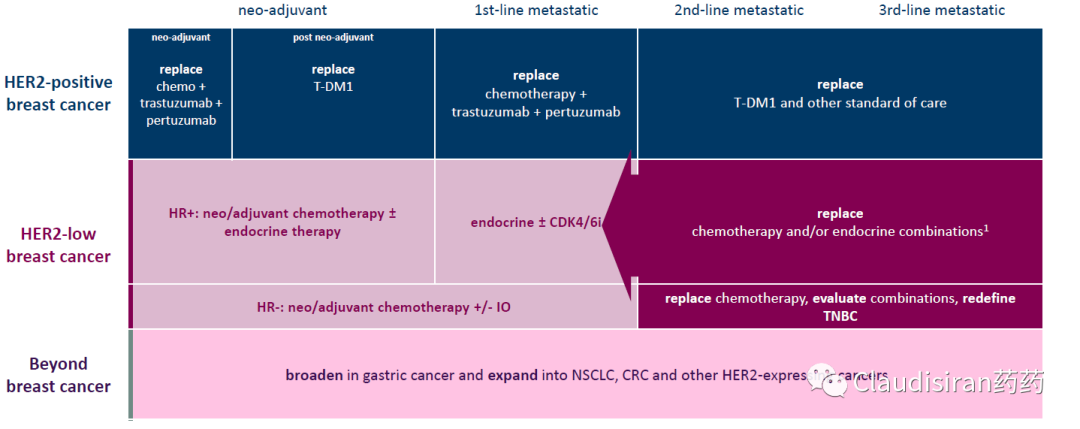
1)HER2+乳腺癌:从新辅助到3L全面替换T-DM1/曲妥珠/帕托珠/化疗成为新的SOC,很重要的一点是现在Destiny-Breast03(去年ESMO公布的研究)已经超过30个月了,T-DXd组的mPFS还没出来(not reached yet);
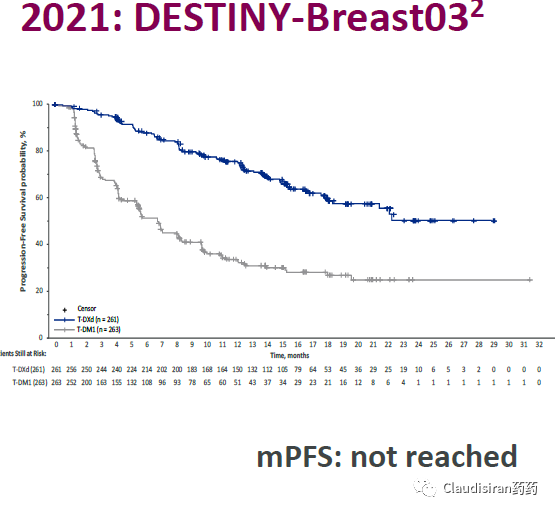
T-DXd雄霸天下?
其实AZ也没有打算完全将其他的HER2品种赶尽杀绝。
2021/3/5,公司开了一个叫Destiny-Breast 09的研究,治疗1L HER2+患者。
该研究一共3个arm:T-Dxd、T-DXd+pertuzumab(HER2+HER3)、SOC chemo,该研究最主要的目的是为了看一看加上pertuzumab是否会带来additional benefit。

2)HER2-low乳腺癌:从3L开始往前推进(约6万患者),先替代化疗,Breast04替代2L化疗,Breast06替代1L化疗;或许以后还可以替代或combo内分泌疗法,是否能够完全替代内分泌疗法还是要看HR的情况,目前考虑内分泌疗法不适用或者耐药/不敏感的患者,ET+CDK4/6患者一年期耐药率大约20~25%,两年后几乎全部耐药,对应患者群体庞大。
3)乳腺癌以外:其他表达HER2的肿瘤,比如GC、NSCLC和CRC等。
Dato-DXd和T-DXd的一大区别
Dato靶向TROP2,T靶向HER2。
HER2这个蛋白基本上跟ADC结合了就会internalize,因此通过HER2的表达量很容易enrich/选择合适的患者群体。
而TROP2在细胞内translate之后又会经过一系列的修饰,导致最终表达在细胞表面的蛋白多多少少不太一样,而抗体特的异性很强,只对其中某一些TROP2蛋白有靶向性,这就是为什么即便用IHC染色测出来的TROP2表达量挺高,但是实际上能被Dato或者其他TROP2 ADC作为靶点,并将其ADC internalize的TROP2蛋白的占比却不高。如果提升剂量,又会影响到身体里其他许多表达TROP2的正常细胞。
因此TROP2 ADC药物的研发,相对HER2 ADC要难一些,需要更多的计算机辅助以及biomarker来精确靶向。
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。





发表评论
注册或登后即可发表评论
登录注册
全部评论(0)