Bringing medical advances from the lab to the clinic.
关键词:遗传性血管性水肿;CRISPR;基因治疗;I-II期;新英格兰医学杂志
2023年11月16日,英国在全球第一个批准了CRISPR疗法(名为exagamglogene autotemcel, exa-cel)上市,用于治疗两种遗传性血液疾病,包括镰状细胞病【1】。2023年12月8日,美国FDA以优先审批的形式评审并批准了exa-cel在美国上市。
这款CRISPR基因编辑疗法由Vertex和CRISPR Therapeutics联合研发。
2024年2月1日,新英格兰医学杂志(NEJM)发表了CRISPR治疗遗传性血管性水肿 (HAE) 的I-II期临床试验结果,这一疗法再次展示了在遗传性疾病中强大的治疗作用。(如需原文,请和healsanq联系,备注20240201NEJM)
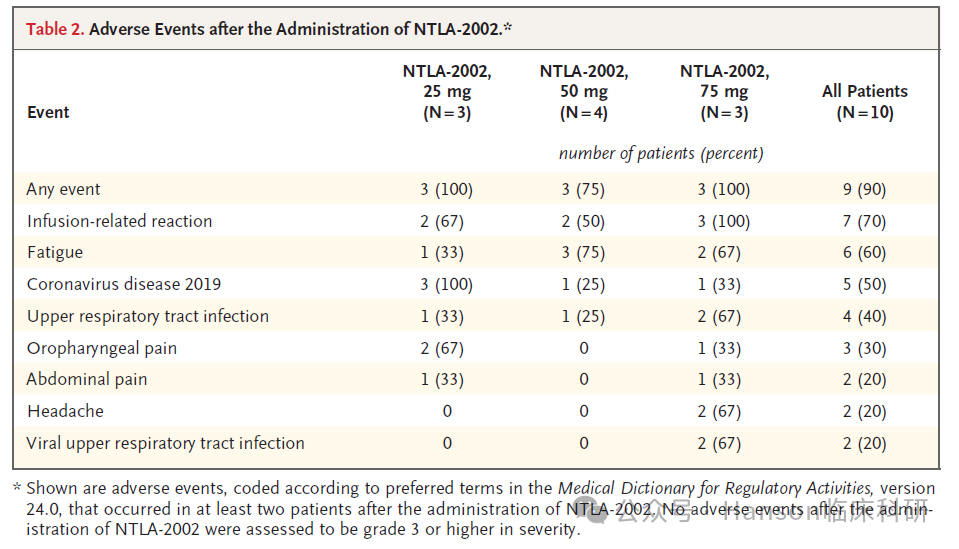
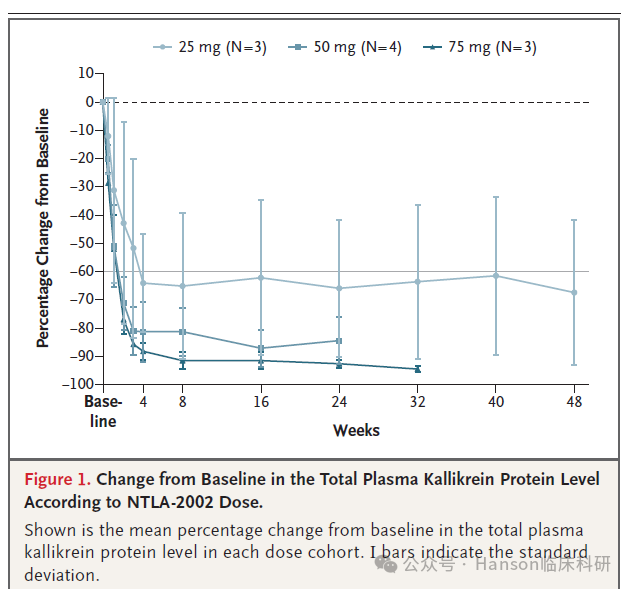
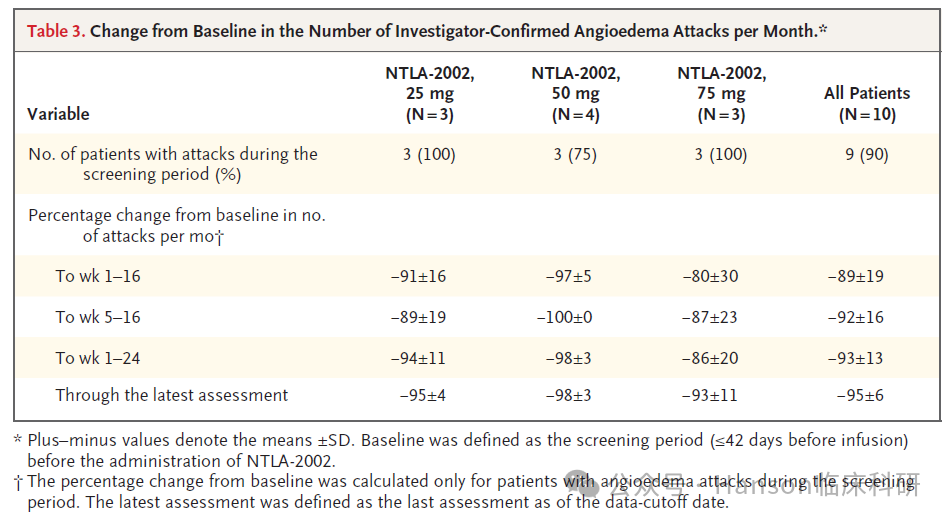
HAE是一种罕见的遗传性疾病,会导致严重的、无法预测的肿胀发作。NTLA-2002 是一种基于 CRISPR-Cas9 的体内基因编辑疗法,旨在通过单次给药即可终身控制血管性水肿发作。该疗法靶向编码激肽原 B1 (KLKB1) 的基因。本研究为一项 I-II 期联合试验的 I 期剂量递增部分,入组了患有 HAE 的成年患者。NTLA-2002 的单剂量分别为 25 mg、50 mg 或 75 mg。主要终点是 NTLA-2002 疗法的安全性和副作用特征。次要和探索性终点包括药代动力学、药效学和临床疗效,根据研究者确认的血管性水肿发作进行评估。共有 3 名患者接受了 25 mg 的 NTLA-2002,4 名患者接受了 50 mg,3 名患者接受了 75 mg。在所有剂量水平下,最常见的副作用是输液相关反应和疲劳。NTLA-2002 给药后未观察到剂量限制性毒性效应、严重不良事件、3 级或更高不良事件或临床重要实验室检查结果。在基线和最新评估之间观察到总血浆激肽原蛋白水平的剂量依赖性降低,25 mg 组的平均百分比变化为 -67%,50 mg 组为 -84%,75 mg 组为 -95% 。在基线和第 1 周至第 16 周(主要观察期)之间,血管性水肿发作次数的平均百分比变化为 25 mg 组为 -91%,50 mg 组为 -97%,75 mg 组为 -80%。在所有患者中,从基线到最新评估的血管性水肿发作次数的平均百分比变化为 -95%。遗传性血管性水肿(Hereditary Angioedema,HAE)是一种罕见的遗传性疾病。目前HAE的治疗主要集中在减少发作的频率和严重性、治疗急性发作以及预防发作。在这项早期临床试验中,应用CRISPR基因编辑的单剂量 NTLA-2002 导致总血浆激肽原水平的强效、剂量依赖性和持久的降低,未观察到严重不良事件。在探索性分析中,观察到所有剂量水平的血管性水肿发作次数均有所减少。本项目由Intellia Therapeutics 研发,由诺贝尔化学奖得主Jennifer Doudna共同创立,目的是开发利用CRISPR/Cas9技术的疗法,用于治疗遗传性疾病和其他条件。我们更关注本研究的主要终点事件涉及及本研究结果的重要科研启发。作为I-II期临床试验,研究的主要终点是不良事件的观察,次要指标观察针对治疗靶点的生物指标变化;结果展示了很好的安全性和与剂量依赖性生物指标降低。同时,次要指标也观察了临床变化。总体均看到了发作次数的显著降低。但因为样本量很小,所以无法观察到剂量依赖性变化。这项研究表明,CRISPR-Cas9 基因编辑技术有可能为包括 HAE 在内的遗传性疾病患者提供一种安全有效的治疗方法;也是临床科研者可以借鉴的重点方向。参考文献:
【1】 Longhurst HJ, et al. CRISPR-Cas9 In Vivo Gene Editing of KLKB1 for Hereditary Angioedema. N Engl J Med. 2024 Feb 1;390(5):432-441. doi: 10.1056/NEJMoa2309149. PMID: 38294975.
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。







发表评论
注册或登后即可发表评论
登录注册
全部评论(0)