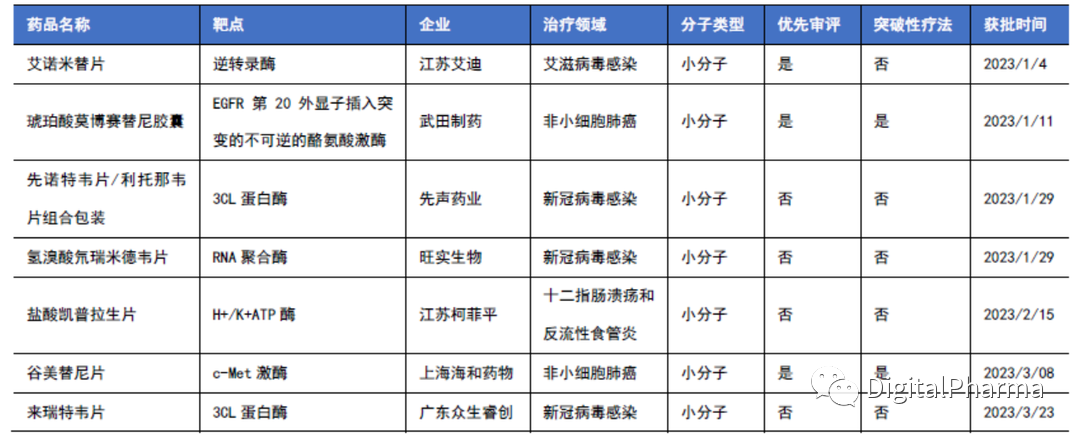
2023年1月1日至3月31日,国家药品监督管理局(NMPA)共批准7款1类创新药(不含中药和疫苗)。从治疗领域看,新冠病毒感染用药获批数量居多,占比42.86%,其次是抗肿瘤药;从分子类型看,2023年第一季度批准的1类创新药均为小分子药物。艾诺米替片、琥珀酸莫博赛替尼胶囊和谷美替尼片3款产品为优先审评品种;同时琥珀酸莫博赛替尼胶囊和谷美替尼片2款产品获国家药品监督管理局药品审评中心(CDE)突破性疗法认定。2023年1季度没有中药新药获批上市。
表 1 2023年1季度NMPA批准的1类创新药
2月10日,国家药监局发布《中药注册管理专门规定》,自2023年7月1日起施行。《专门规定》共11章82条措施。第一章总则,第二章中药注册分类与上市审批,第三章人用经验证据的合理应用,第四章中药创新药,第五章中药改良型新药,第六章古代经典名方中药复方制剂,第七章同名同方药,第八章上市后变更,第九章中药注册标准,第十章药品名称和说明书,第十一章附则。
《专门规定》与新修订《药品管理法》《药品注册管理办法》有机衔接,在药品注册管理通用性规定的基础上,对中药研发相关要求进一步细化,加强中药新药研发与注册管理。《专门规定》充分吸纳药品审评审批制度改革成熟经验,并结合疫情防控中药成果转化实践,借鉴国内外药品监管科学研究成果,构建中药注册管理体系,有望进一步加快中药新药审评审批。
全方位、系统的中药注册管理体系对中医药行业持续规范升级将产生积极推动作用,有望促进行业长期高质量发展。中药创新审评政策逐渐清晰,利好具备产业链及研发管线优势的行业龙头,将极大激发中药新药研发的热情。同时催生中药研发的CRO服务需求,带来中药CRO发展新契机。
CDE颁布24项技术指导原则,弥补国内技术指导原则体系缺口
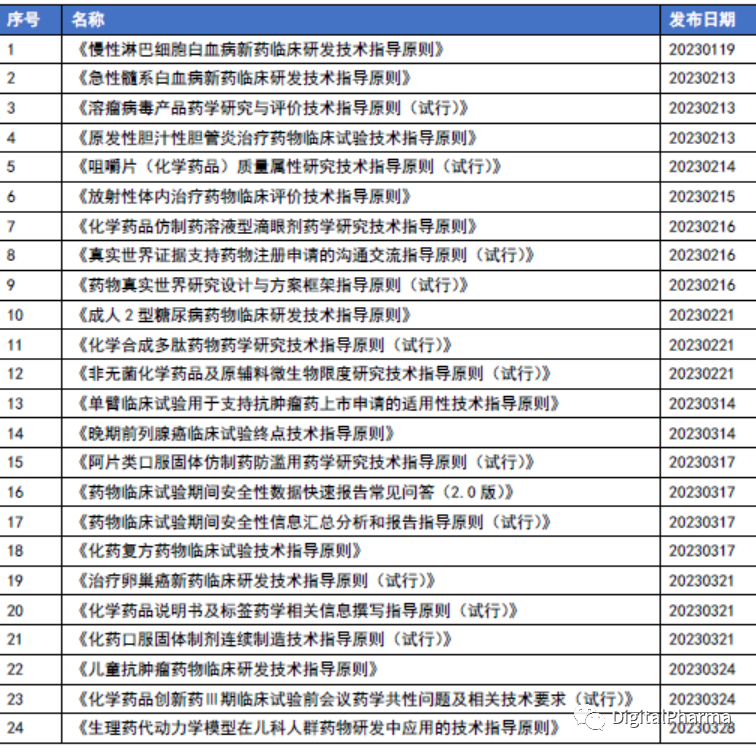
2023年1季度,国家药监局药品审评中心(CDE)陆续发布实施了24个药品注册技术指导原则,其中涵盖慢性淋巴细胞白血病新药、急性髓系白血病新药、溶瘤病毒产品、儿童抗肿瘤药物等。
表 2 2023年1季度CDE颁布的指导原则
来源:岐正医药网



发表评论
注册或登后即可发表评论
登录注册
全部评论(0)