2023-04-04 来源 : IO笔记
一、美国已上市11个免疫检查点抑制剂药物获批汇总
截至2023年3月底,美国FDA批准了5个PD-1单抗,3个PD-L1单抗;另外获批2个CTLA-4单抗,1个LAG-3单抗,共合计11个免疫检查点抑制剂。

不同免疫药物获批癌肿汇总:

附:

| 2023年3月22日,美国食品药品监督管理局(FDA)准许加速批准 retifanlimab-dlwr (商品名:Zynyz,厂家:Incyte Corporation) 用于治疗转移性或复发性局部晚期的 Merkel细胞癌(MCC)成人患者。 retifanlimab-dlwr (音译为:瑞替芬林单抗)是一种靶向程序性死亡受体-1(PD-1)的人源化单克隆抗体(单抗)。 剂量和给药: ZYNYZ的推荐剂量为500mg,每4周静脉滴注30分钟。 该适应症的加速批准是基于缓解率(ORR)和缓解持续时间(DoR)。 该适应症的获批基于 PODIUM-201 (NCT03599713) 研究的安全性和有效性数据。PODIUM-201 (NCT03599713) 研究是一项开放性、多地区、单臂的临床试验,评估人群为 65名既往在晚期阶段未经系统治疗的转移性或复发性局部晚期的 MCC 患者。 主要的疗效结局指标是客观缓解率(ORR)和缓解持续时间(DOR),由独立评估评估委员会按照 RECIST v1.1标准评估。 客观缓解率(ORR)为 52% (95% CI: 40, 65),完全缓解(CR)率为 18%。6个月及以上的 DOR率为 76%,12个月及以上的 DOR率为 62%。 安全性评估人群包含了 105名 MCC 患者。最常见 (≥10%)的不良反应是疲劳、肌肉骨骼疼痛、皮疹、腹泻、皮疹、发热和恶心。 出处:ZYNYZ完整药品说明书信息: https://www.accessdata.fda.gov/drugsatfda_docs/label/2023/761334s000lbl.pdf 备注: MCC是一种罕见且具有侵袭性的皮肤癌症,经常出现在头部、颈部和手臂暴露于阳光下的皮肤上,表现为一个单一的、无痛的红紫色皮肤结节。MCC生长迅速,转移性疾病发生率高,导致预后不良。患有远处转移性疾病的MCC患者的五年总生存率估计为14%。在美国,每10万人中就有不到1人患有MCC,但发病率正在迅速上升,尤其是在65岁以上的成年人中。 |
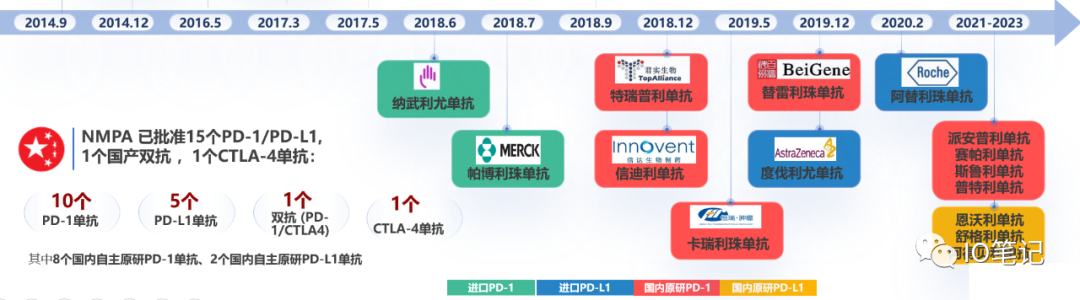
二、中国已上获批上市的17个免疫检查点抑制剂:
包含8个国内原研PD-1单抗、3个国内自主PD-L1单抗,1个国产双抗 (PD-1/CTLA4);
进口2个PD-1,进口2个PD-L1,进口1个CTLA-4.
其中纳入2023年国家医保的为4个,分别为:
特瑞普利单抗(君实)、信迪利单抗(信达)、卡瑞利珠单抗(恒瑞)、替雷利珠单抗(百济),备注在上图中:红色标记为纳入国内医保的适应症(君实3个、信达6个、百济9个、恒瑞8个)有效期:2023年3月1日至2023年12月31日。
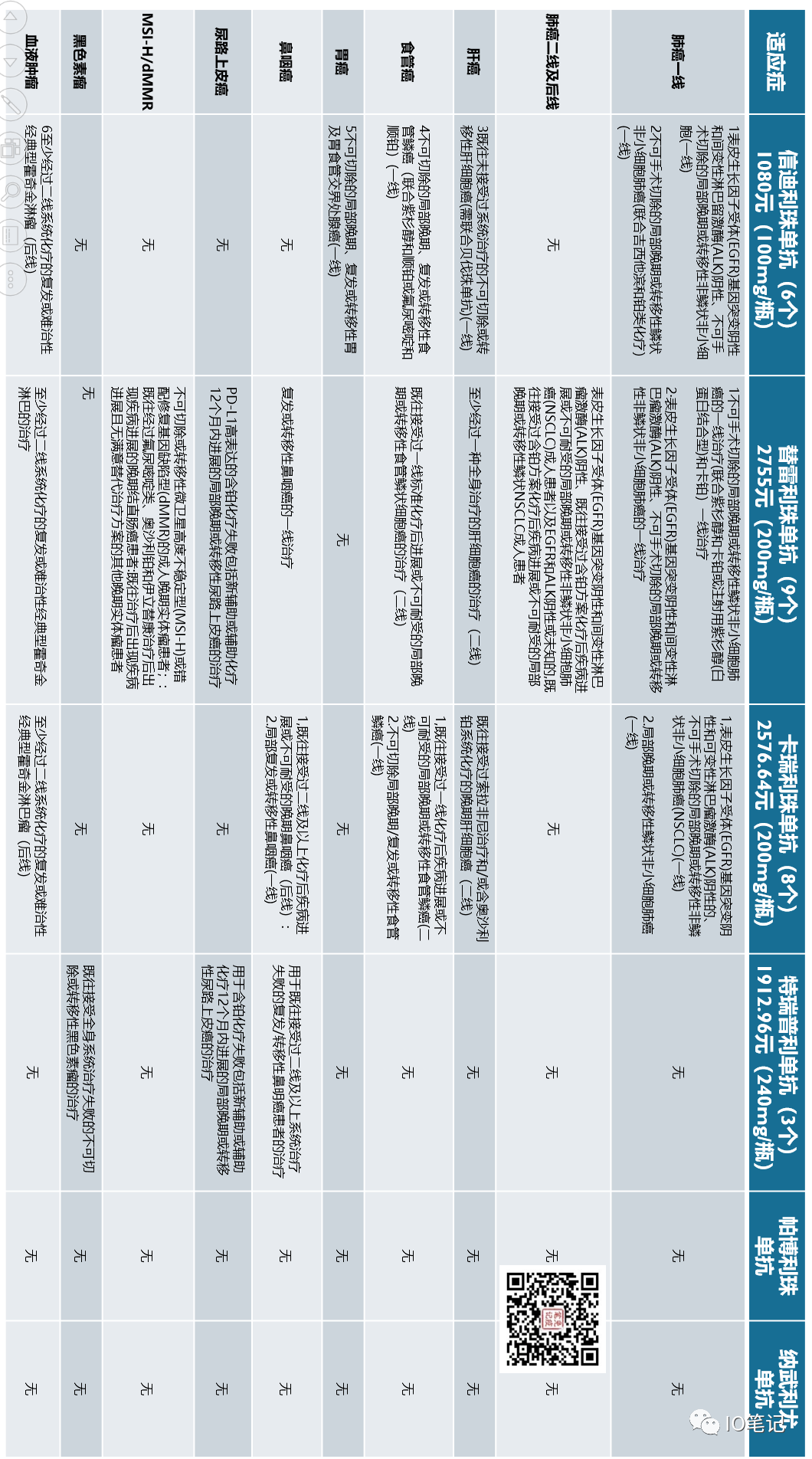
4款PD-1单抗2023医保谈判后价格分别为:
信迪利单抗:1080元(100mg/瓶)
特瑞普利单抗:1912.96元(240mg/瓶)
替雷利珠单抗:2755元(200mg/瓶)
卡瑞利珠单抗:2576.64元(200mg/瓶)
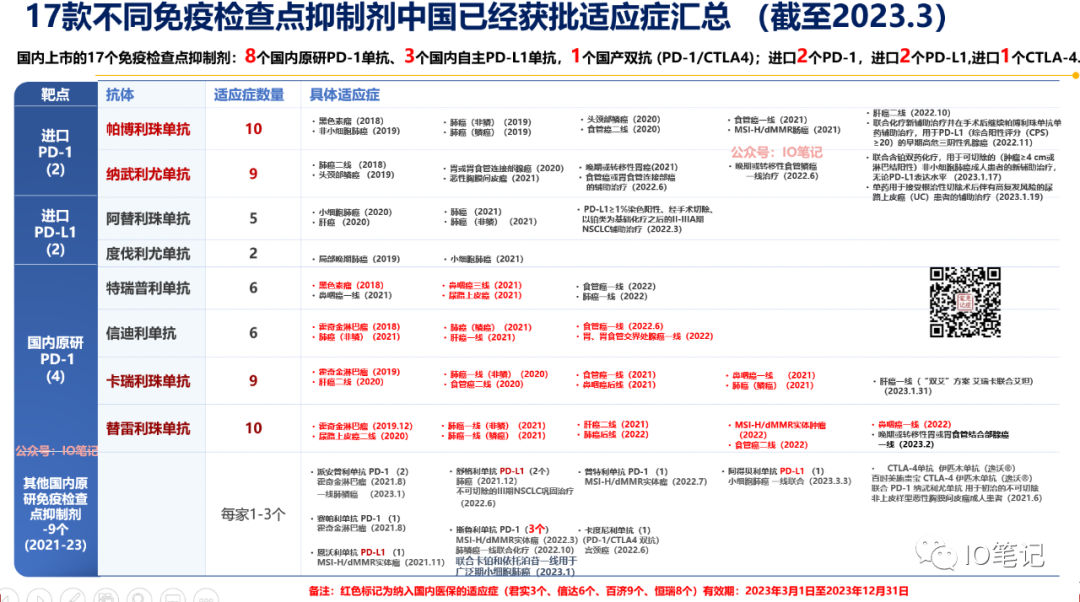
医保适应症详见下图:

1.1非小细胞肺癌免疫治疗竞争格局

1.12小细胞肺癌免疫治疗竞争格局

附:
3.国内已上获批市ADC药物汇总:
截至2023年2月,全球共有15款获批上市的ADC药物。

其中,中国获批上市的ADC药物有6个,分别是罗氏的恩美曲妥珠单抗(T-DM1)、Seagen/武田的维布妥昔单抗、辉瑞的奥加伊妥珠单抗、荣昌生物的维迪西妥单抗和Immunomedics的戈沙妥珠单抗、阿斯利康和第一三共联合开发和商业化的优赫得®(英文商品名:Enhertu® 代号DS-8201,通用名:注射用德曲妥珠单抗)(2023.2.24国内首获批)。
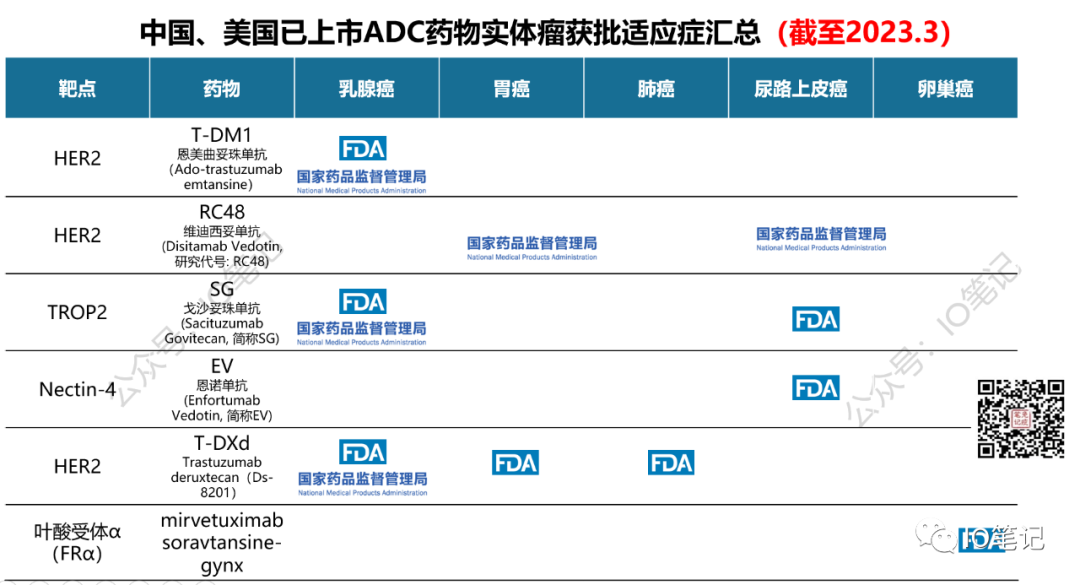
原先国内只有荣昌生物一个国产HER2 ADC上市,目前DS-8201(HER2 ADC)已经上市。经医保谈判后,2023医保目录内新增了2款进口ADC,分别来自武田与罗氏。
盘点ADC新药中国、美国已获批适应症汇总(截至2023.2)
荣昌生物/维迪西妥单抗(RC48):
维迪西妥单抗是我国首个自研的HER2 ADC药物,最新医保适应症为:至少接受过2种系统化疗的HER2过表达局部晚期或转移性胃癌患者;用于既往接受过含铂化疗且HER2过表达局部晚期或转移性尿路上皮癌。谈判价格从13500元降至3800元(2023年医保价),降幅高达71.85%。
武田/维布妥昔单抗:
维布妥昔单抗2020年5月14日在中国获批上市,是全球首个以CD30为靶点的ADC药物。此前该药的定价为18680元/50mg/瓶(仅供参考),2023年谈判后具体价格尚未公布。
罗氏/恩美曲妥珠单抗:
恩美曲妥珠单抗(T-DM1)于2013年获FDA批准上市,这也是中国批准上市的首个ADC药物,于2020年1月21日正式获批上市。2023年谈判后具体价格尚未公布。医保前价格为9200元/100mg(仅供参考)。2023年谈判后具体价格尚未公布。
附:中英文对照 (全球已获批上市24个免疫检查点抑制剂,截至2023年3月)
4、双抗获批药物、适应症
| 汇总常见24个免疫药物名称中英文对照表,方便日常英文文献资料等检索使用。 |

美国FDA批准(11个): pembrolizumab 帕博利珠单抗(Merck & Co., In) nivolumab 纳武利尤单抗(Bristol-Myers Squibb) atezolizumab 阿替利珠单抗 罗氏 (Roche Holding AG) (PD-L1单抗) durvalumab 度伐利尤单抗或德瓦鲁单抗Imfinzi ( astrazeneca) (PD-L1单抗) avelumab 阿维鲁单抗(BAVENCIO)辉瑞(Pfizer Inc) cemiplimab 西米普利单抗 生产厂家:赛诺菲&再生元 LIBTAYO dostarlimab 多塔利单抗 GSK(GlaxoSmithKline PLC) retifanlimab-dlwr (音译为:瑞替芬林单抗) (商品名:Zynyz,厂家:Incyte Corporation) 备注:以上未标注的为PD-1单抗 CTLA-4/Lag-3抑制剂: ipilimumab 伊匹木单抗 (CTLA-4)全人源化单克隆抗(Bristol-Myers Squibb) tremelimumab 曲美木单抗 CTLA-4)全人源化单克隆抗( astrazeneca) relatlimab + nivolumab, Lag-3抑制剂(Bristol-Myers Squibb) |

| 国内自主研发上市免疫药物(12个): camrelizumab 卡瑞利珠单抗 恒瑞 sintilimab 信迪利单抗 信达 tislelizumab 替雷利珠单抗 百济 toripalimab 特瑞普利单抗 君实 penpulimab 派安普利单抗(AK105)康方 cadonilimab 卡度尼利单抗,研发代号:(AK104)PD-1/CTLA-4双抗 康方 serplulimab 斯鲁利单抗 复宏汉霖 sugemalimab 舒格利单抗 基石(PD-L1单抗) envafolimab 恩沃利单抗 康宁杰瑞/思路迪 (PD-L1单抗) zimberelimab 赛帕利单抗 誉衡生物 pucotenlimab 普特利单抗 乐普生物 Adebrelimab 阿得贝利单抗 恒瑞 (PD-L1单抗) 备注:以上未标注的为PD-1单抗 |
俄罗斯(1个): prolgolimab :2020年4月,俄罗斯本土开发的PD-1抑制剂Forteca(INN:prolgolimab)获得了俄罗斯卫生部批准上市,用于治疗最具侵袭性的癌症之一:无法手术切除的或转移性黑色素瘤。 |
| 按照首个英文字母顺序排列(共计24个,中国,美国23个;俄罗斯1个): Adebrelimab 阿得贝利单抗 恒瑞 (PD-L1单抗) atezolizumab 阿替利珠单抗 罗氏 avelumab 阿维鲁单抗,辉瑞 cadonilimab 卡度尼利单抗,PD-1和CTLA-4双抗 camrelizumab 卡瑞利珠单抗 恒瑞 cemiplimab 西米普利单抗 赛诺菲&再生元 dostarlimab 多塔利单抗 GSK durvalumab 度伐利尤单抗或德瓦鲁单抗 envafolimab 恩沃利单抗 康宁杰瑞/思路迪 ipilimumab 伊匹木单抗 (CTLA-4) nivolumab 纳武利尤单抗 pembrolizumab 帕博利珠单抗 penpulimab 派安普利单抗康方 prolgolimab 俄罗斯本土开发PD-1抑制剂 pucotenlimab 普特利单抗 乐普生物. relatlimab + nivolumab, Lag-3抑制剂 retifanlimab-dlwr (音译为:瑞替芬林单抗) (商品名:Zynyz,厂家:Incyte Corporation) serplulimab 斯鲁利单抗 sintilimab 信迪利单抗 sugemalimab 舒格利单抗 tislelizumab 替雷利珠单抗 toripalimab 特瑞普利单抗 tremelimumab 曲美木单抗 (CTLA-4) zimberelimab 赛帕利单抗 备注: 2020年4月,俄罗斯本土开发的PD-1抑制剂Forteca(INN:prolgolimab)获得了俄罗斯卫生部批准上市,用于治疗最具侵袭性的癌症之一:无法手术切除的或转移性黑色素瘤。 |
附:


版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。





发表评论
注册或登后即可发表评论
登录注册
全部评论(0)