2023-07-21 来源 : VIP说
介绍
肝内胆管癌(ICC)是一种致命的恶性肿瘤,其发病率在原发性肝癌中位列第2。在过去的十年中,该病的发病率上升了140%。ICC占所有肝脏恶性肿瘤的20%,占所有胃肠道恶性肿瘤的3%。
已确定的ICC危险因素包括纤维多囊性肝脏疾病(如胆总管囊肿)、原发硬化性胆管炎、肝胆管结石、肝硬化、病毒性肝炎、寄生虫感染(如后睾吸虫、华支睾吸虫)、肥胖相关脂肪性肝炎、糖尿病和致癌物暴露(如亚硝胺、钍造影剂、铁过剩)以及至少四种已知的遗传病症,包括林奇综合征、BRCA 相关蛋白-1 (BAP-1) 肿瘤易感综合征、囊性纤维化和胆管乳头状瘤病。
然而,在大多数诊断为胆管癌的患者中未发现明显的诱发因素。
ICC患者5年总生存率 (OS)仅 9%左右,大多数患者在就诊时已处于晚期,即使在早期发现,微小的肿瘤也可能因其位于肝脏中难以接近的位置或具有高度结缔组织增生性或少细胞性,而限制了诊断方法的应用。
手术切除仍是ICC唯一可能治愈的方法,但仅20%-30%的患者存在手术切除的机会,其术后5年OS率仅20%-35%,术后局部和远处复发成为ICC术后患者的生存阻碍。
相关数据显示,术后使用卡培他滨辅助治疗,中位生存期为53个月;相比之下,接受姑息性化疗的无法切除的ICC患者的中位生存期仅为11.7个月;
而对于晚期患者,吉西他滨(Gem)和顺铂(Cis)联合化疗被认为是最有效的一线方案。

近期三联方案和免疫疗法的使用可能会改变目前的治疗现状。
靶向治疗方面,异柠檬酸脱氢酶 (IDH) 和成纤维细胞生长因子受体 (FGFR) 突变超过40%的患者可进行靶向治疗,但几个月内会逐渐耐药,患者的存活率仍然很低。
Holster等人还开发了结合全身和局部治疗的新兴策略,如经动脉放射栓塞或肝动脉输注 (HAI)等(图1)。
本文重点关注ICC当前和未来的治疗策略,最终可用于针对ICC患者的个性化和多学科的治疗的指导。
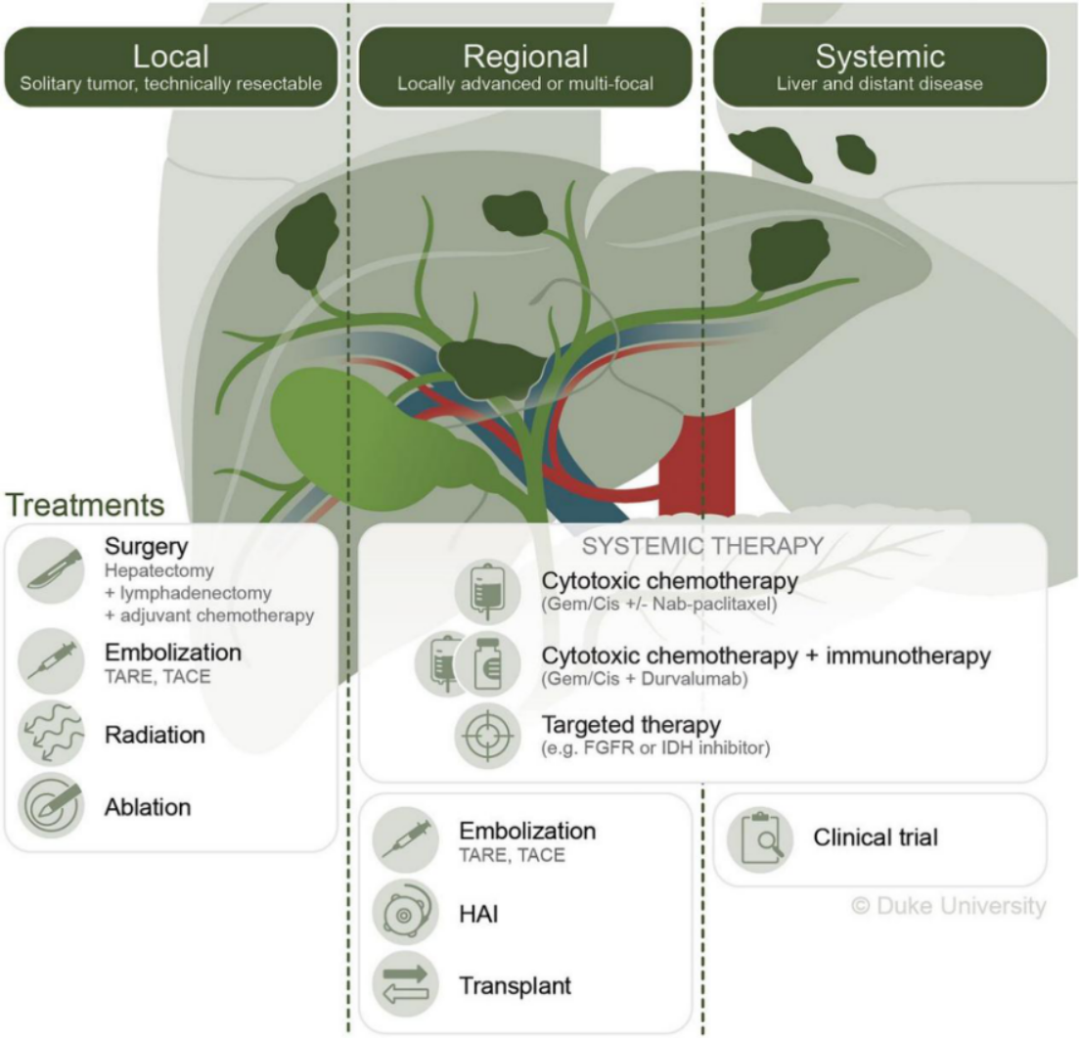
ICC的治疗管理
ICC的治疗通常取决于患者特异性和肿瘤特异性因素,包括年龄、体能状态、患者肝脏的潜在健康状况以及疾病的程度(孤立和局部可切除与局部不可切除与转移)。
理想情况下由多学科专家团队做出治疗决策,该团队评定患者进行手术切除、围手术期化疗、肝脏定向治疗、移植和全身治疗,包括细胞毒性治疗、靶向治疗和/或免疫疗法。
以下各部分详细回顾了每种治疗方式的治疗注意事项及数据(图 2)。
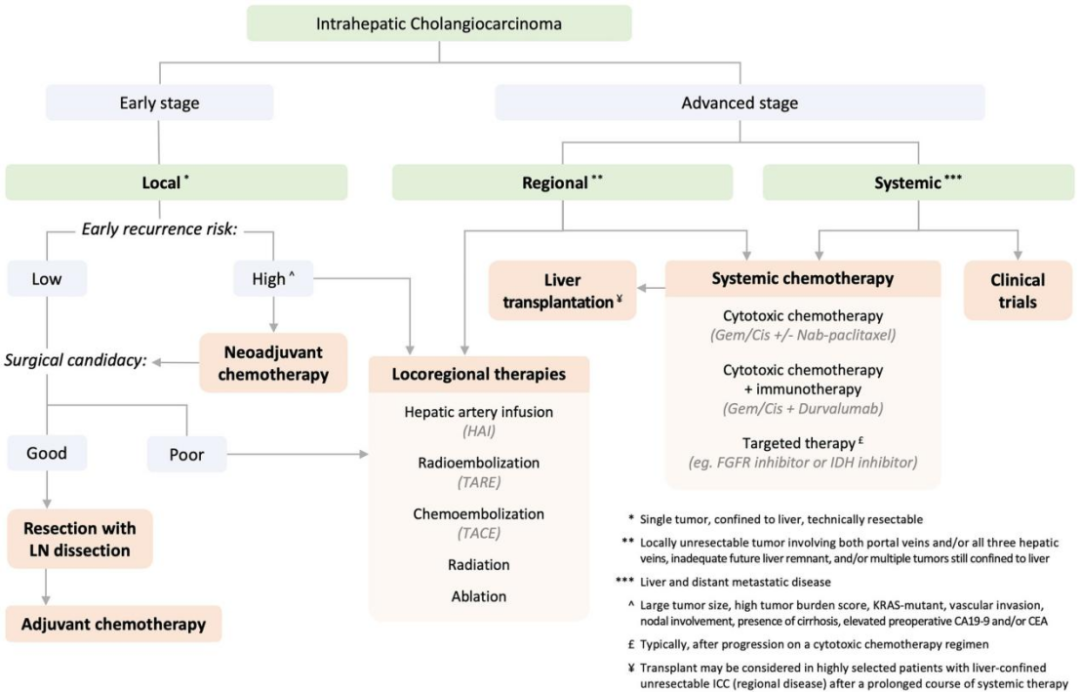
手术切除和淋巴结清扫在早期ICC患者中的作用
手术切除是ICC的主要治疗方法。在238名ICC患者的系列研究中,54%的患者在就诊时被认为不可切除,最常见的原因是肝部多处病灶 (54%)、局部不可切除肿瘤 (29%) 和远处转移 (13%)。
在以治愈为目的剩余患者中,30%被确定为在手术室无法切除,最常见的原因是检测到多发性肝肿瘤 (33%)、淋巴结或腹膜转移 (64%) 或局部晚期 (12 %)。
其中,32%的患者最终接受了切除术,mOS为36个月,而无法切除的患者仅为9个月。切除术可能会产生长达34个月的中位无病生存期。
手术的目标是实现显微镜下切除边缘无病灶 (R0),76%-92%的患者可实现。手术边缘状态与患者的远期生存相关,并与其他癌症的切除术一致。
在无淋巴结转移 (N0) 的患者中,显微镜下阳性 (R1) 切除是生存率低的独立预测因子([OR] 9.6;95% [CI],4.5-20.4)。
在淋巴结阳性患者中,R0和R1切除后的生存期相似(中位数分别为18个月和13个月;p=0 .1)。
此外,中位生存期与切缘宽度相关(≤1毫米,15个月;2-4毫米,36个月;5-9毫米,57个月;≥10毫米,64个月;p <0 .001),并且它证明边缘 >5 mm是生存的独立预测因子(OR,2.22;95% CI,1.59–3.09)。
然而由于局部解剖因素,并不是经常可以获得理想的宽切缘。淋巴结清扫术在减少ICC患者局部复发和提高生存率方面的作用仍存在争议。
尽管淋巴结是否受累是一个重要的预后因素,但淋巴结切除术似乎并没有提供治疗获益,尤其是在有大血管侵犯、术前CEA水平>5.0 IU/ml以及肝十二指肠韧带以外的淋巴结转移的患者中。
一项多中心研究表明淋巴结转移与更差的结果相关(中位生存期,N0为30个月,N1为24个月;p =0 .03 ) 。
淋巴结切除术重要作用是有助于对患者进行准确分期,从而改善疾病复发和死亡率的风险分层。
AJCC和NCCN推荐淋巴结清扫术,包括肝门和胰头之间的肝十二指肠韧带内的所有纤维脂肪和淋巴组织,至少6个淋巴结。
在肝切除术期间对ICC患者相关操作与所有患有胆道恶性肿瘤的患者一致。淋巴结清扫术应包括第8组(肝总动脉)和第12组(肝十二指肠韧带)淋巴结,约82%的淋巴结转移出现在这些部位。
研究显示,仅50%的ICC患者在肝切除术期间常规进行淋巴结清扫术。手术切除后的5年OS率在11%到40%之间,淋巴结阴性且完全切除(R0)的患者的5年生存率高达63%,但仍会复发,复发的模式不可预测。
肝内复发最常见(约60%),尤其是在淋巴结受累的患者中。多中心研究的列线图最近已被用于改进接受切除术ICC患者的预后分层,并可能确定哪些患者的复发风险较高,和可能受益于新辅助和/或辅助治疗。

这些列线图结合了临床病理学和实验室数据,包括肿瘤大小、多灶性、肿瘤负荷评分、KRAS状态、血管侵犯、淋巴结受累、肝硬化的存在以及术前血清肿瘤标志物水平。
此类列线图受到样本量小、机构实践差异和选择偏倚的限制,它们并未常规用于ICC患者的临床决策制定。
ICC切除术后辅助化疗

ICC患者切除术后进行辅助治疗的研究很少,通常会包括胆囊癌和其他胆道癌患者。
PRODIGE 12–ACCORD18研究(ClinicalTrials.gov标识符NCT01313377)是一项多中心、开放标签、3期随机临床试验,包括来自法国多个中心的196名接受R0或R1切除术的胆道恶性肿瘤患者。

患者被随机分配接受Gem和奥沙利铂辅助化疗(GEMOX)或仅接受监测。该试验的中位随访时间为46.5个月(95% CI,42.6-49.3个月),但未显示无复发生存期有任何统计学意义(GEMOX组中位时间为30.4个月),而监测组为18.5个月;
HR,0.88;95% CI,0.62-1.25;p= 0.48)或OS(中位数,GEMOX组为75.8个月,而监测组为50.8个月;HR,1.08;95% CI,0.70-1.66;p= 0.74)。
BILCAP试验(NCT03779035)是来自英国的一项3期、随机、多中心试验,包括447名胆道恶性肿瘤患者。在该研究中,患者被随机分配接受卡培他滨或不接受辅助治疗。

所有患者的中位随访时间为60个月(IQR,37-60个月)。尽管意向治疗分析未显示任何统计学上的显着差异,但针对各种因素(淋巴结状态、分级和性别)进行调整的方案指定的敏感性分析确实导致OS HR为0.71,95% CI , 0.55-0.92;p=0.01。
在预先设定的符合方案分析中(卡培他滨组210名患者和观察组220名患者),卡培他滨组的中位OS为53个月(对比36个月;
调整后的 HR,0.75;95% CI,0.58-0.97;p=0 .028),中位无复发生存期为25.9个月(对比17.4个月;调整后的HR,0.70;95% CI,0.54-0.92;p= 0.0093)。

Bridgewater 等人于2022年报告了该研究的长期随访,证实了这些结果。根据BILCAP试验,卡培他滨辅助治疗6个月已成为ICC切除术患者的标准治疗,且无论切缘或淋巴结状态如何。
进一步验证辅助治疗益处的其他临床试验正在进行中。ACTICCA-1研究(NCT02170090)是一项国际、随机、3期试验,在胆道癌切除患者中比较Gem和Cis的组合与单独使用研究。

日本临床肿瘤学研究组JCOG1202研究是一项开放标签、多中心、随机3期试验,旨在确认S-1辅助化疗可延长已切除胆道癌患者的OS。
其他辅助临床试验包括一项3期随机试验,比较GEMOX与卡培他滨在接受ICC治愈性切除术的患者中的疗效以及评估ICC切除后使用白蛋白结合 (nab)-紫杉醇和Gem联合治疗的安全性和有效性的2期研究。
可切除ICC患者的新辅助化疗
可切除ICC新辅助治疗的基本依据可能包括根除微转移性病灶以降低早期复发的风险;通过识别早期进展的患者来改进患者治疗选择;降低原发肿瘤大小以促进达到R0切除。
尽管有这些理论上的好处,但尚不清楚在新辅助化疗后接受手术切除的患者的生存期是否优于接受前期手术的可切除肿瘤患者。
一项回顾性研究表明,在I-III期ICC患者中,与前期手术切除后辅助化疗相比,新辅助化疗与更长的OS相关(40.3个月与32.8个月;p =0 .01)。
另一项超过4000名患者的队列研究在倾向性匹配后表明,与前期手术相比,新辅助治疗可使死亡风险降低23%。
尽管回顾性系列研究存在固有偏倚和局限性,但这些研究表明新辅助化疗的潜在优势。

在2022年美国临床肿瘤学会年会上报告一项2期单臂试验(NEO-GAP;NCT03579771),评估了Gem、Cis和白蛋白结合型紫杉醇作为新辅助化疗对30名IB-IIIB期ICC患者的疗效。
主要结果指标为完成所有术前和手术治疗患者情况及不良事件的发生率,结果显示:23名患者 (77%) 完成了所有术前化疗并接受了根治性手术切除。
其中10名患者 (33%) 经历了≥3级与治疗相关的不良事件,最常见的是中性粒细胞减少和腹泻,没有治疗相关的死亡数据,疾病控制率 (DCR) 为90%(部分反应为23%;疾病稳定为67%;疾病进展为10%)。

其他正在进行的试验包括一项单中心2期试验(NCT03603834),拟评估改良FOLFOXIRI(氟尿嘧啶、亚叶酸、伊立替康和奥沙利铂的组合)对临界可切除胆管癌 (ICC/pCC/dCC) 的疗效,通过MRI或CT评估的总体反应率。
GAIN试验( NCT03823404)是一项多中心、随机、对照、开放标签的3期研究,患者接受围手术期化疗(Gem加顺式;三循环术前和术后)或单独手术。
随后进行术者选择的治疗,主要终点是OS,次要终点是无进展生存期(PFS)、R0切除率、毒性、围手术期发病率、死亡率和生活质量。

最后一项为FGFR2融合肝内胆管癌的OPT-IC试验(NCT03579771),研究对可切除的ICC患者将使用ctDNA进行分子分析,然后进行一个周期的 Gem、Cis 和白蛋白结合型紫杉醇治疗,
具有FGFR2融合的患者将继续接受两个周期的FGFR2抑制剂,然后进行手术和辅助治疗,而没有FGFR2融合的患者将接受另外两个周期的化疗,然后进行手术和辅助治疗,可行性将作为研究的主要结果,反应和无复发生存作为次要结果。
局限于肝脏、不可切除的ICC的局部治疗
对于晚期、局限于肝脏、不可切除的ICC患者,由于技术因素、生物学因素或患者特异性因素,切除术不可行,临床已经应用了各种局部区域治疗技术,包括经动脉化疗栓塞术 (TACE)、经动脉放射栓塞术 (TARE)、HAI、热消融和外照射放疗。
不可切除的局限于肝脏的ICC的经动脉栓塞治疗
经动脉栓塞疗法是基于肝脏双重血液供应的特性实现肿瘤控制。肝肿瘤几乎全部血液供应来自肝动脉系统,而肝实质的主要血液供应来自门静脉和肝动脉系统。
因此,将任何颗粒物质输注到肿瘤的肝动脉供应中会导致在肿瘤中的蓄积明显高于在正常实质中的蓄积,从而优化抗肿瘤作用并使肝脏和全身毒性最小化。
用于治疗胆管癌的经动脉栓塞疗法包括TACE和TARE。TACE使用化疗剂与乙碘化油的乳液(常规TACE)或与化疗剂结合的特殊颗粒(药物洗脱珠;DEB-TACE)进行。
所用化疗的选择存在显着异质性,TACE与顺铂、多柔比星、丝裂霉素、伊立替康或这些药物的组合的研究报告的客观缓解率 (ORR) 范围为10%至50%,中位生存期为12-20个月。
在最近的一项比较Gem/Cis与 Gem/Cis加DEB-TACE和伊立替康的随机试验中,联合治疗组表现出显着改善的PFS(31.9与 10.1个月)和 OS(33.7与12.6个月),联合治疗组的切除/消融降期也显着高于单独化疗组 (p <0 .005),但具有相似的不良事件特征。
放射性栓塞需要经动脉递送与钇90 (Y90) 结合的放射性玻璃或树脂颗粒。在过去的十年中,Y90已成为越来越受欢迎的不可切除ICC的局部治疗手段。
回顾性研究报告经过中位数1到3次治疗以达到超过100戈瑞 (Gy) 的累积辐射剂量后的结果,产生的ORR在6%到50%之间,中位生存期长达29个月。

Cucchetti 等人,对九项观察性研究进行了荟萃回归分析,表明TARE最适合用于肿块形成的ICC患者(与浸润性ICC相比;中位OS,20与8个月)。
这些患者是初治患者(与之前接受过治疗的相比) ;中位OS,24与12个月)和同时给予全身治疗(与单独TARE相比;中位OS,20与6个月)。
TARE可以促进降期至切除,从而使3年生存率达到60%;切除术通常需要进行大肝切除术和血管重建,这可能与接近40%的围手术期发病率和25%的术后死亡率相关。
延长生存期的重要预测因素是体能状态、肿瘤负荷、RECIST反应和重复放射栓塞治疗。一种越来越流行的放射栓塞治疗改进方法是使用局限于小体积荷瘤肝脏的超高剂量,称为放射段切除术,其中对目标肿瘤提供高达400-800 Gy。
许多研究已经证明了这种方法的安全性,并且在各种肿瘤类型中,随着剂量的增加,完全病理性坏死的发生率越来越高。

最近的一项2期非随机研究报告了无法切除的ICC患者的 ORR(NCT 19122053),未经治疗、不可切除的ICC超过2厘米且功能状态和肝功能保持不变的患者中,共有41名患者接受了1次(65%)、2次 (30%) 或3次 (5%) 的Y90治疗,
向目标肝脏提供120 Gy的中位剂量,包括317 Gy的肿瘤和87 Gy到周围的薄壁组织;同时给予Gem和Cis的中位数6个周期。
研究显示Y90在3个月时产生了39%的ORR和98%的DCR,mPFS为14m,mOS为12m。这种令人鼓舞的结果促使一项基于Gem的化疗±Y90的随机研究开展。
ICC肝动脉输液泵化疗
HAI泵化疗是一种治疗策略,包括手术植入的皮下泵通过动脉循环将高剂量化疗药物直接输送到肝脏。
与上述TACE和其他经动脉疗法的基本原理类似,HAI实现了肝脏的生理和药理学隔离。由于泵化疗的基石氟尿苷 (FUDR) 的半衰期短且首过代谢率高,因此HAI 可以在肝脏中达到比使用药物可以达到的浓度高400倍的药物浓度。
HAI的作用被很好地描述为治疗结直肠癌肝转移患者的一种疗法,这是其最常见的适应症。最近,新出现的数据支持HAI化疗在晚期、不可切除的ICC患者中的作用。一项多机构研究比较了多灶性ICC患者接受HAI加FUDR与切除后的OS。
HAI和切除术之间的中位OS无统计学显着差异(20.3个月与18.9个月;p =0 .32)。HAI的5年OS率为12.5%(95% CI,7.4%-21.1%),而切除的5年OS率为20.7%(95% CI,14.4%-29.7%)。

接受HAI或切除术治疗的多病灶ICC患者OS降低的危险因素包括肿瘤直径(HR,1.74;95% CI,1.20-2.52;p <0.01)、病灶数量(HR,1.84;95% CI , 1.39-2.44;p <0 .01)和区域性淋巴结病(HR,1.51;95% CI,1.17-1.96;p <0 .01)。
这些数据强调了患者治疗选择的重要性,并表明对于多病灶的患者应严格评估手术切除的时机,缺乏生存优势反而增加复发率。
评估HAI治疗局部晚期ICC的前瞻性数据包括三项2期临床试验,这些试验报告的中位OS范围为25.0个月至29.5个月。
Cercek等人报告了一项最近的2期单臂研究,该研究评估了接受HAI和同步GEMOX治疗的无法切除的ICC患者的PFS。

该队列包括38名患者,其中大多数是初治患者 (92%)、双叶 (66%) 和/或多病灶 (55%) 肿瘤以及47%的门静脉淋巴结阳性。
尽管存在这些不利特征,HAI治疗仍有84%的DCR,部分缓解率为58%,并且有4名患者 (11%) 转为可进行手术切除。
主要终点显示中位PFS为11.8个月,6个月 PFS率为84%,中位OS为25个月。这些结果促使一项多中心、随机试验(NCT04891289)启动,以评估HAI与同步GEMOX在不可切除ICC中的疗效。
热消融
消融方式包括射频消融 (RFA)、微波消融 (MWA) 和冷冻消融。RFA是第一种被广泛采用的热消融方式,而MWA是一种更新的技术,由于消融时间大大缩短,可实现的消融区域更大,因此正在取代RFA。
一般来说,热消融的理想候选者需要肿瘤大小<5 cm(理想情况下<3 cm)并且位置不邻近关键结构,例如主要门脉三角区、胆囊或肠;然而,有一些技术,如水力解剖,可用于充分置换后者以安全地进行消融。
尽管热消融已被证明对不同器官的各种肿瘤具有很高的治愈潜力,但由于小尺寸的孤立性或寡灶性的ICC相对罕见,因此文献对胆管癌的支持性较差。

最近一项针对917名接受RFA或MWA治疗的患者的20项研究的系统回顾和荟萃分析报告称,1年时的汇总OS率为82.4%,3年时为42.1%,5年时为28.5%,主要并发症发生率为5.7%。1年、3年和5年的局部肿瘤进展率汇总时间分别为79.3%、59.5%和58.2%。
每项研究中治疗的平均肿瘤大小高达4.4厘米,肿瘤大小> 3厘米与较短的OS相关。更多的肿瘤病灶、高龄和肝硬化的存在也与较短的生存期相关。
在一项比较复发性ICC切除与消融后结果的研究中,<3 cm病灶的OS和无病生存率相似,但肝再切除后主要并发症显着增加。然而,对于>3 cm的病灶,重复肝切除术可延长OS。
因此,作者建议对<3 cm的复发病灶进行热消融,对>3 cm的病灶重复切除。与手术切除相比,热消融具有主要并发症发生率低、费用低、住院时间短等优点。
鉴于发生其他远处肝内转移的可能性很高,通过保留最大的肝实质,可以为后续病变提供更多治疗选择,这可能具有长期益处。值得注意的是,与切除术类似,由于ICC的浸润性,建议至少扩大1 cm的消融边缘以优化疾病控制。
放疗
放疗是局部非转移性疾病的一种选择,特别是对于不适合手术切除的患者,或对于出现转移性疾病患者的姑息治疗。
放疗方法包括化放疗或消融放疗(包括立体定向放疗)。消融辐射在有限数量的治疗中提供高剂量辐射,结合治疗计划优化目标覆盖范围,同时最大限度地减少对周围正常组织的剂量和治疗时的图像引导,以确保准确的治疗实施。
肝脏恶性肿瘤的一项挑战是固有的呼吸运动。在辐射模拟过程中,对运动进行评估,如果判断为显着,则可以使用多种呼吸管理技术进行管理,如腹部压缩、呼吸周期阶段的门控治疗或屏气技术。
在德克萨斯大学MD安德森癌症中心的一个研究系列中,79名无法手术的ICC患者接受了根治性放射治疗。
中位肿瘤大小为7.9厘米,大多数患者在放疗前接受了全身治疗。3-30次治疗中提供的辐射剂量在35到100 Gy之间。
结果显示患者中位OS为30个月,总体预后与辐射剂量高度相关,接受较高生物等效辐射剂量的患者的3年OS率为73%,在该队列中,未观察到显着的治疗相关毒性。
一项2期、多机构研究评估了92名经多学科审查确定为不可切除的HCC或ICC患者的质子放疗使用情况。患者接受了高达67.5 Gy的等效剂量,分15次。

ICC患者的中位肿瘤大小为6 cm,其中25%患有多发性肿瘤,30%患有血管血栓形成。在ICC队列中,2年局部控制率为94%,2年OS率为47%。
尽管数据有限,但放疗提供了一种潜在的选择,可以提供局部疾病控制和潜在的长期生存,且毒性适中。对于手术切除的不良或边缘候选者,考虑这种方法是合理的。
ICC肝移植
在引入肝移植 (LT) 作为终末期肝病患者的治疗选择后,LT的主要适应症之一是不可切除的恶性肝和胆管肿瘤。
然而,早期治疗结果伴随着高复发率和不良事件。在过去的几十年里,随着LT后结果的改善,LT的适应症已经扩展到HCC之外,特别是在对神经内分泌肝转移、肝门胆管癌和最近结直肠肝转移的最佳选择患者的治疗策略中。
在无法切除的 ICC患者中,LT传统上是禁忌的,因为结果不佳。贝克尔等估了LT在280 名ICC患者中的作用,显示1年OS率为74%,5年OS率为38%,显著低于HCC患者的LT结果,其中基准5年生存率为75%。

Sapisochin 等人报告了类似的发现,他们评估了27名ICC患者,他们在LT后1年、3年和5年的OS与接受LT治疗HCC的匹配患者相比更差( 78 %、66%和51%,分别与100%、98% 和 93%;p <0.001)。
患有多灶性或孤立性肿瘤>2 cm的患者的OS比患有较小肿瘤的ICC患者的OS更差(1年、3年和5年分别为80%、66%和61%)。
尽管LT治疗ICC后的结果在历史上是不可接受的,但最近的研究对这一前提提出了挑战:LT 联合新辅助化疗在精心评估的ICC患者中取得了相对令人满意的移植结果。

伦斯福德等人,发表12名无法切除的ICC患者,他们在至少6个月的基于Gem的化疗后接受LT及放疗后或稳定的结果。
该研究取得了积极的结果,1年的OS为100%(95% CI,100%–100%),3年的OS为83.3%(95% CI,27.3%–97.5%),5年的OS为 83.3%(95% CI,27.3%–97.5%),5年无复发生存率为50%(95% CI,11.1%–80.4%)。

在考虑进行LT时,患者选择仍然至关重要:接受LT的早期(孤立性肿瘤 <2 cm)ICC患者与晚期(多结节或孤立性肿瘤 >2 cm)ICC患者相比,早期ICC组的1年、3年和5年生存率分别为93%、84%和65%,而晚期ICC组分别为79%、50%和45%,( p=0 .02)。
在另一项研究中,McMillan等人发现,在接受新辅助化疗并证明疾病稳定6个月且无肝外疾病的局部晚期、不可切除的ICC患者中,接受LT的患者的1年、3年和5年总生存率为100%,71 %和57%。
因为这些结果来自回顾性分析和/或单中心、非随机研究,所以目前不被推荐LT作为ICC的治疗标准。目前,正在进行多项临床试验以确定LT对该人群的益处,并确定哪些的患者可能是LT的理想人选。
晚期ICC患者的全身治疗
全身化疗是治疗70%-80%不可切除和转移性ICC患者的关键策略。根据2010年报告的 ABC-02试验(NCT01926236)的结果,Gem和Cis的组合是首选的一线疗法。

在试验第3阶段,比较了Gem/Cis与单独使用Gem的OS和PFS,联合治疗组获益更佳:OS和PFS分别为11.7m vs 8.1m及8m vs 5m,DCR为81% vs72%。
在美国以外,第3期数据支持的替代策略是Gem加S-1 (Gem/S-1),该策疗效不劣于Gem/Cis(中位OS,Gem/Cis为13.4个月,Gem/S-1为15.1个月;HR,0.945;90% CI,0.78-1.15;p = 0.046;中位PFS分别为5.8个月vs 6.8个月HR,0.86;95% CI,0.70-1.07)。

已经发表的三联方案在局部晚期不可切除或转移性胆道癌(包括ICC)中的结果喜忧参半。
在 PRODIGE 38 AMEBICA试验(NCT02591030)中,奥沙利铂、伊立替康和输注氟尿嘧啶 (mFOLFIRINOX) 的组合在一线中不如 Gem/Cis。
在该随机 2/3 期试验中,6个月PFS(mFOLFIRINOX 组为44.6%,Gem/Cis 组为47.3%)、中位PFS(分别为 6.2个月和7.4个月)和中位OS(分别为 11.7个月和13.8个月) 在Gem/Cis 组更优。
最近在单臂2期试验中也报道了在一线中将白蛋白结合型紫杉醇添加到Gem/Cis中的结果:
Gem/Cis/Nab-紫杉醇的中位PFS为 11.8个月,中位OS为19.2个月,38名ICC患者亚组中观察到15 (44%)名患者ORR、14(41%)名患者SD,8(21%) 名无法切除的ICC 患者,最终接受了切除术,这表明该方案可能具有降低疾病分期以促进根治性手术的潜在作用。

与使用双重方案的历史经验相比,这些更好的结果推动了一项随机试验(NCT03768414)开展,以验证将白蛋白结合型紫杉醇添加到 Gem/Cis 中的益处。
ICC中的靶向治疗和免疫治疗
大规模肿瘤测序工作已经确定ICC中的存在大量基因组改变,尽管只有少数商业批准的疗法如FGFR2和IDH1抑制剂等,但人们对针对其他靶标(例如 BRAF、HER2 和 IDH2)的研究仍在进行。
10%-15%的ICC中检测到FGFR2融合并且倾向于出现在年轻患者中,25%的ICC患者中发现IDH1突变。
Abou-Alfa等人报告了一项2期非随机研究的结果,该研究评估了pemigatinib(培美替尼) 在146名基于Gem的化疗后进展的不可切除或转移性胆管癌患者中的作用。
该研究的主要终点是FGFR2融合/重排阳性患者的ORR,次要终点包括具有其他FGFR2改变的患者的ORR、DCR、PFS、OS、安全性和药代动力学。

Javle 等人评估了 BGJ398(infigratinib,英菲格拉替尼)在基于Gem化疗进展后不可切除/转移性FGFR2融合阳性ICC患者中的作用。
该2期非随机研究包括61名患者,主要终点是ORR,次要终点是PFS、DCR和不良事件。中位 PFS为5.8个月,ORR为15%,DCR为75%。

对于患有IDH1突变型ICC的患者,一项1期研究评估了 ivosidenib(艾伏尼布)单一疗法对 73名IDH1突变型胆管癌患者的疗效。
中位PFS为3.8个月(95% CI,3.6-7.3个月),6个月 PFS率为40.1%(95% CI,28.4%-51.6%),12个月PFS率为21.8%(95% CI,12.3%-33.0%),中位OS为13.8个月(95% CI,11.1-29.3个月)。
基于这种功效,Abou-Alfa 等人最近报道了 ClarIDHy 3期全球双盲随机试验(NCT02989857)在185 名IDH1患者中比较ivosidenib与安慰剂的结果。

与安慰剂相比,ivosidenib显着改善了PFS(2.7个月 [95% CI,1.6-4.2个月] 对比1.4个月[95% CI,1.4-1.6个月];HR 0.37;95% CI ,0.25-0.54 ; 单侧p< 0.0001);
然而,在意向治疗人群中,OS在数值上有所改善,但在统计学上没有显着改善(中位OS,ivosidenib组为10.3个月 [95% CI,7.8-12.4个月] vs. 安慰剂组为7.5个月[95% CI,4.8-11.1个月];HR,0.79 [95% CI,0.56-1.12];单侧p =0.09)。
这一结果被认为是由 57%的交叉率引起的;交叉调整后,安慰剂组的中位OS为5.1个月(95% CI,3.8-7.6个月;HR,0.49 [95% CI,0.34-0.70];单侧 p <0 .001 ) 。

此外,Ivosidenib的耐受性良好,只有2%的严重不良事件被认为与 ivosidenib 相关,并且没有与治疗相关的死亡。与安慰剂组相比,ivosidenib治疗组的生活质量没有下降。
近期免疫检查点抑制剂在ICC治疗中发挥了作用。先前对难治性疾病中单药或双药免疫检查点阻断的研究表明,10%–20%的患者有反应,但结果并未获得监管部门的批准;

TOPAZ-1 试验(NCT03875235)重新燃起了研究者的热情,这是一项比较Gem/Cis 加 durvalumab(度伐利尤单抗)与Gem/Cis加安慰剂的3期、随机、双盲、安慰剂对照研究。
durvalumab 组的中位OS为12.8个月,而Gem/Cis为11.5个月(HR,0.80;95% CI,0.66-0.97;p= 0.021),中位PFS为7.2个月,而 Gem/Cis 为5.7个月(HR,0.75;95% CI,0.64-0.89;p= 0.001),ORR为26.7%,Gem/Cis为18.7%。

尽管这些生存终点(尤其是OS)的绝对差异非常小,但生存曲线上的尾部数据令人振奋,高达25%的患者在2年时还活着,并且可能会看到前所未有的持久反应细胞毒性疗法。
其他有待解决的问题是该治疗策略是否对世界不同地区的患者存在疗效差异。不同地区登记的患者进行的预先指定的疗效亚组分析显示,亚洲的OS HR在数值上较低,但研究结果仍表明,无论地理位置如何,OS获益趋势都倾向于联合durvalumab。
结论
ICC是一种罕见且具有侵袭性的致命恶性肿瘤,其发病率逐年增加。尽管ICC 一直通过手术切除和对局部晚期或转移性疾病患者进行细胞毒性治疗,但近期多模式的治疗方式已经显示其具有改善患者的生存的趋势。

本文全面回顾了改善ICC患者预后的各种现代多模式疗法。对于局部可切除的ICC患者,切缘阴性的肝切除术和淋巴结清扫术后以卡培他滨辅助治疗应被视为标准治疗;
在不可切除或转移性ICC的患者中,包括局部区域治疗、三联全身方案、靶免治疗现在被临床医生越来越多地使用,并在经过优化选择的患者中取得了令人振奋的结果。
尽管目前的文献支持多模式治疗的方式以及这些替代方案的治疗,但未来的努力仍然至关重要,开发进一步改善ICC患者预后的更有效的治疗方法仍是努力的方向。
参考文献
Moris Dimitrios,Palta Manisha,Kim Charles et al. Advances in the treatment of intrahepatic cholangiocarcinoma: An overview of the current andfuture therapeutic landscape for clinicians.[J] .CA Cancer J Clin, 2023, 73: 198-222.
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。





发表评论
注册或登后即可发表评论
登录注册
全部评论(0)