2023-10-30

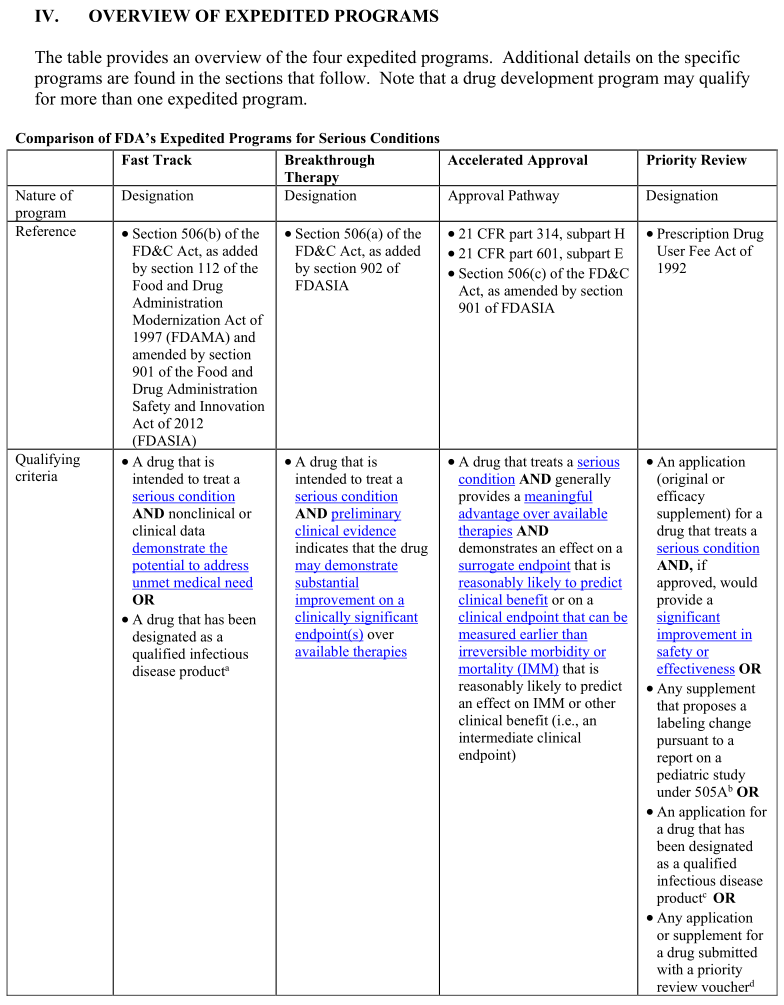
《二期三期临床试验实操训练营》模块一的学习目标是:掌握了FDA新药申请的四个加速通道的特点和区别,包括快速通道(Fast Track)、突破性疗法(Breakthrough Therapy)、优先审评(Priority Review),以及加速批准(Accelerated Approval)。

这四种加速通道的设立是为了帮助药物从开发快速推进到上市阶段,因此递交这些程序的申请项目多是在临床试验申请(IND)阶段。
汤黎教授详细讲解了这四个加速通道项目的申请条件和申请时间,可以获得的相应福利和特殊照顾。

罗晟教授的博士研究生作为特邀嘉宾,分享药企在申请加速审批项目时,会有哪些商业上的考量和注意事项:
1.一些资金雄厚的大型药企,为了在激烈的竞争中获得更多宝贵时间,通常会开展更多的临床试验,以积累更多成熟的安全性数据,甚至会跳过二期直接进入三期临床试验,以期在激烈的竞争中争取更多宝贵时间;
2. 加速审批的药物,很多情况下跟保险部门的沟通会比较困难,需要综合考虑药品的市场获利的情况;
3.药品审批非常复杂,FDA有自己的决策考量,成功的案例有它们的共性,我们可以作为参考,但每个研究本身有其独特的差异性,切不可被表面的“相似”所误导;
4.我们不能简单的认为只要满足FDA的申请流程和条件就足够了,相反,申请方要去说服FDA认可你的研究,这是一个“说服”和“协商”的过程;
5. 最重要的一点,我们不能把“怎么样设计出更容易获得FDA批准的研究”作为目标,获批的关键是一个医学问题,我们应该考虑的是:研究是不是一个紧急的、未被满足的医学需求?目前的标准治疗是什么?你的新药缩短了疗程?减少了给药难度?有更小的毒性?让病人痛苦更小...... ?这些进步才是有意义的、FDA能看的到、最有效的申请策略,当我们把这些医学问题说清楚了,就已经说服FDA一半了!
课程内容:
1. 如何申请快速通道
2. 如何申请突破性疗法
3. 对比分析快速通道 vs. 突破性疗法
4. 如何申请快速批准
5. 对比分析快速批准 vs.常规批准
6. 成功获得FDA加速批准项目的策略分析
7. 申请FDA四个加速通道应避免的错误
授课导师:
罗晟教授/美国杜克大学医学中心
汤黎教授/美国圣犹达儿童研究医院
课程试听:





添加小编微信

百度浏览 来源 : 国际临研
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。




发表评论
注册或登后即可发表评论
登录注册
全部评论(0)