2022年ASCO将于6月初在美国芝加哥举行,作为全球重磅的肿瘤年会之一, ASCO集聚了各大癌种的前沿进展。肝癌是我国第五大肿瘤,PD-1单抗开启了肝癌治疗的免疫时代,目前我国上市了7款PD-1单抗,本次入选ASCO肝癌治疗领域的有4篇涉及到国产PD-1单抗,在ASCO召开之际,让我们来看看国产PD-1单抗的肝癌成果!在肝癌治疗中常用的局部治疗手段为介入治疗(常用的有肝动脉栓塞化疗(TACE)、肝动脉灌注化疗(HAIC)等)、放疗、手术治疗等,多种治疗手段的联合是抗肿瘤治疗的有效策略之一,因此,越来越多的联合手段应用于临床。Poster Session-Abstract No.4106
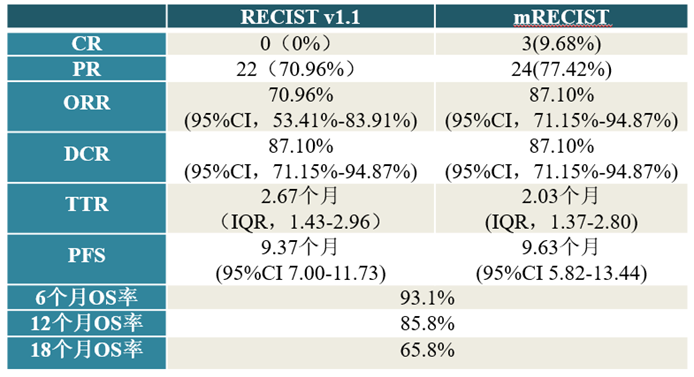
肝动脉灌注化疗(HAIC)联合阿帕替尼和卡瑞利珠单抗治疗BCLC C期肝细胞癌(HCC):一项前瞻性、单臂、II期试验(TRIPLET研究)【研究设计】该研究入组了初治的BCLC C期的HCC患者,接受HAIC(奥沙利铂85mg/m2、亚叶酸钙400mg/m2和氟尿嘧啶2500mg/m2 q3w)联合阿帕替尼(250mg qd)及卡瑞利珠单抗(200mg q3w)治疗6周期,随后采用卡瑞利珠单抗联合阿帕替尼维持治疗,直至疾病进展或出现不可耐受的毒性。主要终点为客观缓解率(ORR)。研究采用Simon 2阶段设计,第一阶段需纳入26例合格患者,当至少11例患者达到客观缓解,进入第二阶段的入组。【研究结果】第一阶段,根据RECIST v1.1和mRECIST标准评估,分别有16例和20例患者达到确认的ORR,顺利进入第二阶段的入组。从2020年4月13日至2022年1月31日,31例合格患者入组,29例可用于疗效分析评价。截至2022年1月31日,中位随访时间为18.07个月(95%CI14.10-22.04)。74.19%的患者发生≥3级不良事件(AE),其中最常见的AE为中性粒细胞减少(52.17%)、淋巴细胞减少(43.38%)、ALT和AST升高(各占30.43%和43.48%)【结论】HAIC、阿帕替尼和卡瑞利珠单抗三联治疗对BCLC C期HCC显示出有前景的临床获益和可接受的安全性。进一步的确证性随机对照试验即将进行。2021年ESMO公布了TRIPLET研究第一阶段的数据[1],26例患者在RECIST v1.1和mRECIST标准下的ORR分别为61.54%、76.92%,本次结果相较于去年,样本量进一步扩展到31例,同时ORR有所提升,也表明HAIC联合卡瑞利珠单抗和阿帕替尼的治疗显示出对BCLC C期HCC的良好临床获益,我们也期待后续的随机对照试验来进一步确证此治疗方式的有效性和安全性。同时入选的介入+免靶联合组合还有信迪利单抗,该研究聚焦于肝癌的转化治疗,也进一步将该组合前提至肝癌围手术期治疗。Poster Session-AbstractNo.4073肝动脉灌注化疗(HAIC)联合信迪利单抗和贝伐珠单抗生物类似药(IBI305)治疗初治不可切除的肝细胞癌(HCC):一项前瞻性、单臂、II期试验。【研究设计】该研究入组了中国肝癌分期(CNLC)IIb-IIIb期、既往未接受过全身治疗、Child-Pugh A或B级、ECOG PS 0或1的肝细胞癌患者,接受FOLOFOX HAIC联合信迪利单抗(200 mg,每3周1次,4个周期)和IBI305(7.5 mg/kg,每3周1次,3个周期)。主要终点是根据mRECIST评估的客观缓解率(ORR)。次要终点为手术转化率、pCR率和R0切除率。【研究结果】2021年5月至2021年9月期间,共入组30例合格患者,其中 23例(76.7%)为乙型肝炎患者和5例(16.7%)丙型肝炎患者。最常见的TRAE包括高血压(23.3%)、皮疹(16.7%)、肝功能异常(10.0%)。未观察到3-4级TRAE。值得注意的是,在接受手术治疗的患者中,1例发生1级胆瘘,1例发生肝衰竭,最终导致死亡。【结论】HAIC联合信迪利单抗和IBI305治疗不可切除的初治晚期肝细胞癌具有良好的ORR、R0手术转换率和pCR率,安全性可控。肝癌转化治疗目前并无标准治疗手段,局部联合系统治疗为一种可行策略。2022ASCO GI公布了信迪利单抗联合仑伐替尼用于肝癌转化治疗的结果[2],ORR为38%,转化率为34%,但未公布详细的手术及术后评估。本次结果,在免靶的基础上联合HAIC治疗,ORR(66.7%)和转化率[初步测算为46.7%(14/30)]进一步提升,同时获得了良好的R0切除率和pCR率,也表明HAIC+免靶联合作为肝癌转化治疗的可行性。Poster Session-AbstractNo.4071
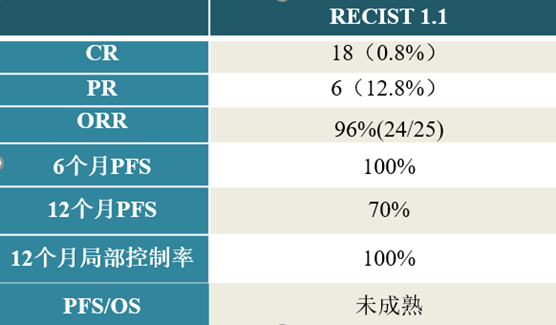
立体定向放射治疗(SBRT)联合信迪利单抗治疗复发性或寡转移性肝细胞癌(HCC)的II期研究【研究设计】该研究入组了Child-Pugh A级、ECOG PS≤1的复发性或寡转移性HCC(定义为≤5个转移/复发病灶)患者,接受信迪利单抗(200mg IV Q3W)治疗至12个月、疾病进展、出现不可耐受的毒性或退出研究。从第1周期第1天开始对所有病灶进行SBRT。主要终点为根据RECIST 1.1评估的无进展生存期(PFS),次要终点包括安全性、客观缓解率(ORR)、疾病控制率(DCR)和总生存期(OS)。【研究结果】截止到2021年12月28日,25例患者的32处病灶接受了SBRT+信迪利单抗治疗。大多数患者既往接受过≥2种局部治疗。14例患者(56%)发生治疗相关不良事件(TRAE)。最常见的TRAE为皮疹(16%)、血小板计数降低(12%)、肌炎(8%)。1例患者(4%)发生3级TRAE(肌炎)。未发生4-5级TRAE。TRAE导致6例患者(24%)停药。SAE为心肌炎(1例患者1级)、病毒性肝炎(1例患者3级)和上消化道出血(1例患者3级)。【结论】在复发性或寡转移性HCC患者中,SBRT联合信迪利单抗可耐受,并显示令人鼓舞的ORR(96%)。需要更长时间的随访来进一步评价疗效和安全性。SBRT是一种治疗寡转移灶的有效方法,放疗的应用,可以对局部病灶产生良好的控制作用,该研究的初步结果已于2021 EASL肝癌峰会发布[3],入组的20例患者中有16例患者可评估疗效,ORR为93.8%,6个月和12个月的PFS率分别为100%、71.4%,12个月的局部控制率为100%。本次ASCO更新了入组数据,总体疗效相似,期待着更长时间的随访来确认其疗效和安全性。目前PD-1单抗已成为肝癌晚期的标准治疗手段,国产PD-1中,卡瑞利珠单抗、替雷利珠单抗均获得了肝癌二线治疗单药适应症。本次ASCO中替雷利珠单抗公布了RATIONALE-208中既往接受过索拉非尼(SOR)或仑伐替尼(LEN)治疗人群的疗效和安全性。Poster Session-AbstractNo.4072
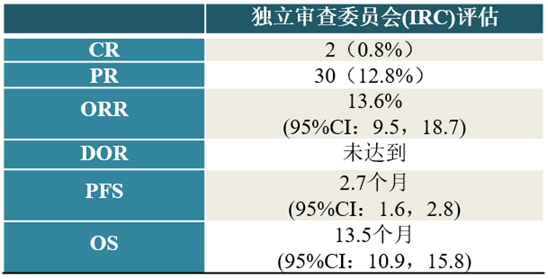
RATIONALE-208研究中替雷利珠单抗在既往接受过索拉非尼(SOR)或仑伐替尼(LEN)治疗的晚期肝细胞癌(HCC)患者(pts)中的临床结局【方法】既往接受过≥1线晚期HCC全身治疗的患者接受替雷利珠单抗200 mg静脉给药,每3周一次。在既往接受过SOR/LEN治疗的患者中,评价了独立审查委员会(IRC)评估的客观缓解率(ORR)(ORRIRC)、IRC评估的缓解持续时间(DORIRC)、IRC评估的无进展生存期(PFSIRC)、总生存期(OS)和安全性。【结果】截至2020年2月,入组了249例患者,235例患者既往接受过SOR/LEN治疗,中位随访持续时间为12.5个月。替雷利珠单抗在既往接受过SOR/LEN治疗的患者中耐受良好(表),最常见的治不良事件为天冬氨酸氨基转移酶升高(n=70;28.1%)和丙氨酸氨基转移酶升高(n=52;20.9%)。【结论】晚期HCC患者二线和三线治疗的有效选择有限,且存在未满足的医疗需求,该分析表明,替雷利珠单抗在既往接受过SOR/LEN全身治疗的晚期HCC患者中具有临床活性且耐受性良好。RATIONALE-208研究是一项开放标签、全球多中心、Ⅱ期临床研究,研究结果表明替雷利珠单抗单药在HCC二线治疗中良好的疗效和安全性,ORR为13.3%、PFS为2.7个月、OS为13.2个月。本次ASCO将既往接受过SOR/LEN全身治疗的晚期HCC患者数据更新,进一步巩固了替雷利珠单抗二线治疗的地位。
[1] Tianqi Zhang, et al. 2021 ESMO. 946P.[2] Lijun Wang,et al. ASCO GI 2022. Poster 449[3] Chen Y X,et al.2021 EASL Digital Liver Cancer Summit, O04.
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。









发表评论
注册或登后即可发表评论
登录注册
全部评论(0)